よむ、つかう、まなぶ。
資料1-4 申請技術の概要及びロードマップ (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38038.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第159回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
薬事承認申請までのロードマップ(先進⇒治験)
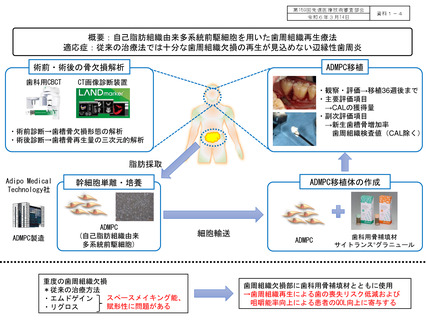
先進医療技術名:自己脂肪組織由来多系統前駆細胞を用いた歯周組織再生療法
試験薬または試験機器:脂肪組織由来多系統前駆細胞(製品名:AMT-102)
先進医療での適応症:従来の治療法では十分な歯周組織欠損の再生が見込めない辺縁性歯周炎
先進医療
臨床研究
・試験名:自己脂肪組織由
来幹細胞を用いた新しい歯
周組織再生療法開発
・試験デザイン:
単群有効性探索試験
・期間:2012年~2018年
・被験者数:12名
・結果の概要:12名すべて
の症例において歯周組織
再生(歯槽骨の再生および
臨床的アタッチメントの獲
得)が認められ、重篤な有
害事象は観察されなかった。
・試験名:自己脂肪組織由来多系統前駆細胞を用いた歯
周組織再生療法
・試験デザイン:
多施設単群有効性探索試験
・期間:2024年~2028年
・被験者数:30名
・主要評価項目:臨床的アタッチメントの獲得量
・副次評価項目:新生歯槽骨の増加量・歯周組織検査値の
経時的変化
当該先進医療における
選択基準:20歳以上で重度歯周炎と診断された
歯を有する患者
除外基準:評価に支障をきたす補綴物等が存在す
る、あるいは全身的な問題を有する患者
予想される有害事象:歯周外科手術に伴う局所麻
酔に対する過敏症、口腔内感染症、歯肉の炎症等
先進医療もし
くは治験
・先行研究の結果等
を踏まえ試験デザイ
ンを検討
海外での現状
薬事承認:米国(有・無)、英国(有・無)、フランス(有・無)、ドイツ(有・無)、
カナダ(有・無)、オーストラリア(有・無)、その他(有・無 有ならば国名: )
ガイドライン記載:(有・無)
進行中の臨床試験(有・無)
本邦での現状
ガイドライン記載:(有・無)
進行中の臨床試験(有・無)
薬
事
承
認
申
請
先進医療技術名:自己脂肪組織由来多系統前駆細胞を用いた歯周組織再生療法
試験薬または試験機器:脂肪組織由来多系統前駆細胞(製品名:AMT-102)
先進医療での適応症:従来の治療法では十分な歯周組織欠損の再生が見込めない辺縁性歯周炎
先進医療
臨床研究
・試験名:自己脂肪組織由
来幹細胞を用いた新しい歯
周組織再生療法開発
・試験デザイン:
単群有効性探索試験
・期間:2012年~2018年
・被験者数:12名
・結果の概要:12名すべて
の症例において歯周組織
再生(歯槽骨の再生および
臨床的アタッチメントの獲
得)が認められ、重篤な有
害事象は観察されなかった。
・試験名:自己脂肪組織由来多系統前駆細胞を用いた歯
周組織再生療法
・試験デザイン:
多施設単群有効性探索試験
・期間:2024年~2028年
・被験者数:30名
・主要評価項目:臨床的アタッチメントの獲得量
・副次評価項目:新生歯槽骨の増加量・歯周組織検査値の
経時的変化
当該先進医療における
選択基準:20歳以上で重度歯周炎と診断された
歯を有する患者
除外基準:評価に支障をきたす補綴物等が存在す
る、あるいは全身的な問題を有する患者
予想される有害事象:歯周外科手術に伴う局所麻
酔に対する過敏症、口腔内感染症、歯肉の炎症等
先進医療もし
くは治験
・先行研究の結果等
を踏まえ試験デザイ
ンを検討
海外での現状
薬事承認:米国(有・無)、英国(有・無)、フランス(有・無)、ドイツ(有・無)、
カナダ(有・無)、オーストラリア(有・無)、その他(有・無 有ならば国名: )
ガイドライン記載:(有・無)
進行中の臨床試験(有・無)
本邦での現状
ガイドライン記載:(有・無)
進行中の臨床試験(有・無)
薬
事
承
認
申
請