よむ、つかう、まなぶ。
議題3 患-3患者申出療養の終了に伴う取下げについて (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40866.html |
| 出典情報 | 患者申出療養評価会議(第51回 6/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
患
-
3
6 . 6 . 2 0
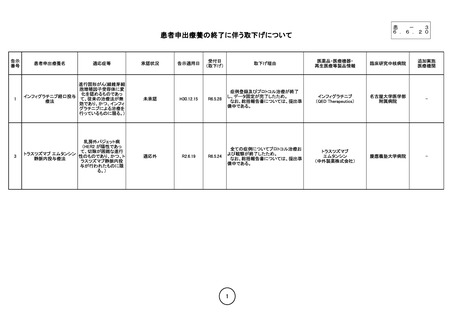
患者申出療養の終了に伴う取下げについて
告示
番号
承認状況
告示適用日
受付日
(取下げ)
取下げ理由
医薬品・医療機器・
再生医療等製品情報
臨床研究中核病院
追加実施
医療機関
1
進行固形がん(線維芽細
胞増殖因子受容体に変
化を認めるものであっ
インフィグラチニブ経口投与
て、従来の治療法が無
療法
効であり、かつ、インフィ
グラチニブによる治療を
行っているものに限る。)
未承認
H30.12.15
R6.5.28
症例登録及びプロトコル治療が終了
し、データ固定が完了したため。
なお、総括報告書については、提出準
備中である。
インフィグラチニブ
(QED Therapeutics)
名古屋大学医学部
附属病院
3
乳房外パジェット病
(HER2 が陽性であっ
て、切除が困難な進行
トラスツズマブ エムタンシン
性のものであり、かつ、ト
静脈内投与療法
ラスツズマブ静脈内投
与が行われたものに限
る。)
適応外
R2.6.19
R6.5.24
全ての症例についてプロトコル治療お
よび観察が終了したため。
なお、総括報告書については、提出準
備中である。
トラスツズマブ
エムタンシン
(中外製薬株式会社)
慶應義塾大学病院
患者申出療養名
適応症等
1
-
3
6 . 6 . 2 0
患者申出療養の終了に伴う取下げについて
告示
番号
承認状況
告示適用日
受付日
(取下げ)
取下げ理由
医薬品・医療機器・
再生医療等製品情報
臨床研究中核病院
追加実施
医療機関
1
進行固形がん(線維芽細
胞増殖因子受容体に変
化を認めるものであっ
インフィグラチニブ経口投与
て、従来の治療法が無
療法
効であり、かつ、インフィ
グラチニブによる治療を
行っているものに限る。)
未承認
H30.12.15
R6.5.28
症例登録及びプロトコル治療が終了
し、データ固定が完了したため。
なお、総括報告書については、提出準
備中である。
インフィグラチニブ
(QED Therapeutics)
名古屋大学医学部
附属病院
3
乳房外パジェット病
(HER2 が陽性であっ
て、切除が困難な進行
トラスツズマブ エムタンシン
性のものであり、かつ、ト
静脈内投与療法
ラスツズマブ静脈内投
与が行われたものに限
る。)
適応外
R2.6.19
R6.5.24
全ての症例についてプロトコル治療お
よび観察が終了したため。
なお、総括報告書については、提出準
備中である。
トラスツズマブ
エムタンシン
(中外製薬株式会社)
慶應義塾大学病院
患者申出療養名
適応症等
1