よむ、つかう、まなぶ。
資料3-5 医薬関係者からの副作用報告等の状況[2.4MB] (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
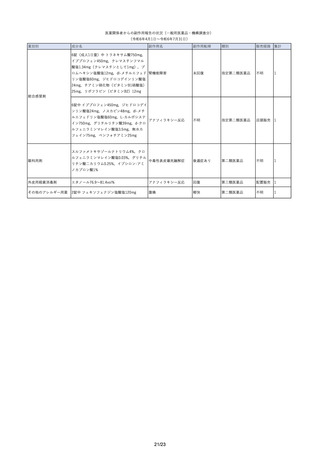
2.要指導医薬品の国内副作用報告の状況について
(機構調査分)
(令和6年4月1日から令和6年7月 31 日までの報告受付分)
<報告無し>
要指導医薬品の国内副作用報告の状況(機構調査分)についての注意事項
1) 副作用報告については、医薬品医療機器総合機構の調査担当分(以下、「機構調査
分」という。)の令和6年8月1日時点の情報を調査が完了している症例と調査中の症
例を区別せずとりまとめたものであり、個別に医薬品との関連性を評価したものでは
ない。
2) 機構調査分とは、報告者から被疑薬の製造販売業者への情報提供がなされなかっ
た重篤及び死亡症例が該当する。重篤症例とは、報告者又は医薬品医療機器総合
機構の調査により重篤と判断されたものである。
3) 令和6年4月1日から令和6年7月 31 日(以下「本報告期間」という。)に新たに報告さ
れたもののうち、機構調査分について示したものである。
4) 被疑薬と副作用名別の件数を示したものであり、1症例で複数の副作用を発現する
場合や1症例に複数の被疑薬を含む場合があるので、集計値の合計は報告症例数
にならない。
5) 報告者が本報告期間中に報告した後に、本報告期間中に医薬品医療機器総合機構
の調査により因果関係が否定された場合や重篤性が変更となり報告対象外となった
場合等、件数から除外されている。
6) 副作用名は、用語の統一のため、ICH国際医薬用語集日本語版(MedDRA/J)に収
載されている用語(Preferred Term:基本語)で表示している。
19/23
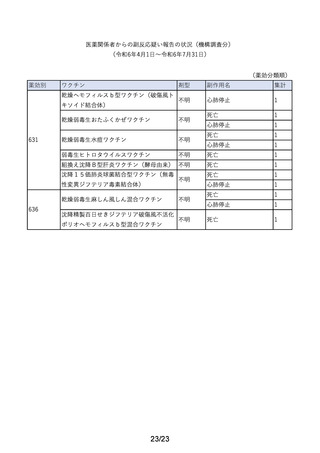
(機構調査分)
(令和6年4月1日から令和6年7月 31 日までの報告受付分)
<報告無し>
要指導医薬品の国内副作用報告の状況(機構調査分)についての注意事項
1) 副作用報告については、医薬品医療機器総合機構の調査担当分(以下、「機構調査
分」という。)の令和6年8月1日時点の情報を調査が完了している症例と調査中の症
例を区別せずとりまとめたものであり、個別に医薬品との関連性を評価したものでは
ない。
2) 機構調査分とは、報告者から被疑薬の製造販売業者への情報提供がなされなかっ
た重篤及び死亡症例が該当する。重篤症例とは、報告者又は医薬品医療機器総合
機構の調査により重篤と判断されたものである。
3) 令和6年4月1日から令和6年7月 31 日(以下「本報告期間」という。)に新たに報告さ
れたもののうち、機構調査分について示したものである。
4) 被疑薬と副作用名別の件数を示したものであり、1症例で複数の副作用を発現する
場合や1症例に複数の被疑薬を含む場合があるので、集計値の合計は報告症例数
にならない。
5) 報告者が本報告期間中に報告した後に、本報告期間中に医薬品医療機器総合機構
の調査により因果関係が否定された場合や重篤性が変更となり報告対象外となった
場合等、件数から除外されている。
6) 副作用名は、用語の統一のため、ICH国際医薬用語集日本語版(MedDRA/J)に収
載されている用語(Preferred Term:基本語)で表示している。
19/23