よむ、つかう、まなぶ。
議題4 患-4患者申出療養の終了に伴う取下げについて (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45823.html |
| 出典情報 | 患者申出療養評価会議(第55回 11/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
患
-
4
6 .1 1. 2 1
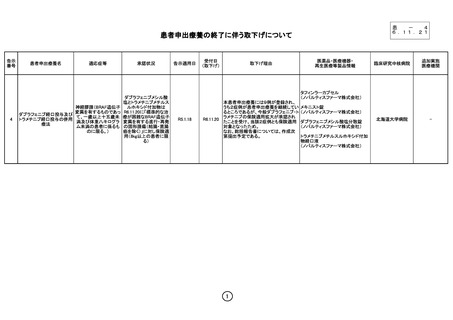
患者申出療養の終了に伴う取下げについて
告示
番号
4
患者申出療養名
適応症等
承認状況
ダブラフェニブメシル酸
塩とトラメチニブメチルス
神経膠腫(BRAF遺伝子 ルホキシド付加物は
変異を有するものであっ R6.11.20に「標準的な治
ダブラフェニブ経口投与及び
て、一歳以上十五歳未 療が困難なBRAF遺伝子
トラメチニブ経口投与の併用
満及び体重八キログラ 変異を有する進行・再発
療法
ム未満の患者に係るも の固形腫瘍(結腸・直腸
のに限る。)
癌を除く)」に対し保険適
用(8kg以上の患者に限
る)
告示適用日
受付日
(取下げ)
取下げ理由
医薬品・医療機器・
再生医療等製品情報
臨床研究中核病院
追加実施
医療機関
北海道大学病院
タフィンラーカプセル
(ノバルティスファーマ株式会社)
R5.1.18
本患者申出療養には9例が登録され、
うち2症例が患者申出療養を継続してい メキニスト錠
るところであるが、今般ダブラフェニブ・ト (ノバルティスファーマ株式会社)
ラメチニブの保険適用拡大が承認され
R6.11.20
たことを受け、当該2症例とも保険適用 ダブラフェニブメシル酸塩分散錠
対象となったため。
(ノバルティスファーマ株式会社)
なお、総括報告書については、作成次
第提出予定である。
トラメチニブメチルスルホキシド付加
物経口液
(ノバルティスファーマ株式会社)
1
-
4
6 .1 1. 2 1
患者申出療養の終了に伴う取下げについて
告示
番号
4
患者申出療養名
適応症等
承認状況
ダブラフェニブメシル酸
塩とトラメチニブメチルス
神経膠腫(BRAF遺伝子 ルホキシド付加物は
変異を有するものであっ R6.11.20に「標準的な治
ダブラフェニブ経口投与及び
て、一歳以上十五歳未 療が困難なBRAF遺伝子
トラメチニブ経口投与の併用
満及び体重八キログラ 変異を有する進行・再発
療法
ム未満の患者に係るも の固形腫瘍(結腸・直腸
のに限る。)
癌を除く)」に対し保険適
用(8kg以上の患者に限
る)
告示適用日
受付日
(取下げ)
取下げ理由
医薬品・医療機器・
再生医療等製品情報
臨床研究中核病院
追加実施
医療機関
北海道大学病院
タフィンラーカプセル
(ノバルティスファーマ株式会社)
R5.1.18
本患者申出療養には9例が登録され、
うち2症例が患者申出療養を継続してい メキニスト錠
るところであるが、今般ダブラフェニブ・ト (ノバルティスファーマ株式会社)
ラメチニブの保険適用拡大が承認され
R6.11.20
たことを受け、当該2症例とも保険適用 ダブラフェニブメシル酸塩分散錠
対象となったため。
(ノバルティスファーマ株式会社)
なお、総括報告書については、作成次
第提出予定である。
トラメチニブメチルスルホキシド付加
物経口液
(ノバルティスファーマ株式会社)
1