よむ、つかう、まなぶ。
資料4 副反応疑い報告様式の改訂について[372KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00138.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第106回 4/14)医薬品等安全対策部会安全対策調査会(令和7年度第1回 4/14)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
報告先:(独)医薬品医療機器総合機構
(別紙様式1)
FAX番号:0120-176-146(各種ワクチン共通)
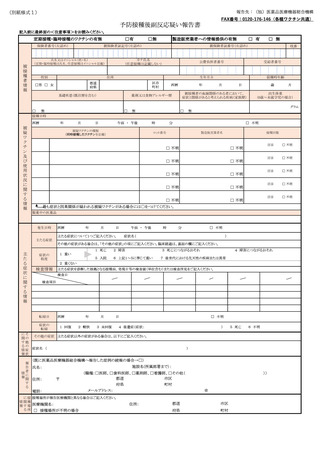
予防接種後副反応疑い報告書
記入前に最終面の<注意事項>をお読みください。
定期接種・臨時接種のワクチンの有無
保険者番号(左詰め)
被
接
種
者
情
報
□有
□無
製造販売業者への情報提供の有無
被保険者証記号(左詰め)
性別
□男 □ 女
枝番
公費負担者番号
住所
受給者番号
生年月日
区市
町村
都道
府県
基礎疾患(既往歴を含む)
□ 無
被保険者証番号(左詰め)
カナ氏名
(任意接種は記載しない)
氏名又はイニシャル(姓・名)
(定期・臨時接種は氏名、任意接種はイニシャル記載)
□ 有
西暦
年
接種時年齢
月
日
歳
被接種者の血縁関係のある者において、
症状と関係があると考えられる疾病(家族歴)
薬剤又は食物アレルギー歴
月
出生体重
(0歳~未就学児の場合)
グラム
グラム
□
無
接種日時
□
西暦
被
疑
ワ
ク
チ
ン
及
び
使
用
状
況
に
関
す
る
情
報
年
月
日
無
午前 ・ 午後
□
時
被疑ワクチンの種類
(同時接種したワクチンを記載)
無
分
□ 不明
ロット番号
製造販売業者名
接種回数
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
最も症状と因果関係が疑われる被疑ワクチンがある場合には〇をつけてください。
服薬中の医薬品
発生日時
西暦
年
月
日
主たる症状について1つご記入ください。
午前 ・ 午後
時
分
□ 不明
症状名(
)
主たる症状
その他の症状がある場合は、「その他の症状」の項にご記入ください。臨床経過は、裏面の欄にご記入ください。
主
た
る
症
状
に
関
す
る
情
報
1 死亡
2 障害
3 死亡につながるおそれ
4 障害につながるおそれ
5 入院
6 上記1~5に準じて重い
7 後世代における先天性の疾病または異常
1 重い
症状の
程度
2 重くない
検査情報
主たる症状を診断した根拠となる接種前、発現日等の検査値(単位含む)または検査所見をご記入ください。
検査日
検査項目
転帰日
西暦
症状の
転帰
1 回復
年
2 軽快
月
日
3 未回復
□ 不明
4 後遺症(症状:
)
にそ
その他の症状 主たる症状以外の症状がある場合は、以下にご記入ください。
関の
す他
るの
情 症 症状名 (
報状
5 死亡
6 不明
)
(既に医薬品医療機器総合機構へ報告した症例の続報の場合→□)
報
告 氏名:
者
情
に
報
関 住所:
す
る
電話:
施設名(所属部署まで):
〒
(職種:□医師、□歯科医師、□薬剤師、□看護師、□その他(
都道
市区
府県
町村
メールアドレス:
に 接 接種場所が報告医療機関と異なる場合はご記入ください。
情関種
報 す 場 医療機関名:
る 所 □ 接種場所が不明の場合
))
@
住所:
都道
市区
府県
町村
(別紙様式1)
FAX番号:0120-176-146(各種ワクチン共通)
予防接種後副反応疑い報告書
記入前に最終面の<注意事項>をお読みください。
定期接種・臨時接種のワクチンの有無
保険者番号(左詰め)
被
接
種
者
情
報
□有
□無
製造販売業者への情報提供の有無
被保険者証記号(左詰め)
性別
□男 □ 女
枝番
公費負担者番号
住所
受給者番号
生年月日
区市
町村
都道
府県
基礎疾患(既往歴を含む)
□ 無
被保険者証番号(左詰め)
カナ氏名
(任意接種は記載しない)
氏名又はイニシャル(姓・名)
(定期・臨時接種は氏名、任意接種はイニシャル記載)
□ 有
西暦
年
接種時年齢
月
日
歳
被接種者の血縁関係のある者において、
症状と関係があると考えられる疾病(家族歴)
薬剤又は食物アレルギー歴
月
出生体重
(0歳~未就学児の場合)
グラム
グラム
□
無
接種日時
□
西暦
被
疑
ワ
ク
チ
ン
及
び
使
用
状
況
に
関
す
る
情
報
年
月
日
無
午前 ・ 午後
□
時
被疑ワクチンの種類
(同時接種したワクチンを記載)
無
分
□ 不明
ロット番号
製造販売業者名
接種回数
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
回目
□ 不明
最も症状と因果関係が疑われる被疑ワクチンがある場合には〇をつけてください。
服薬中の医薬品
発生日時
西暦
年
月
日
主たる症状について1つご記入ください。
午前 ・ 午後
時
分
□ 不明
症状名(
)
主たる症状
その他の症状がある場合は、「その他の症状」の項にご記入ください。臨床経過は、裏面の欄にご記入ください。
主
た
る
症
状
に
関
す
る
情
報
1 死亡
2 障害
3 死亡につながるおそれ
4 障害につながるおそれ
5 入院
6 上記1~5に準じて重い
7 後世代における先天性の疾病または異常
1 重い
症状の
程度
2 重くない
検査情報
主たる症状を診断した根拠となる接種前、発現日等の検査値(単位含む)または検査所見をご記入ください。
検査日
検査項目
転帰日
西暦
症状の
転帰
1 回復
年
2 軽快
月
日
3 未回復
□ 不明
4 後遺症(症状:
)
にそ
その他の症状 主たる症状以外の症状がある場合は、以下にご記入ください。
関の
す他
るの
情 症 症状名 (
報状
5 死亡
6 不明
)
(既に医薬品医療機器総合機構へ報告した症例の続報の場合→□)
報
告 氏名:
者
情
に
報
関 住所:
す
る
電話:
施設名(所属部署まで):
〒
(職種:□医師、□歯科医師、□薬剤師、□看護師、□その他(
都道
市区
府県
町村
メールアドレス:
に 接 接種場所が報告医療機関と異なる場合はご記入ください。
情関種
報 す 場 医療機関名:
る 所 □ 接種場所が不明の場合
))
@
住所:
都道
市区
府県
町村