よむ、つかう、まなぶ。
資料 先-1○先進医療Bに係る新規技術の科学的評価等について (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00055.html |
| 出典情報 | 先進医療会議(第119回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先
-
1
5.3 .2
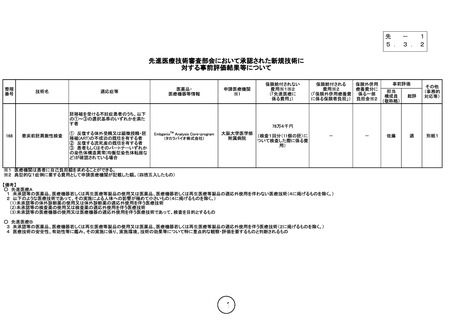
先進医療技術審査部会において承認された新規技術に
対する事前評価結果等について
整理
番号
技術名
適応症等
医薬品・
医療機器等情報
申請医療機関
※1
EmbgenixTM Analysis Core-program
(タカラバイオ株式会社)
大阪大学医学部
附属病院
胚移植を受ける不妊症患者のうち、以下
の①~③の選択基準のいずれかを満た
す者
168
着床前胚異数性検査
① 反復する体外受精又は顕微授精・胚
移植(ART)の不成功の既往を有する者
② 反復する流死産の既往を有する者
③ 患者もしくはそのパートナーいずれか
の染色体構造異常(均衡型染色体転座な
ど)が確認されている場合
保険給付されない
費用※1※2
(「先進医療に
係る費用」)
事前評価
保険給付される
保険外併用
費用※2
療養費分に
担当
(「保険外併用療養費
係る一部
総評
構成員
に係る保険者負担」) 負担金※2 (敬称略)
その他
(事務的
対応等)
78万4千円
(検査1回分(11個の胚)に
ついて検査した際に係る費
用)
-
※1 医療機関は患者に自己負担額を求めることができる。
※2 典型的な1症例に要する費用として申請医療機関が記載した額。(四捨五入したもの)
【備考】
○ 先進医療A
1 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴わない医療技術(4に掲げるものを除く。)
2 以下のような医療技術であって、その実施による人体への影響が極めて小さいもの(4に掲げるものを除く。)
(1)未承認等の体外診断薬の使用又は体外診断薬の適応外使用を伴う医療技術
(2)未承認等の検査薬の使用又は検査薬の適応外使用を伴う医療技術
(3)未承認等の医療機器の使用又は医療機器の適応外使用を伴う医療技術であって、検査を目的とするもの
○ 先進医療B
3 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴う医療技術(2に掲げるものを除く。)
4 医療技術の安全性、有効性等に鑑み、その実施に係り、実施環境、技術の効果等について特に重点的な観察・評価を要するものと判断されるもの
1
-
佐藤
適
別紙1
-
1
5.3 .2
先進医療技術審査部会において承認された新規技術に
対する事前評価結果等について
整理
番号
技術名
適応症等
医薬品・
医療機器等情報
申請医療機関
※1
EmbgenixTM Analysis Core-program
(タカラバイオ株式会社)
大阪大学医学部
附属病院
胚移植を受ける不妊症患者のうち、以下
の①~③の選択基準のいずれかを満た
す者
168
着床前胚異数性検査
① 反復する体外受精又は顕微授精・胚
移植(ART)の不成功の既往を有する者
② 反復する流死産の既往を有する者
③ 患者もしくはそのパートナーいずれか
の染色体構造異常(均衡型染色体転座な
ど)が確認されている場合
保険給付されない
費用※1※2
(「先進医療に
係る費用」)
事前評価
保険給付される
保険外併用
費用※2
療養費分に
担当
(「保険外併用療養費
係る一部
総評
構成員
に係る保険者負担」) 負担金※2 (敬称略)
その他
(事務的
対応等)
78万4千円
(検査1回分(11個の胚)に
ついて検査した際に係る費
用)
-
※1 医療機関は患者に自己負担額を求めることができる。
※2 典型的な1症例に要する費用として申請医療機関が記載した額。(四捨五入したもの)
【備考】
○ 先進医療A
1 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴わない医療技術(4に掲げるものを除く。)
2 以下のような医療技術であって、その実施による人体への影響が極めて小さいもの(4に掲げるものを除く。)
(1)未承認等の体外診断薬の使用又は体外診断薬の適応外使用を伴う医療技術
(2)未承認等の検査薬の使用又は検査薬の適応外使用を伴う医療技術
(3)未承認等の医療機器の使用又は医療機器の適応外使用を伴う医療技術であって、検査を目的とするもの
○ 先進医療B
3 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴う医療技術(2に掲げるものを除く。)
4 医療技術の安全性、有効性等に鑑み、その実施に係り、実施環境、技術の効果等について特に重点的な観察・評価を要するものと判断されるもの
1
-
佐藤
適
別紙1