よむ、つかう、まなぶ。
薬-4別添○関係業界からの意見聴取について (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00065.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第203回 7/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
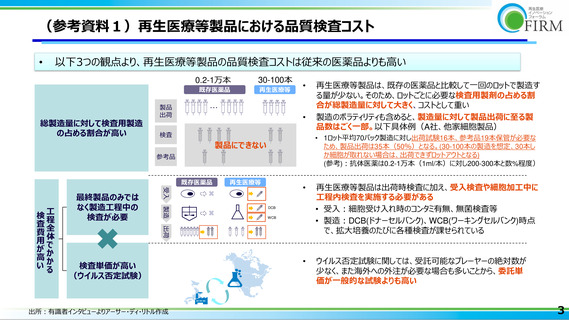
(参考資料1)再生医療等製品における品質検査コスト
•
以下3つの観点より、再生医療等製品の品質検査コストは従来の医薬品よりも高い
総製造量に対して検査用製造
の占める割合が高い
製品
出荷
0.2-1万本
30-100本
既存医薬品
再生医療等
•
…
•
検査
• 1ロット平均70バック製造に対し出荷試験16本、参考品19本保管が必要な
ため、製品出荷は35本(50%)となる。(30-100本の製造を想定、30本し
か細胞が取れない場合は、出荷できずロットアウトとなる)
(参考):抗体医薬は0.2-1万本(1ml/本)に対し200-300本と数%程度)
製品にできない
参考品
既存医薬品
再生医療等
受入
製造
•
再生医療等製品は出荷時検査に加え、受入検査や細胞加工中に
工程内検査を実施する必要がある
• 受入:細胞受け入れ時のコンタミ有無、無菌検査等
• 製造:DCB(ドナーセルバンク)、WCB(ワーキングセルバンク)時点
で、拡大培養のたびに各種検査が課せられている
•
ウイルス否定試験に関しては、受託可能なプレーヤーの絶対数が
少なく、また海外への外注が必要な場合も多いことから、委託単
価が一般的な試験よりも高い
DCB
WCB
出荷
検工
査程
費全
用体
がで
高か
いか
る
最終製品のみでは
なく製造工程中の
検査が必要
検査単価が高い
(ウイルス否定試験)
出所:有識者インタビューよりアーサー・ディ・リトル作成
再生医療等製品は、既存の医薬品と比較して一回のロットで製造す
る量が少ない。そのため、ロットごとに必要な検査用製剤の占める割
合が総製造量に対して大きく、コストとして重い
製造のボラティリティも含めると、製造量に対して製品出荷に至る製
品数はごく一部。以下具体例(A社、他家細胞製品)
3
•
以下3つの観点より、再生医療等製品の品質検査コストは従来の医薬品よりも高い
総製造量に対して検査用製造
の占める割合が高い
製品
出荷
0.2-1万本
30-100本
既存医薬品
再生医療等
•
…
•
検査
• 1ロット平均70バック製造に対し出荷試験16本、参考品19本保管が必要な
ため、製品出荷は35本(50%)となる。(30-100本の製造を想定、30本し
か細胞が取れない場合は、出荷できずロットアウトとなる)
(参考):抗体医薬は0.2-1万本(1ml/本)に対し200-300本と数%程度)
製品にできない
参考品
既存医薬品
再生医療等
受入
製造
•
再生医療等製品は出荷時検査に加え、受入検査や細胞加工中に
工程内検査を実施する必要がある
• 受入:細胞受け入れ時のコンタミ有無、無菌検査等
• 製造:DCB(ドナーセルバンク)、WCB(ワーキングセルバンク)時点
で、拡大培養のたびに各種検査が課せられている
•
ウイルス否定試験に関しては、受託可能なプレーヤーの絶対数が
少なく、また海外への外注が必要な場合も多いことから、委託単
価が一般的な試験よりも高い
DCB
WCB
出荷
検工
査程
費全
用体
がで
高か
いか
る
最終製品のみでは
なく製造工程中の
検査が必要
検査単価が高い
(ウイルス否定試験)
出所:有識者インタビューよりアーサー・ディ・リトル作成
再生医療等製品は、既存の医薬品と比較して一回のロットで製造す
る量が少ない。そのため、ロットごとに必要な検査用製剤の占める割
合が総製造量に対して大きく、コストとして重い
製造のボラティリティも含めると、製造量に対して製品出荷に至る製
品数はごく一部。以下具体例(A社、他家細胞製品)
3