よむ、つかう、まなぶ。
参考資料1○患者申出療養の総括報告書に関する評価について (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00029.html |
| 出典情報 | 患者申出療養評価会議(第47回 12/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
薬事承認・保険収載までのロードマップ
日本における薬
事承認状況
効能・効果
・CD20陽性のB細胞性非ホ
ジキンリンパ腫
・CD20陽性の慢性リンパ性
白血病
・免疫抑制状態下のCD20陽
性のB細胞性リンパ増殖性
疾患
・多発血管炎性肉芽腫症、
顕微鏡的多発血管炎
・難治性のネフローゼ症候
群
・慢性特発性血小板減少性
紫斑病
・後天性血栓性血小板減少
性紫斑病
・腎移植、肝移植のABO血
液型不適合移植における
抗体関連型拒絶反応の抑
制
・インジウム イブリツモマブ
チウキセタン及びイットリウ
ムイブリツモマブ チウキ
セタン投与の前投与
承認年月
2001年6月初回承認
2020年2月(最終適応追加)
米国における薬
事承認状況
CIDPに対する適応 無
2021年2月末現在
「免疫グロブリンGサブクラス4(IgG4)自己抗体陽性の難治性慢
性炎症性脱髄性多発神経炎(CIDP)患者に対するリツキシマブ
(遺伝子組換え)の有効性及び安全性を検討する探索的臨床
試験(RECIPE試験)」(jRCT2041180037・NCT03864185)
国内医師主導治験
対象: EFNS/PNS診断基準のDefinite CIDP
(副腎皮質ステロイド治療(12週間)並びに経静脈的免疫グロブリン療法(8週間)で十分な改善が認められなかった難
治性の患者、もしくはいずれの治療も実施又は継続が困難な患者)
デザイン: プラセボ対象二重盲検無作為化比較試験
登録症例数: IgG4自己抗体(抗NF155抗体)陽性CIDP15例、陰性例10例の計25名
進捗状況: 2019年3月~2020年6月(登録終了)、観察期間 2021年6月まで(予定)
有用性が認められた場合
参考
データ
適
応
追
加
【患者申出療養】
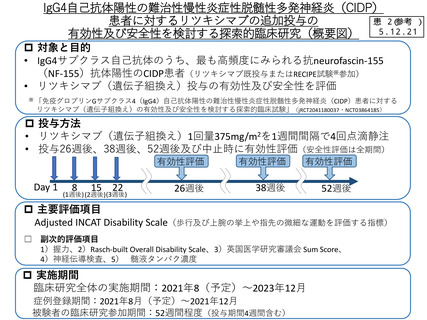
免疫グロブリンGサブクラス4(IgG4)自己抗体陽性の難治性慢性炎症性脱髄性多発神経炎(CIDP)患者
に対するリツキシマブ(遺伝子組換え)の追加投与の有効性及び安全性を検討する探索的臨床研究
対象: 抗NF155抗体陽性のCIDP患者(リツキシマブ既投与またはRECIPE試験参加)
目的:リツキシマブ(遺伝子組換え)投与の有効性及び安全性を評価
主要評価項目:Adjusted INCAT Disability Scale(歩行及び上腕の挙上や指先の微細な運動を評価する指標)
開発中止
医療としての有
用性が認めら
れなかった場合
実施期間: 2021年8月(予定)~2023年12月
実施医療機関:名古屋大学医学部附属病院
安全性上の問題等で、実施継続が
不適切と考えられた場合
2
患者申出療養の取り下げ
日本における薬
事承認状況
効能・効果
・CD20陽性のB細胞性非ホ
ジキンリンパ腫
・CD20陽性の慢性リンパ性
白血病
・免疫抑制状態下のCD20陽
性のB細胞性リンパ増殖性
疾患
・多発血管炎性肉芽腫症、
顕微鏡的多発血管炎
・難治性のネフローゼ症候
群
・慢性特発性血小板減少性
紫斑病
・後天性血栓性血小板減少
性紫斑病
・腎移植、肝移植のABO血
液型不適合移植における
抗体関連型拒絶反応の抑
制
・インジウム イブリツモマブ
チウキセタン及びイットリウ
ムイブリツモマブ チウキ
セタン投与の前投与
承認年月
2001年6月初回承認
2020年2月(最終適応追加)
米国における薬
事承認状況
CIDPに対する適応 無
2021年2月末現在
「免疫グロブリンGサブクラス4(IgG4)自己抗体陽性の難治性慢
性炎症性脱髄性多発神経炎(CIDP)患者に対するリツキシマブ
(遺伝子組換え)の有効性及び安全性を検討する探索的臨床
試験(RECIPE試験)」(jRCT2041180037・NCT03864185)
国内医師主導治験
対象: EFNS/PNS診断基準のDefinite CIDP
(副腎皮質ステロイド治療(12週間)並びに経静脈的免疫グロブリン療法(8週間)で十分な改善が認められなかった難
治性の患者、もしくはいずれの治療も実施又は継続が困難な患者)
デザイン: プラセボ対象二重盲検無作為化比較試験
登録症例数: IgG4自己抗体(抗NF155抗体)陽性CIDP15例、陰性例10例の計25名
進捗状況: 2019年3月~2020年6月(登録終了)、観察期間 2021年6月まで(予定)
有用性が認められた場合
参考
データ
適
応
追
加
【患者申出療養】
免疫グロブリンGサブクラス4(IgG4)自己抗体陽性の難治性慢性炎症性脱髄性多発神経炎(CIDP)患者
に対するリツキシマブ(遺伝子組換え)の追加投与の有効性及び安全性を検討する探索的臨床研究
対象: 抗NF155抗体陽性のCIDP患者(リツキシマブ既投与またはRECIPE試験参加)
目的:リツキシマブ(遺伝子組換え)投与の有効性及び安全性を評価
主要評価項目:Adjusted INCAT Disability Scale(歩行及び上腕の挙上や指先の微細な運動を評価する指標)
開発中止
医療としての有
用性が認めら
れなかった場合
実施期間: 2021年8月(予定)~2023年12月
実施医療機関:名古屋大学医学部附属病院
安全性上の問題等で、実施継続が
不適切と考えられた場合
2
患者申出療養の取り下げ