よむ、つかう、まなぶ。
資料2-9 HPVワクチン(ガーダシル)の副反応疑い報告状況について[346KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00106.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第102回 7/29)医薬品等安全対策部会安全対策調査会(令和6年度第4回 7/29)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第102回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和6年度第4回薬
事審議会医薬品等安全対策部会安全対策調査会
資料2-9
2024(令和6)年7月29日
HPVワクチン(ガーダシル)の
副反応疑い報告状況について
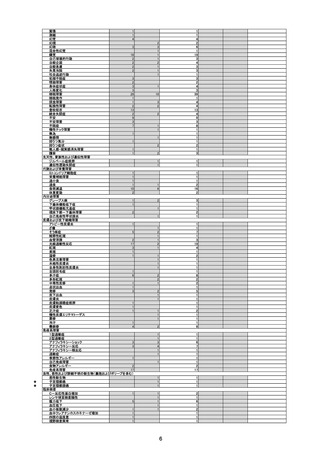
○組換え沈降4 価ヒトパピローマウイルス様粒子ワクチン(酵母由来)
商
品
名
製 造 販 売 業 者
販
売
開
始
効 能 ・ 効 果
: ガーダシル
: MSD株式会社
: 平成23年8月
: ヒトパピローマウイルス 6 、11、16及び18型の感染に起因する以下の疾患の予防
・子宮頸癌(扁平上皮癌及び腺癌)及びその前駆病変(子宮頸部上皮内腫瘍(CIN)1 、2 及び3 並びに
上皮内腺癌(AIS))
・外陰上皮内腫瘍(VIN)1、2 及び3 並びに腟上皮内腫瘍(VaIN)1、2 及び3
・肛門癌(扁平上皮癌)及びその全区病変(肛門上皮内腫瘍(AIN)1、2 及び3)
・尖圭コンジローマ
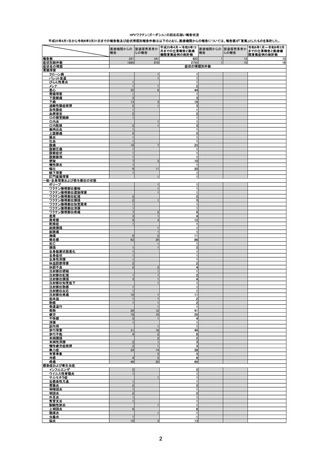
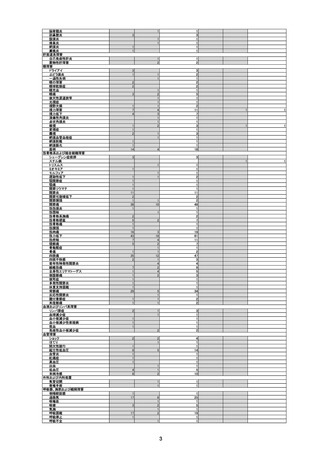
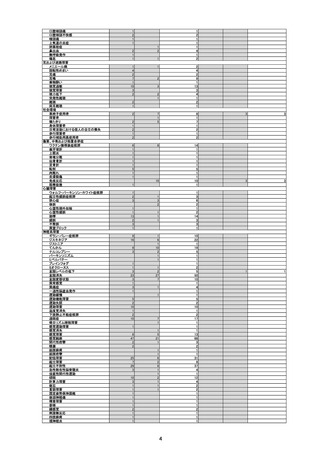
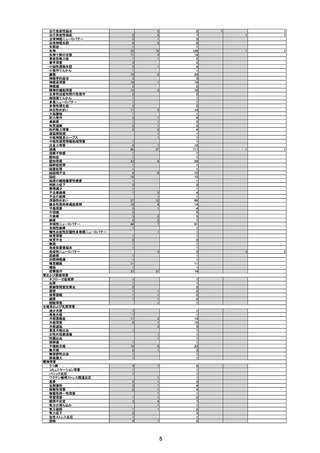
副反応疑い報告数
(令和6年1月1日から令和6年3月31日報告分まで:報告日での集計)
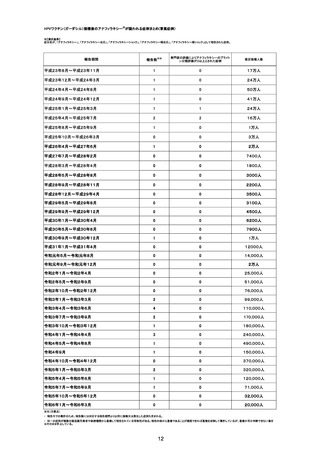
令和6年1月1日から令和6年3月31日までの医療機関への納入数量を接種可能のべ人数とし、副反応疑い報告頻度を計算したものは以下のとおり。な
お、製造販売業者によると、接種スケジュールを勘案し、これまでの1人あたりの平均接種回数を2.5回と仮定して出荷数量より推計した接種者数は、
180万人とのことである。
※報告日での集計のため、以下の件数には接種日や発生日が対象期間以前の症例も含まれている。
(単位:例)
接種可能のべ人数
(回数)
注1)
製造販売業者からの報告
医療機関からの報告
報告数
():接種日が左記期間内
の症例
報告数
():接種日が左記期間内の症例
令和6年1月1日
20,585
~令和6年3月31日
(参考)
販売開始からの累計
4,517,813
注2)
報告頻度
報告頻度
うち重篤
12
(0)
0.0583%
0.0000%
3
(1)
0.0146%
0.0049%
1
(0)
0.0049%
0.0000%
408
742
243
0.0090%
0.0164%
0.0054%
(注意点)
注1) 販売開始からの累計接種のべ人数は、返品された数を加味した場合
注2) 「(参考)販売開始からの累計」は、医療機関から症状の程度が「重い」として報告された事例の累計。「令和6年1月1日~令和6年3月31日」は、医療機関から症状の程
度が「重い」として報告された事例に加えて、医療機関からの報告では症状の程度が「重くない」とされた事例であっても、製造販売業者の調査の結果、重篤として報告され
た事例も集計。
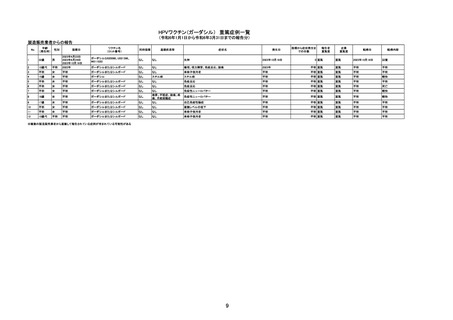
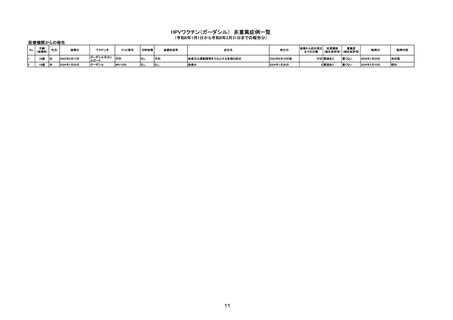
令和6年1月1日から令和6年3月31日報告分の重篤例の転帰
(単位:例)
製造販売業者からの報告
重篤例数
医療機関からの報告
回復/
軽快
未回復
後遺症
死亡
不明
計
回復/
軽快
未回復
後遺症
死亡
不明
計
4
0
0
1
7
12
0
0
0
0
1
1
(注意点)
※ 副反応疑い報告については、医薬品との因果関係が不明なものを含め、製造販売業者又は医療機関から報告されたものであり、個別に医薬品との関連性を評価したもので
はない。
※ 販売開始からの累計において、製造販売業者からの報告は、販売開始~令和6年3月31日までの報告分、医療機関からの報告は、平成23年9月20日 ~令和6年3月31日までの
報告分である。
※ 「重篤」とは、死亡、障害、それらに繋がるおそれのあるもの、入院相当以上のものが報告対象とされているが、必ずしも重篤でないものも「重篤」として報告される
ケースがある。
※
非重篤症例には、重篤度が不明の症例も含まれている。
※ 製造販売業者からの報告は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第68条の10に基づき「重篤」と判断された症例について報告されたもの
である。なお、製造販売業者からの報告には、医療機関から報告された症例と重複している症例が含まれている可能性があり、重複症例は、医療機関報告として計上してい
る。また、その後の調査等によって、報告対象でないことが確認され、報告が取り下げられた症例が含まれる可能性がある。
※
製造販売業者からの報告には、複数の製造販売業者から重複して報告されている症例が含まれている可能性がある。
1
事審議会医薬品等安全対策部会安全対策調査会
資料2-9
2024(令和6)年7月29日
HPVワクチン(ガーダシル)の
副反応疑い報告状況について
○組換え沈降4 価ヒトパピローマウイルス様粒子ワクチン(酵母由来)
商
品
名
製 造 販 売 業 者
販
売
開
始
効 能 ・ 効 果
: ガーダシル
: MSD株式会社
: 平成23年8月
: ヒトパピローマウイルス 6 、11、16及び18型の感染に起因する以下の疾患の予防
・子宮頸癌(扁平上皮癌及び腺癌)及びその前駆病変(子宮頸部上皮内腫瘍(CIN)1 、2 及び3 並びに
上皮内腺癌(AIS))
・外陰上皮内腫瘍(VIN)1、2 及び3 並びに腟上皮内腫瘍(VaIN)1、2 及び3
・肛門癌(扁平上皮癌)及びその全区病変(肛門上皮内腫瘍(AIN)1、2 及び3)
・尖圭コンジローマ
副反応疑い報告数
(令和6年1月1日から令和6年3月31日報告分まで:報告日での集計)
令和6年1月1日から令和6年3月31日までの医療機関への納入数量を接種可能のべ人数とし、副反応疑い報告頻度を計算したものは以下のとおり。な
お、製造販売業者によると、接種スケジュールを勘案し、これまでの1人あたりの平均接種回数を2.5回と仮定して出荷数量より推計した接種者数は、
180万人とのことである。
※報告日での集計のため、以下の件数には接種日や発生日が対象期間以前の症例も含まれている。
(単位:例)
接種可能のべ人数
(回数)
注1)
製造販売業者からの報告
医療機関からの報告
報告数
():接種日が左記期間内
の症例
報告数
():接種日が左記期間内の症例
令和6年1月1日
20,585
~令和6年3月31日
(参考)
販売開始からの累計
4,517,813
注2)
報告頻度
報告頻度
うち重篤
12
(0)
0.0583%
0.0000%
3
(1)
0.0146%
0.0049%
1
(0)
0.0049%
0.0000%
408
742
243
0.0090%
0.0164%
0.0054%
(注意点)
注1) 販売開始からの累計接種のべ人数は、返品された数を加味した場合
注2) 「(参考)販売開始からの累計」は、医療機関から症状の程度が「重い」として報告された事例の累計。「令和6年1月1日~令和6年3月31日」は、医療機関から症状の程
度が「重い」として報告された事例に加えて、医療機関からの報告では症状の程度が「重くない」とされた事例であっても、製造販売業者の調査の結果、重篤として報告され
た事例も集計。
令和6年1月1日から令和6年3月31日報告分の重篤例の転帰
(単位:例)
製造販売業者からの報告
重篤例数
医療機関からの報告
回復/
軽快
未回復
後遺症
死亡
不明
計
回復/
軽快
未回復
後遺症
死亡
不明
計
4
0
0
1
7
12
0
0
0
0
1
1
(注意点)
※ 副反応疑い報告については、医薬品との因果関係が不明なものを含め、製造販売業者又は医療機関から報告されたものであり、個別に医薬品との関連性を評価したもので
はない。
※ 販売開始からの累計において、製造販売業者からの報告は、販売開始~令和6年3月31日までの報告分、医療機関からの報告は、平成23年9月20日 ~令和6年3月31日までの
報告分である。
※ 「重篤」とは、死亡、障害、それらに繋がるおそれのあるもの、入院相当以上のものが報告対象とされているが、必ずしも重篤でないものも「重篤」として報告される
ケースがある。
※
非重篤症例には、重篤度が不明の症例も含まれている。
※ 製造販売業者からの報告は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第68条の10に基づき「重篤」と判断された症例について報告されたもの
である。なお、製造販売業者からの報告には、医療機関から報告された症例と重複している症例が含まれている可能性があり、重複症例は、医療機関報告として計上してい
る。また、その後の調査等によって、報告対象でないことが確認され、報告が取り下げられた症例が含まれる可能性がある。
※
製造販売業者からの報告には、複数の製造販売業者から重複して報告されている症例が含まれている可能性がある。
1