よむ、つかう、まなぶ。
「核酸等の第一種使用等に関する専門委員会(仮)の設立について」 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_55798.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第104回 3/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
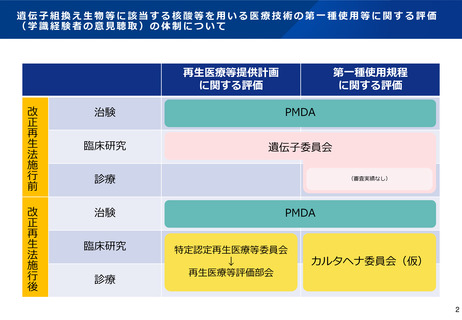
カルタヘナ委員会で評価を行う第一種使用規程について(案)
カルタヘナ委員会で評価を行う第一種使用規程について(案)
• 臨床研究(治験を除く。)及び診療の目的で、再生医療等安全性確保法の下で、カルタヘナ法上の遺伝子組換え生物等(LMO)に該当
する特定核酸等を用いる場合には、その第一種使用規程については、カルタヘナ委員会で学識経験者の意見聴取を行う。
• ただし、将来的に医薬品や再生医療等製品として、将来一般流通を目指す場合には、その前提での対応が必要となることから、原則と
して、医薬品医療機器総合機構(PMDA)相談(対面助言)を行う必要がある。
• このことから、申請者が、特定の医療機関において、特定の状況の下で実施される場合に限定した使用を想定する場合に限り、カルタ
ヘナ委員会において評価を行う。(第一種使用規程の承認は特定の状況の下での実施に限られたものとなる。)
• カルタヘナ委員会において評価を行うか、PMDA相談を求めるかは、PMDAとの連携のもと再生医療等評価部会事務局において判断。
• 診療で用いる場合については、特定核酸等を用いる医療技術は第一種再生医療等に該当することから、その提供の前提として、有効性
が確立しており科学的妥当性が認められた医療技術として厚生科学審議会再生医療等評価部会において確認されたものに限定する。
臨床研究
診
研究開発の目標として、医薬品・再生医療等製品として一般流通
を見据えた研究である。
Yes
療
有効性が確立しており科学的妥当性が認められた医療技術として、
厚生科学審議会再生医療等評価部会で確認されている。
No
カルタヘナ委員会
Yes
前提条件(チェックリスト※)を満たすことを確認
PMDA相談
(対面助言)
カルタヘナ委員会
•
•
•
•
•
特定の医療機関においてのみ実施する
医療機関において適切なLMOの封じ込めが可能な体制を有している
人に投与可能な適切な品質のLMOを使用している
LMOの入手経路が遡及可能である
宿主、供与核酸、全塩基配列の情報を有している 等
Yes
第一種使用規程及び生物多様性影響評価書に関する学識経験者意見聴取
No
※ カルタヘナ委員会において策定
No
評価不適
3
カルタヘナ委員会で評価を行う第一種使用規程について(案)
• 臨床研究(治験を除く。)及び診療の目的で、再生医療等安全性確保法の下で、カルタヘナ法上の遺伝子組換え生物等(LMO)に該当
する特定核酸等を用いる場合には、その第一種使用規程については、カルタヘナ委員会で学識経験者の意見聴取を行う。
• ただし、将来的に医薬品や再生医療等製品として、将来一般流通を目指す場合には、その前提での対応が必要となることから、原則と
して、医薬品医療機器総合機構(PMDA)相談(対面助言)を行う必要がある。
• このことから、申請者が、特定の医療機関において、特定の状況の下で実施される場合に限定した使用を想定する場合に限り、カルタ
ヘナ委員会において評価を行う。(第一種使用規程の承認は特定の状況の下での実施に限られたものとなる。)
• カルタヘナ委員会において評価を行うか、PMDA相談を求めるかは、PMDAとの連携のもと再生医療等評価部会事務局において判断。
• 診療で用いる場合については、特定核酸等を用いる医療技術は第一種再生医療等に該当することから、その提供の前提として、有効性
が確立しており科学的妥当性が認められた医療技術として厚生科学審議会再生医療等評価部会において確認されたものに限定する。
臨床研究
診
研究開発の目標として、医薬品・再生医療等製品として一般流通
を見据えた研究である。
Yes
療
有効性が確立しており科学的妥当性が認められた医療技術として、
厚生科学審議会再生医療等評価部会で確認されている。
No
カルタヘナ委員会
Yes
前提条件(チェックリスト※)を満たすことを確認
PMDA相談
(対面助言)
カルタヘナ委員会
•
•
•
•
•
特定の医療機関においてのみ実施する
医療機関において適切なLMOの封じ込めが可能な体制を有している
人に投与可能な適切な品質のLMOを使用している
LMOの入手経路が遡及可能である
宿主、供与核酸、全塩基配列の情報を有している 等
Yes
第一種使用規程及び生物多様性影響評価書に関する学識経験者意見聴取
No
※ カルタヘナ委員会において策定
No
評価不適
3