よむ、つかう、まなぶ。
資料3-4 申請技術の概要及びロードマップ (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_25542.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第133回 5/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
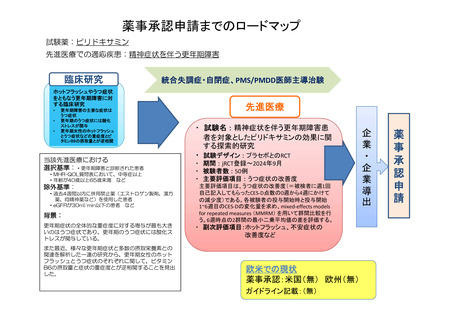
薬事承認申請までのロードマップ
試験薬:ピリドキサミン
先進医療での適応疾患:精神症状を伴う更年期障害
臨床研究
統合失調症・自閉症、PMS/PMDD医師主導治験
ホットフラッシュやうつ症状
をともなう更年期障害に対
する臨床研究
•
•
•
更年期障害の主要な症状は
うつ症状
更年期のうつ症状には酸化
ストレスが関与
更年期女性のホットフラッシュ
とうつ症状などの重症度とビ
タミンB6の摂取量とが逆相関
当該先進医療における
選択基準:・更年期障害と診断された患者
・MHR-QOL質問表において、中等症以上
・年齢が40歳以上65歳未満 など
除外基準:
・過去4週間以内に併用禁止薬(エストロゲン製剤、漢方
薬、向精神薬など)を使用した患者
・eGFRが30ml/min以下の患者 など
背景:
更年期症状の全体的な重症度に対する寄与が最も大き
いのはうつ症状であり、更年期のうつ症状には酸化ス
トレスが関与している。
また最近、様々な更年期症状と多数の摂取栄養素との
関連を解析した一連の研究から、更年期女性のホット
フラッシュとうつ症状のそれぞれに関して、ビタミン
B6の摂取量と症状の重症度とが逆相関することを見出
した。
先進医療
・ 試験名 : 精神症状を伴う更年期障害患
者を対象としたピリドキサミンの効果に関
する探索的研究
・ 試験デザイン : プラセボとのRCT
・ 期間 : jRCT登録~2024年9月
・ 被験者数 : 50例
・ 主要評価項目 : うつ症状の改善度
主要評価項目は、うつ症状の改善度(=被検者に週1回
自己記入してもらったCES-D点数の0週から4週にかけて
の減少度)である。各被験者の投与開始時と投与開始
1~6週目のCES-Dの変化量を求め、mixed-effects models
for repeated measures (MMRM) を用いて群間比較を行
う。6週時点の2群間の最小二乗平均値の差を評価する。
・ 副次評価項目:ホットフラッシュ、不安症状の
改善度など
欧米での現状
薬事承認:米国(無) 欧州(無)
ガイドライン記載:(無)
企
業
・
企
業
導
出
薬
事
承
認
申
請
試験薬:ピリドキサミン
先進医療での適応疾患:精神症状を伴う更年期障害
臨床研究
統合失調症・自閉症、PMS/PMDD医師主導治験
ホットフラッシュやうつ症状
をともなう更年期障害に対
する臨床研究
•
•
•
更年期障害の主要な症状は
うつ症状
更年期のうつ症状には酸化
ストレスが関与
更年期女性のホットフラッシュ
とうつ症状などの重症度とビ
タミンB6の摂取量とが逆相関
当該先進医療における
選択基準:・更年期障害と診断された患者
・MHR-QOL質問表において、中等症以上
・年齢が40歳以上65歳未満 など
除外基準:
・過去4週間以内に併用禁止薬(エストロゲン製剤、漢方
薬、向精神薬など)を使用した患者
・eGFRが30ml/min以下の患者 など
背景:
更年期症状の全体的な重症度に対する寄与が最も大き
いのはうつ症状であり、更年期のうつ症状には酸化ス
トレスが関与している。
また最近、様々な更年期症状と多数の摂取栄養素との
関連を解析した一連の研究から、更年期女性のホット
フラッシュとうつ症状のそれぞれに関して、ビタミン
B6の摂取量と症状の重症度とが逆相関することを見出
した。
先進医療
・ 試験名 : 精神症状を伴う更年期障害患
者を対象としたピリドキサミンの効果に関
する探索的研究
・ 試験デザイン : プラセボとのRCT
・ 期間 : jRCT登録~2024年9月
・ 被験者数 : 50例
・ 主要評価項目 : うつ症状の改善度
主要評価項目は、うつ症状の改善度(=被検者に週1回
自己記入してもらったCES-D点数の0週から4週にかけて
の減少度)である。各被験者の投与開始時と投与開始
1~6週目のCES-Dの変化量を求め、mixed-effects models
for repeated measures (MMRM) を用いて群間比較を行
う。6週時点の2群間の最小二乗平均値の差を評価する。
・ 副次評価項目:ホットフラッシュ、不安症状の
改善度など
欧米での現状
薬事承認:米国(無) 欧州(無)
ガイドライン記載:(無)
企
業
・
企
業
導
出
薬
事
承
認
申
請