よむ、つかう、まなぶ。
参考資料1 新型コロナワクチン「コミナティ筋注(1価:起源株)」(ファイザー株式会社)添付文書 (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00055.html |
| 出典情報 | 第 88 回厚生科学審議会予防接種・ワクチン分科会 副反応検討部会、令和4年度第 18 回薬事・食品衛生審 議会薬事分科会医薬品等安全対策部会安全対策調査会(11/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
9. 特定の背景を有する者に関する注意
9.1 接種要注意者(接種の判断を行うに際し、注意を要する者)
被接種者が次のいずれかに該当すると認められる場合は、健康状態
及び体質を勘案し、診察及び接種適否の判断を慎重に行い、予防接
種の必要性、副反応、有用性について十分な説明を行い、同意を確
実に得た上で、注意して接種すること。
[8.2参照]
9.1.1 抗凝固療法を受けている者、血小板減少症又は凝固障害を有す
る者
本剤接種後に出血又は挫傷があらわれることがある。
9.1.2 過去に免疫不全の診断がなされている者及び近親者に先天性免
疫不全症の者がいる者
本剤に対する免疫応答が低下する可能性がある。
9.1.3 心臓血管系疾患、腎臓疾患、肝臓疾患、血液疾患、発育障害等
の基礎疾患を有する者
9.1.4 予防接種で接種後2日以内に発熱のみられた者及び全身性発疹
等のアレルギーを疑う症状を呈したことがある者
9.1.5 過去に痙攣の既往のある者
9.1.6 本剤の成分に対して、アレルギーを呈するおそれのある者
[2.3、8.4、11.1.1参照]
9.2 腎機能障害を有する者
接種要注意者である。
9.3 肝機能障害を有する者
接種要注意者である。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には予防接種上の有益性が
危険性を上回ると判断される場合にのみ接種すること。
9.6 授乳婦
予防接種上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又
は中止を検討すること。ヒト母乳中への移行は不明である。
9.7 小児等
12歳未満を対象とした臨床試験は実施していない。
9.8 高齢者
接種にあたっては、問診等を慎重に行い、被接種者の健康状態を十
分に観察すること。一般に、生理機能が低下している。
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 保存方法
(1)冷凍保存
本剤は-90~-60℃から-25~-15℃に移し、-25~-15℃で最長14日間
保存することができる。なお1回に限り、再度-90~-60℃に戻し保存
することができる。いずれの場合も有効期間内に使用すること。
(2)冷蔵保存
本剤を冷蔵庫(2~8℃)で解凍する場合は、2~8℃で1ヵ月間保存す
ることができる。なお、解凍後は再冷凍せず、有効期間内に使用す
ること。
14.1.2 解凍方法
(1)室温で解凍する場合は、解凍及び希釈を2時間以内に行うこと。
(2)解凍の際は、室内照明による曝露を最小限に抑えること。直射日
光及び紫外線が当たらないようにすること。
(3)解凍後は再冷凍しないこと。
14.1.3 希釈方法
(1)希釈前に室温に戻しておくこと。
(2)本剤は保存料を含まないため、操作にあたっては雑菌が迷入しな
いよう注意すること。
(3)本剤のバイアルに日局生理食塩液1.8mLを加え、白色の均一な液に
なるまでゆっくりと転倒混和すること。振り混ぜないこと。
(4)希釈前の液は白色の微粒子を含むことがある。希釈後に微粒子が
認められる場合には、使用しないこと。
(5)希釈後の液は6回接種分(1回0.3mL)を有する。デッドボリューム
の少ない注射針又は注射筒を使用した場合、6回分を採取することが
できる。標準的な注射針及び注射筒等を使用した場合、6回目の接種
分を採取できないことがある。1回0.3mLを採取できない場合、残量
は廃棄すること。
(6)希釈後の液は2~30℃で保存し、希釈後6時間以内に使用すること。
希釈後6時間以内に使用しなかった液は廃棄すること。
(7)希釈後保存の際には、室内照明による曝露を最小限に抑えること。
直射日光及び紫外線が当たらないようにすること。
14.2 薬剤接種時の注意
14.2.1 室温に戻した希釈後のバイアルから接種量0.3mLを取り、微粒
子や変色がないことを目視で確認すること。異常が認められる場合
は使用しないこと。
14.2.2 通常、三角筋に筋肉内接種すること。静脈内、皮内、皮下への
接種は行わないこと。
14.2.3 組織・神経等への影響を避けるため下記の点に注意すること。
(1)針長は筋肉内接種に足る長さで、組織や血管あるいは骨に到達し
ないよう、各被接種者に対して適切な針長を決定すること。
(2)神経走行部位を避けること。
(3)注射針を刺入したとき、激痛の訴えや血液の逆流がみられた場合
は直ちに針を抜き、部位をかえて注射すること。
11. 副反応
次の副反応があらわれることがあるので、観察を十分に行い、異常
が認められた場合には適切な処置を行うこと。
11.1 重大な副反応
11.1.1 ショック、アナフィラキシー(頻度不明)
[2.3、8.4、9.1.6参照]
11.1.2 心筋炎、心膜炎(頻度不明)
[8.6、15.1.1、15.1.2参照]
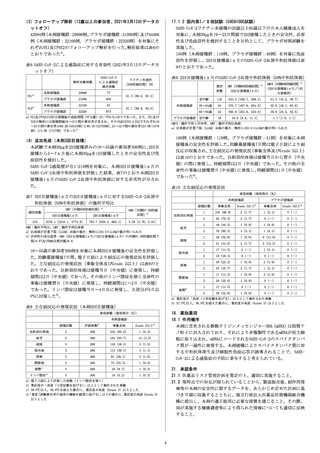
11.2 その他の副反応
5%以上
1%~5%未満
局 所 症 状 疼痛(85.6%)a)、腫脹
(注射部位) (10.3%)a)、発赤・紅
斑a)
a)
精神神経系
頭痛(59.4%)
消化器
下痢(14.8%)a)
嘔吐a)
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外において、コロナウイルス修飾ウリジンRNAワクチン
(SARS-CoV-2)接種後に心筋炎、心膜炎が報告されている。初回免疫
において報告された症例の多くは若年男性であり、特に2回目接種後
数日以内に発現している。また、大多数の症例で、入院による安静
臥床により症状が改善している1)。
[8.6、11.1.2参照]
15.1.2 接種開始後の国内副反応疑い報告における心筋炎、心膜炎の
報告率と、国内の医療情報データベースを用いて算出した一般集団
から推測される心筋炎、心膜炎の発現率とを比較したところ、初回
免疫として本剤2回接種後の若年男性で頻度が高いことが示唆され
た2)。[8.6、11.1.2参照]
15.1.3 海外において、皮膚充填剤との関連性は不明であるが、皮膚充
填剤注入歴のある被接種者において、コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV-2)接種後に、皮膚充填剤注入部位周辺の腫
脹(特に顔面腫脹)が報告されている。
悪心、食欲減退
口腔咽頭痛、鼻閉
筋肉痛(38.8%)a)、関
節痛(23.0%)a)
四肢痛、背部痛
皮膚
多汗症、発疹、寝汗
血液
リンパ節症
免疫系
その他
頻度不明
浮動性めまい、嗜眠、 錯感覚、感覚鈍麻
不眠症、顔面麻痺
呼吸器
筋・骨格系
1%未満
そう痒感、熱感、内出
血、浮腫
過敏症(発疹、そ
う痒症、紅斑、蕁
麻疹 、血 管 性 浮
腫、顔面腫脹等)
疲労(66.0%)a)、悪寒 疼痛
( 36.0% ) a )、 発 熱
(16.8%)a)
倦怠感、無力症、イン
フルエンザ様症状
a)臨床試験において電子日誌により収集した副反応の発現割合
注)海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート及び国内第Ⅰ/Ⅱ相試験
(C4591005試験)の2回接種に関するデータより集計
2
9.1 接種要注意者(接種の判断を行うに際し、注意を要する者)
被接種者が次のいずれかに該当すると認められる場合は、健康状態
及び体質を勘案し、診察及び接種適否の判断を慎重に行い、予防接
種の必要性、副反応、有用性について十分な説明を行い、同意を確
実に得た上で、注意して接種すること。
[8.2参照]
9.1.1 抗凝固療法を受けている者、血小板減少症又は凝固障害を有す
る者
本剤接種後に出血又は挫傷があらわれることがある。
9.1.2 過去に免疫不全の診断がなされている者及び近親者に先天性免
疫不全症の者がいる者
本剤に対する免疫応答が低下する可能性がある。
9.1.3 心臓血管系疾患、腎臓疾患、肝臓疾患、血液疾患、発育障害等
の基礎疾患を有する者
9.1.4 予防接種で接種後2日以内に発熱のみられた者及び全身性発疹
等のアレルギーを疑う症状を呈したことがある者
9.1.5 過去に痙攣の既往のある者
9.1.6 本剤の成分に対して、アレルギーを呈するおそれのある者
[2.3、8.4、11.1.1参照]
9.2 腎機能障害を有する者
接種要注意者である。
9.3 肝機能障害を有する者
接種要注意者である。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には予防接種上の有益性が
危険性を上回ると判断される場合にのみ接種すること。
9.6 授乳婦
予防接種上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又
は中止を検討すること。ヒト母乳中への移行は不明である。
9.7 小児等
12歳未満を対象とした臨床試験は実施していない。
9.8 高齢者
接種にあたっては、問診等を慎重に行い、被接種者の健康状態を十
分に観察すること。一般に、生理機能が低下している。
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 保存方法
(1)冷凍保存
本剤は-90~-60℃から-25~-15℃に移し、-25~-15℃で最長14日間
保存することができる。なお1回に限り、再度-90~-60℃に戻し保存
することができる。いずれの場合も有効期間内に使用すること。
(2)冷蔵保存
本剤を冷蔵庫(2~8℃)で解凍する場合は、2~8℃で1ヵ月間保存す
ることができる。なお、解凍後は再冷凍せず、有効期間内に使用す
ること。
14.1.2 解凍方法
(1)室温で解凍する場合は、解凍及び希釈を2時間以内に行うこと。
(2)解凍の際は、室内照明による曝露を最小限に抑えること。直射日
光及び紫外線が当たらないようにすること。
(3)解凍後は再冷凍しないこと。
14.1.3 希釈方法
(1)希釈前に室温に戻しておくこと。
(2)本剤は保存料を含まないため、操作にあたっては雑菌が迷入しな
いよう注意すること。
(3)本剤のバイアルに日局生理食塩液1.8mLを加え、白色の均一な液に
なるまでゆっくりと転倒混和すること。振り混ぜないこと。
(4)希釈前の液は白色の微粒子を含むことがある。希釈後に微粒子が
認められる場合には、使用しないこと。
(5)希釈後の液は6回接種分(1回0.3mL)を有する。デッドボリューム
の少ない注射針又は注射筒を使用した場合、6回分を採取することが
できる。標準的な注射針及び注射筒等を使用した場合、6回目の接種
分を採取できないことがある。1回0.3mLを採取できない場合、残量
は廃棄すること。
(6)希釈後の液は2~30℃で保存し、希釈後6時間以内に使用すること。
希釈後6時間以内に使用しなかった液は廃棄すること。
(7)希釈後保存の際には、室内照明による曝露を最小限に抑えること。
直射日光及び紫外線が当たらないようにすること。
14.2 薬剤接種時の注意
14.2.1 室温に戻した希釈後のバイアルから接種量0.3mLを取り、微粒
子や変色がないことを目視で確認すること。異常が認められる場合
は使用しないこと。
14.2.2 通常、三角筋に筋肉内接種すること。静脈内、皮内、皮下への
接種は行わないこと。
14.2.3 組織・神経等への影響を避けるため下記の点に注意すること。
(1)針長は筋肉内接種に足る長さで、組織や血管あるいは骨に到達し
ないよう、各被接種者に対して適切な針長を決定すること。
(2)神経走行部位を避けること。
(3)注射針を刺入したとき、激痛の訴えや血液の逆流がみられた場合
は直ちに針を抜き、部位をかえて注射すること。
11. 副反応
次の副反応があらわれることがあるので、観察を十分に行い、異常
が認められた場合には適切な処置を行うこと。
11.1 重大な副反応
11.1.1 ショック、アナフィラキシー(頻度不明)
[2.3、8.4、9.1.6参照]
11.1.2 心筋炎、心膜炎(頻度不明)
[8.6、15.1.1、15.1.2参照]
11.2 その他の副反応
5%以上
1%~5%未満
局 所 症 状 疼痛(85.6%)a)、腫脹
(注射部位) (10.3%)a)、発赤・紅
斑a)
a)
精神神経系
頭痛(59.4%)
消化器
下痢(14.8%)a)
嘔吐a)
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外において、コロナウイルス修飾ウリジンRNAワクチン
(SARS-CoV-2)接種後に心筋炎、心膜炎が報告されている。初回免疫
において報告された症例の多くは若年男性であり、特に2回目接種後
数日以内に発現している。また、大多数の症例で、入院による安静
臥床により症状が改善している1)。
[8.6、11.1.2参照]
15.1.2 接種開始後の国内副反応疑い報告における心筋炎、心膜炎の
報告率と、国内の医療情報データベースを用いて算出した一般集団
から推測される心筋炎、心膜炎の発現率とを比較したところ、初回
免疫として本剤2回接種後の若年男性で頻度が高いことが示唆され
た2)。[8.6、11.1.2参照]
15.1.3 海外において、皮膚充填剤との関連性は不明であるが、皮膚充
填剤注入歴のある被接種者において、コロナウイルス修飾ウリジン
RNAワクチン(SARS-CoV-2)接種後に、皮膚充填剤注入部位周辺の腫
脹(特に顔面腫脹)が報告されている。
悪心、食欲減退
口腔咽頭痛、鼻閉
筋肉痛(38.8%)a)、関
節痛(23.0%)a)
四肢痛、背部痛
皮膚
多汗症、発疹、寝汗
血液
リンパ節症
免疫系
その他
頻度不明
浮動性めまい、嗜眠、 錯感覚、感覚鈍麻
不眠症、顔面麻痺
呼吸器
筋・骨格系
1%未満
そう痒感、熱感、内出
血、浮腫
過敏症(発疹、そ
う痒症、紅斑、蕁
麻疹 、血 管 性 浮
腫、顔面腫脹等)
疲労(66.0%)a)、悪寒 疼痛
( 36.0% ) a )、 発 熱
(16.8%)a)
倦怠感、無力症、イン
フルエンザ様症状
a)臨床試験において電子日誌により収集した副反応の発現割合
注)海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート及び国内第Ⅰ/Ⅱ相試験
(C4591005試験)の2回接種に関するデータより集計
2