よむ、つかう、まなぶ。
資料2 先進医療Bの継続の可否に係る審議結果の報告について(告示番号50/ jRCTs032200423)【報告事項】 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29488.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第143回 12/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
員会の評価を経て、先進医療技術審査部会へ報告するとともに、多施設共同臨床
試験としての継続を併せて申請し、承認が得られた後に症例登録を再開するこ
と、とされている。
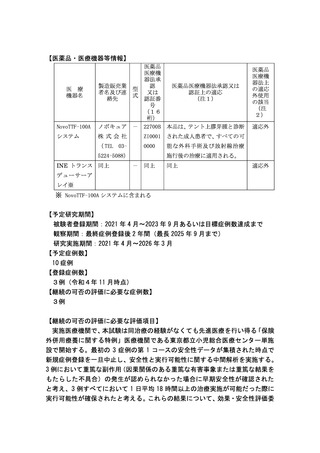
【継続の可否に係る独立した委員会の審議結果】
研究代表医師によると、重篤な副作用(因果関係のある重篤な有害事象または
重篤な結果をもたらした不具合)の発生は認められず、早期安全性が確認され、
実施可能性については、1例第1コースのみ、使用時間率が 53%と、1 日平均 18
時間(75%)の基準には未達であったが、アレイ配置の修正により第 2 コースは
基準を達成し、その他2症例は基準を達成したため、実行可能性は確保されてい
る、との報告をうけて、効果安全性評価委員会が開催された、当該研究の中間段
階(最初の3例)での安全性の評価の審議の結果、研究の継続が勧告された。
その結果を受けて、先進医療技術審査部会構成員(主担当および生物統計家)
によってご審議(メール稟議)いただいた結果、先進医療継続可との評価を得た
ため、新規症例登録が再開された(※)。
(※)第 59 回先進医療技術審査部会にて、評価に必要な数症例の試験結果および、その結
果について独立データモニタリング委員会等で審議された結果を、評価担当構成員(申請時
の主担当、副担当(生物統計担当))の先生方にご確認いただき、先進医療継続の可否につ
いてご評価(メール稟議)いただくこと、継続可となれば速やかに試験を再開してよいこと
とし、後日先進医療技術審査部会に報告することが了承されている。なお、諸事情により申
請時の構成員にお引き受けいただくことが難しい場合、適宜別の構成員にご確認いただく
こととする。
以上
試験としての継続を併せて申請し、承認が得られた後に症例登録を再開するこ
と、とされている。
【継続の可否に係る独立した委員会の審議結果】
研究代表医師によると、重篤な副作用(因果関係のある重篤な有害事象または
重篤な結果をもたらした不具合)の発生は認められず、早期安全性が確認され、
実施可能性については、1例第1コースのみ、使用時間率が 53%と、1 日平均 18
時間(75%)の基準には未達であったが、アレイ配置の修正により第 2 コースは
基準を達成し、その他2症例は基準を達成したため、実行可能性は確保されてい
る、との報告をうけて、効果安全性評価委員会が開催された、当該研究の中間段
階(最初の3例)での安全性の評価の審議の結果、研究の継続が勧告された。
その結果を受けて、先進医療技術審査部会構成員(主担当および生物統計家)
によってご審議(メール稟議)いただいた結果、先進医療継続可との評価を得た
ため、新規症例登録が再開された(※)。
(※)第 59 回先進医療技術審査部会にて、評価に必要な数症例の試験結果および、その結
果について独立データモニタリング委員会等で審議された結果を、評価担当構成員(申請時
の主担当、副担当(生物統計担当))の先生方にご確認いただき、先進医療継続の可否につ
いてご評価(メール稟議)いただくこと、継続可となれば速やかに試験を再開してよいこと
とし、後日先進医療技術審査部会に報告することが了承されている。なお、諸事情により申
請時の構成員にお引き受けいただくことが難しい場合、適宜別の構成員にご確認いただく
こととする。
以上