よむ、つかう、まなぶ。
参考資料5 新型コロナワクチン「コミナティ筋注5~11歳用(1価:起源株)」(ファイザー株式会社)添付文書 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591007試験)第Ⅱ/Ⅲ相パート
SARS-CoV-2ワクチン未接種の5~11歳の小児参加者を対象に、本剤
10µgを19~23日間隔で2回接種したときの免疫原性及び安全性を検
討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。さらに、本試験で本剤10µgを2回接種済みの5~11歳の小
児参加者に本剤10µgを1回接種したときの免疫原性及び安全性も検
討した。
(1)初回免疫(本剤2回接種)
本試験における5~11歳群
(本剤10µg)のSARS-CoV-2感染歴がない264
例及び海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)における16~25歳
群(本剤30µg)(17.1.2項参照)のSARS-CoV-2感染歴がない253例を
対象に、本剤2回目接種後1ヵ月のSARS-CoV-2血清中和抗体価及び抗
体応答率を評価した結果、
表1及び表2のとおり本試験における5~11
歳群(本剤10µg)の海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)にお
ける16~25歳群(本剤30µg)に対する免疫ブリッジングの成功基準
を満たした3)。
発現例数(発現割合[%])
本剤接種群
接種 評価
回数 例数a)
発熱c)
1.04
[0.93, 1.18]
GMR:幾何平均比、GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)免疫ブリッジングの成功基準:GMR(5~11歳/16~25歳)の両側95%信頼区間下限>0.67及
びGMR点推定値≥0.8
16~25歳群(本剤30µg)
262(99.2)
[97.3, 99.9]
251(99.2)
[97.2, 99.9]
253
0.0[-2.0, 2.2]
a)抗体価がベースライン値(ベースライン値が定量下限(LLOQ)未満の場合はLLOQ値)から
4倍以上上昇した治験参加者数
b)免疫ブリッジングの成功基準:抗体応答率の差(5~11歳 - 16~25歳)の両側95%信頼区
間の下限が>-10.0%
疲労
頭痛
筋肉痛
悪寒
関節痛
10(1.3)
1(0.1)
741
9(1.2)
1(0.1)
合計
測定例数
GMT[両側95%信頼区間]a)
1回目接種前b)
146
20.5[20.5, 20.5]
2回目接種後1ヵ月b)
96
1253.9[1116.0, 1408.9]
3回目接種前
67
271.0[229.1, 320.6]
3回目接種後1ヵ月
67
2720.9[2280.1, 3247.0]
本剤接種群
接種回数
評価例数a)
事象全体
Grade 3以上b)
注射部位疼痛
3
371
274(73.9)
2(0.5)
疲労
3
371
169(45.6)
7(1.9)
頭痛
3
371
126(34.0)
3(0.8)
筋肉痛
3
371
68(18.3)
0(-)
悪寒
3
371
39(10.5)
1(0.3)
関節痛
3
371
25(6.7)
0(-)
発熱c)
3
371
25(6.7)
3(0.8)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
発現例数(発現割合[%])
注射部位疼痛
749
9(0.6)
発現例数(発現割合[%])
表3 主な副反応の発現状況
本剤接種群
3(0.2)
98(6.5)
表5 主な副反応の発現状況
2268例(本剤接種群:1518例、プラセボ接種群:750例)を対象に本
剤接種後の安全性を評価した。治験薬接種後7日間、電子日誌により
副反応の発現状況を評価し、主な副反応の発現状況(事象全体及び
Grade 3以上)は表3のとおりであった3)。注射部位疼痛は接種当日
(中央値)に発現し、持続期間は2日(中央値)であった。その他の
全身性の事象は接種翌日(中央値)に発現し、持続期間は1日(中央
値)であった4)。
接種 評価
回数 例数a)
38(2.5)
1501
401例を対象に本剤3回目接種後の安全性を評価した。治験薬接種後
7日間、電子日誌により副反応の発現状況を評価し、主な副反応の発
現状況(事象全体及びGrade 3以上)は表5のとおりであった。注射
部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)
であった。その他の全身性の事象は接種翌日(中央値)に発現し、
持続期間は1日(中央値)であった5)。
差(%)
na)(抗体応答率[%])
na)(抗体応答率[%])
b)
測定例数 [両側95%信頼区間] 測定例数 [両側95%信頼区間] [両側95%信頼区間]
(2回目接種後1ヵ月)
(2回目接種後1ヵ月)
264
1511
2
GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)1回目接種前時点及び2回目接種後1ヵ月時点のデータには2回接種集団[初回免疫(2回接
種)の免疫ブリッジング解析に用いた評価可能免疫原性集団から無作為に選定された参加者]
のデータも含む
表2 5~11歳群の16~25歳群に対するSARS-CoV-2血清中和抗体応答率
の差
5~11歳群(本剤10µg)
1
測定時点
1146.5
[1045.5, 1257.2]
253
Grade 3
以上b)
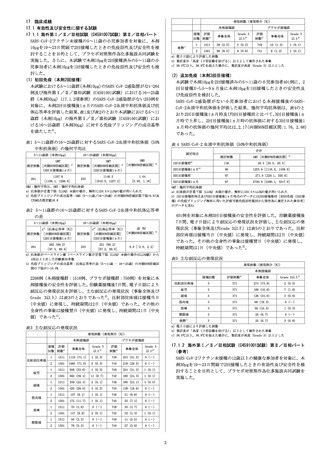
表 4 SARS-CoV-2 血清中和抗体価(50%中和抗体価)
16~25歳群(本剤30µg)
1197.6
[1106.1, 1296.6]
事象全体
(2)追加免疫(本剤3回目接種)
本試験で本剤10µgを2回接種済みの5~11歳の小児参加者401例に、2
回目接種から5~9ヵ月後に本剤10µgを1回接種したときの安全性及
び免疫原性を検討した。
SARS-CoV-2感染歴がない小児参加者における本剤接種後のSARSCoV-2血清中和抗体価を評価した結果、幾何平均抗体価は、表4のと
おり2回目接種後1ヵ月時及び3回目接種前と比べて、3回目接種後1ヵ
月時で上昇し、2回目接種後1ヵ月時の抗体価に対する3回目接種後1
ヵ月時の抗体価の幾何平均比は、2.17(両側95%信頼区間:1.76, 2.68)
であった。
GMR
GMT
GMT
b)
測定例数 [両側95%信頼区間]a) 測定例数 [両側95%信頼区間]a) [両側95%信頼区間]
(2回目接種後1ヵ月)
(2回目接種後1ヵ月)
264
事象全体
評価
例数a)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
表1 5~11歳群の16~25歳群に対するSARS-CoV-2血清中和抗体価(50%
中和抗体価)の幾何平均比
5~11歳群(本剤10µg)
プラセボ接種群
Grade 3
以上b)
プラセボ接種群
事象全体
Grade 3
以上b)
評価
例数a)
事象全体
Grade 3
以上b)
0(-)
1
1511
1119(74.1)
4(0.3)
748
234(31.3)
2
1501
1065(71.0)
5(0.3)
740
218(29.5)
0(-)
1
1511
508(33.6)
4(0.3)
748
234(31.3)
1(0.1)
2
1501
592(39.4)
11(0.7)
740
180(24.3)
1(0.1)
1
1511
339(22.4)
2(0.1)
748
180(24.1)
4(0.5)
2
1501
420(28.0)
3(0.2)
740
138(18.6)
0(-)
1
1511
137(9.1)
1(0.1)
748
51(6.8)
0(-)
2
1501
175(11.7)
1(0.1)
740
55(7.4)
0(-)
1
1511
70(4.6)
0(-)
748
35(4.7)
0(-)
2
1501
147(9.8)
2(0.1)
740
32(4.3)
1(0.1)
1
1511
50(3.3)
0(-)
748
41(5.5)
0(-)
2
1501
78(5.2)
0(-)
740
27(3.6)
0(-)
17.1.2 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート
(参考)
SARS-CoV-2ワクチン未接種の12歳以上の健康な参加者を対象に、本
剤30µgを19~23日間隔で2回接種したときの有効性及び安全性を検
討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。
3
17.1 有効性及び安全性に関する試験
17.1.1 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591007試験)第Ⅱ/Ⅲ相パート
SARS-CoV-2ワクチン未接種の5~11歳の小児参加者を対象に、本剤
10µgを19~23日間隔で2回接種したときの免疫原性及び安全性を検
討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。さらに、本試験で本剤10µgを2回接種済みの5~11歳の小
児参加者に本剤10µgを1回接種したときの免疫原性及び安全性も検
討した。
(1)初回免疫(本剤2回接種)
本試験における5~11歳群
(本剤10µg)のSARS-CoV-2感染歴がない264
例及び海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)における16~25歳
群(本剤30µg)(17.1.2項参照)のSARS-CoV-2感染歴がない253例を
対象に、本剤2回目接種後1ヵ月のSARS-CoV-2血清中和抗体価及び抗
体応答率を評価した結果、
表1及び表2のとおり本試験における5~11
歳群(本剤10µg)の海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)にお
ける16~25歳群(本剤30µg)に対する免疫ブリッジングの成功基準
を満たした3)。
発現例数(発現割合[%])
本剤接種群
接種 評価
回数 例数a)
発熱c)
1.04
[0.93, 1.18]
GMR:幾何平均比、GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)免疫ブリッジングの成功基準:GMR(5~11歳/16~25歳)の両側95%信頼区間下限>0.67及
びGMR点推定値≥0.8
16~25歳群(本剤30µg)
262(99.2)
[97.3, 99.9]
251(99.2)
[97.2, 99.9]
253
0.0[-2.0, 2.2]
a)抗体価がベースライン値(ベースライン値が定量下限(LLOQ)未満の場合はLLOQ値)から
4倍以上上昇した治験参加者数
b)免疫ブリッジングの成功基準:抗体応答率の差(5~11歳 - 16~25歳)の両側95%信頼区
間の下限が>-10.0%
疲労
頭痛
筋肉痛
悪寒
関節痛
10(1.3)
1(0.1)
741
9(1.2)
1(0.1)
合計
測定例数
GMT[両側95%信頼区間]a)
1回目接種前b)
146
20.5[20.5, 20.5]
2回目接種後1ヵ月b)
96
1253.9[1116.0, 1408.9]
3回目接種前
67
271.0[229.1, 320.6]
3回目接種後1ヵ月
67
2720.9[2280.1, 3247.0]
本剤接種群
接種回数
評価例数a)
事象全体
Grade 3以上b)
注射部位疼痛
3
371
274(73.9)
2(0.5)
疲労
3
371
169(45.6)
7(1.9)
頭痛
3
371
126(34.0)
3(0.8)
筋肉痛
3
371
68(18.3)
0(-)
悪寒
3
371
39(10.5)
1(0.3)
関節痛
3
371
25(6.7)
0(-)
発熱c)
3
371
25(6.7)
3(0.8)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
発現例数(発現割合[%])
注射部位疼痛
749
9(0.6)
発現例数(発現割合[%])
表3 主な副反応の発現状況
本剤接種群
3(0.2)
98(6.5)
表5 主な副反応の発現状況
2268例(本剤接種群:1518例、プラセボ接種群:750例)を対象に本
剤接種後の安全性を評価した。治験薬接種後7日間、電子日誌により
副反応の発現状況を評価し、主な副反応の発現状況(事象全体及び
Grade 3以上)は表3のとおりであった3)。注射部位疼痛は接種当日
(中央値)に発現し、持続期間は2日(中央値)であった。その他の
全身性の事象は接種翌日(中央値)に発現し、持続期間は1日(中央
値)であった4)。
接種 評価
回数 例数a)
38(2.5)
1501
401例を対象に本剤3回目接種後の安全性を評価した。治験薬接種後
7日間、電子日誌により副反応の発現状況を評価し、主な副反応の発
現状況(事象全体及びGrade 3以上)は表5のとおりであった。注射
部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)
であった。その他の全身性の事象は接種翌日(中央値)に発現し、
持続期間は1日(中央値)であった5)。
差(%)
na)(抗体応答率[%])
na)(抗体応答率[%])
b)
測定例数 [両側95%信頼区間] 測定例数 [両側95%信頼区間] [両側95%信頼区間]
(2回目接種後1ヵ月)
(2回目接種後1ヵ月)
264
1511
2
GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)1回目接種前時点及び2回目接種後1ヵ月時点のデータには2回接種集団[初回免疫(2回接
種)の免疫ブリッジング解析に用いた評価可能免疫原性集団から無作為に選定された参加者]
のデータも含む
表2 5~11歳群の16~25歳群に対するSARS-CoV-2血清中和抗体応答率
の差
5~11歳群(本剤10µg)
1
測定時点
1146.5
[1045.5, 1257.2]
253
Grade 3
以上b)
表 4 SARS-CoV-2 血清中和抗体価(50%中和抗体価)
16~25歳群(本剤30µg)
1197.6
[1106.1, 1296.6]
事象全体
(2)追加免疫(本剤3回目接種)
本試験で本剤10µgを2回接種済みの5~11歳の小児参加者401例に、2
回目接種から5~9ヵ月後に本剤10µgを1回接種したときの安全性及
び免疫原性を検討した。
SARS-CoV-2感染歴がない小児参加者における本剤接種後のSARSCoV-2血清中和抗体価を評価した結果、幾何平均抗体価は、表4のと
おり2回目接種後1ヵ月時及び3回目接種前と比べて、3回目接種後1ヵ
月時で上昇し、2回目接種後1ヵ月時の抗体価に対する3回目接種後1
ヵ月時の抗体価の幾何平均比は、2.17(両側95%信頼区間:1.76, 2.68)
であった。
GMR
GMT
GMT
b)
測定例数 [両側95%信頼区間]a) 測定例数 [両側95%信頼区間]a) [両側95%信頼区間]
(2回目接種後1ヵ月)
(2回目接種後1ヵ月)
264
事象全体
評価
例数a)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
表1 5~11歳群の16~25歳群に対するSARS-CoV-2血清中和抗体価(50%
中和抗体価)の幾何平均比
5~11歳群(本剤10µg)
プラセボ接種群
Grade 3
以上b)
プラセボ接種群
事象全体
Grade 3
以上b)
評価
例数a)
事象全体
Grade 3
以上b)
0(-)
1
1511
1119(74.1)
4(0.3)
748
234(31.3)
2
1501
1065(71.0)
5(0.3)
740
218(29.5)
0(-)
1
1511
508(33.6)
4(0.3)
748
234(31.3)
1(0.1)
2
1501
592(39.4)
11(0.7)
740
180(24.3)
1(0.1)
1
1511
339(22.4)
2(0.1)
748
180(24.1)
4(0.5)
2
1501
420(28.0)
3(0.2)
740
138(18.6)
0(-)
1
1511
137(9.1)
1(0.1)
748
51(6.8)
0(-)
2
1501
175(11.7)
1(0.1)
740
55(7.4)
0(-)
1
1511
70(4.6)
0(-)
748
35(4.7)
0(-)
2
1501
147(9.8)
2(0.1)
740
32(4.3)
1(0.1)
1
1511
50(3.3)
0(-)
748
41(5.5)
0(-)
2
1501
78(5.2)
0(-)
740
27(3.6)
0(-)
17.1.2 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート
(参考)
SARS-CoV-2ワクチン未接種の12歳以上の健康な参加者を対象に、本
剤30µgを19~23日間隔で2回接種したときの有効性及び安全性を検
討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。
3