よむ、つかう、まなぶ。
資料4-2 企業から提出された開発工程表における進捗について (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00031.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第57回 ) |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
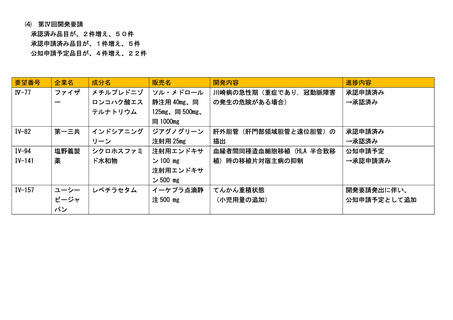
⑷ 第Ⅳ回開発要請
承認済み品目が、2件増え、50件
承認申請済み品目が、1件増え、5件
公知申請予定品目が、4件増え、22件
要望番号
企業名
成分名
販売名
開発内容
進捗内容
Ⅳ-77
ファイザ
ー
メチルプレドニゾ
ロンコハク酸エス
テルナトリウム
ソル・メドロール
静注用 40mg、同
125mg、同 500mg、
同 1000mg
川崎病の急性期(重症であり,冠動脈障害
の発生の危険がある場合)
承認申請済み
→承認済み
IV-82
第一三共
インドシアニング
リーン
ジアグノグリーン
注射用 25mg
肝外胆管(肝門部領域胆管と遠位胆管)の
描出
承認申請済み
→承認済み
IV-94
IV-141
塩野義製
薬
シクロホスファミ
ド水和物
注射用エンドキサ
ン 100 mg
注射用エンドキサ
ン 500 mg
血縁者間同種造血細胞移植 (HLA 半合致移
植) 時の移植片対宿主病の抑制
公知申請予定
→承認申請済み
IV-157
ユーシー
ビージャ
パン
レベチラセタム
イーケプラ点滴静
注 500 mg
てんかん重積状態
(小児用量の追加)
開発要請発出に伴い、
公知申請予定として追加
承認済み品目が、2件増え、50件
承認申請済み品目が、1件増え、5件
公知申請予定品目が、4件増え、22件
要望番号
企業名
成分名
販売名
開発内容
進捗内容
Ⅳ-77
ファイザ
ー
メチルプレドニゾ
ロンコハク酸エス
テルナトリウム
ソル・メドロール
静注用 40mg、同
125mg、同 500mg、
同 1000mg
川崎病の急性期(重症であり,冠動脈障害
の発生の危険がある場合)
承認申請済み
→承認済み
IV-82
第一三共
インドシアニング
リーン
ジアグノグリーン
注射用 25mg
肝外胆管(肝門部領域胆管と遠位胆管)の
描出
承認申請済み
→承認済み
IV-94
IV-141
塩野義製
薬
シクロホスファミ
ド水和物
注射用エンドキサ
ン 100 mg
注射用エンドキサ
ン 500 mg
血縁者間同種造血細胞移植 (HLA 半合致移
植) 時の移植片対宿主病の抑制
公知申請予定
→承認申請済み
IV-157
ユーシー
ビージャ
パン
レベチラセタム
イーケプラ点滴静
注 500 mg
てんかん重積状態
(小児用量の追加)
開発要請発出に伴い、
公知申請予定として追加