よむ、つかう、まなぶ。
資料6 先進医療Bの試験実施計画の変更について(告示番号54/ jRCTs051210055) (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36522.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第156回 12/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
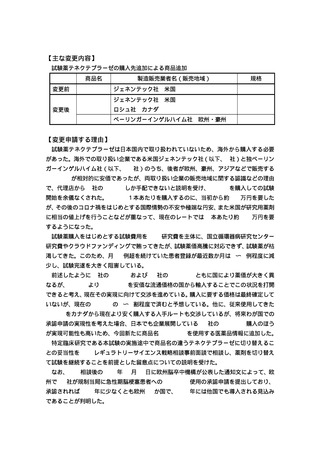
【主な変更内容】
試験薬テネクテプラーゼの購入先追加による商品追加
商品名
変更前
変更後
TNKase®
TNKase®
Metalyse®
製造販売業者名(販売地域)
ジェネンテック社 (米国)
ジェネンテック社 (米国)
ロシュ社 (カナダ)
ベーリンガーインゲルハイム社 (欧州・豪州)
規格
50mg
50mg
40mg, 50mg
【変更申請する理由】
試験薬テネクテプラーゼは日本国内で取り扱われていないため、海外から購入する必要
があった。海外での取り扱い企業である米国ジェネンテック社(以下、G 社)と独ベーリン
ガーインゲルハイム社(以下、BI 社)のうち、後者が欧州、豪州、アジアなどで販売する
Metalyse®が相対的に安価であったが、両取り扱い企業の販売地域に関する認識などの理由
で、代理店から G 社の TNKase®しか手配できないと説明を受け、TNKase®を購入しての試験
開始を余儀なくされた。TNKase®1本あたりを購入するのに、当初から約 100 万円を要した
が、その後のコロナ禍をはじめとする国際情勢の不安や極端な円安、また米国が研究用薬剤
に相当の値上げを行うことなどが重なって、現在のレートでは 1 本あたり約 200 万円を要
するようになった。
試験薬購入をはじめとする試験費用を AMED 研究費を主体に、国立循環器病研究センター
研究費やクラウドファンディングで賄ってきたが、試験薬価高騰に対応できず、試験薬が枯
渇してきた。このため、月 10 例超を続けていた患者登録が最近数か月は 1〜2 例程度に減
少し、試験完遂を大きく阻害している。
前述したように G 社の TNKase®および BI 社の Metalyse®ともに国により薬価が大きく異
なるが、TNKase®より Metalyse®を安価な流通価格の国から輸入することでこの状況を打開
できると考え、現在その実現に向けて交渉を進めている。購入に要する価格は最終確定して
いないが、現在の TNKase®の 2〜3 割程度で済むと予想している。他に、従来使用してきた
TNKase®をカナダから現在より安く購入する入手ルートも交渉しているが、将来わが国での
承認申請の実現性を考えた場合、日本でも企業展開している BI 社の Metalyse®購入のほう
が実現可能性も高いため、今回新たに商品名 Metalyse®を使用する医薬品情報に追加した。
特定臨床研究である本試験の実施途中で商品名の違うテネクテプラーゼに切り替えるこ
との妥当性を PMDA レギュラトリーサイエンス戦略相談事前面談で相談し、薬剤を切り替え
て試験を継続することを前提とした留意点についての説明を受けた。
なお、PMDA 相談後の 2023 年 11 月 29 日に欧州脳卒中機構が公表した通知文によって、欧
州で BI 社が規制当局に急性期脳梗塞患者への Metalyse®使用の承認申請を提出しており、
承認されれば 2024 年に少なくとも欧州 11 か国で、2025 年には他国でも導入される見込み
であることが判明した。
試験薬テネクテプラーゼの購入先追加による商品追加
商品名
変更前
変更後
TNKase®
TNKase®
Metalyse®
製造販売業者名(販売地域)
ジェネンテック社 (米国)
ジェネンテック社 (米国)
ロシュ社 (カナダ)
ベーリンガーインゲルハイム社 (欧州・豪州)
規格
50mg
50mg
40mg, 50mg
【変更申請する理由】
試験薬テネクテプラーゼは日本国内で取り扱われていないため、海外から購入する必要
があった。海外での取り扱い企業である米国ジェネンテック社(以下、G 社)と独ベーリン
ガーインゲルハイム社(以下、BI 社)のうち、後者が欧州、豪州、アジアなどで販売する
Metalyse®が相対的に安価であったが、両取り扱い企業の販売地域に関する認識などの理由
で、代理店から G 社の TNKase®しか手配できないと説明を受け、TNKase®を購入しての試験
開始を余儀なくされた。TNKase®1本あたりを購入するのに、当初から約 100 万円を要した
が、その後のコロナ禍をはじめとする国際情勢の不安や極端な円安、また米国が研究用薬剤
に相当の値上げを行うことなどが重なって、現在のレートでは 1 本あたり約 200 万円を要
するようになった。
試験薬購入をはじめとする試験費用を AMED 研究費を主体に、国立循環器病研究センター
研究費やクラウドファンディングで賄ってきたが、試験薬価高騰に対応できず、試験薬が枯
渇してきた。このため、月 10 例超を続けていた患者登録が最近数か月は 1〜2 例程度に減
少し、試験完遂を大きく阻害している。
前述したように G 社の TNKase®および BI 社の Metalyse®ともに国により薬価が大きく異
なるが、TNKase®より Metalyse®を安価な流通価格の国から輸入することでこの状況を打開
できると考え、現在その実現に向けて交渉を進めている。購入に要する価格は最終確定して
いないが、現在の TNKase®の 2〜3 割程度で済むと予想している。他に、従来使用してきた
TNKase®をカナダから現在より安く購入する入手ルートも交渉しているが、将来わが国での
承認申請の実現性を考えた場合、日本でも企業展開している BI 社の Metalyse®購入のほう
が実現可能性も高いため、今回新たに商品名 Metalyse®を使用する医薬品情報に追加した。
特定臨床研究である本試験の実施途中で商品名の違うテネクテプラーゼに切り替えるこ
との妥当性を PMDA レギュラトリーサイエンス戦略相談事前面談で相談し、薬剤を切り替え
て試験を継続することを前提とした留意点についての説明を受けた。
なお、PMDA 相談後の 2023 年 11 月 29 日に欧州脳卒中機構が公表した通知文によって、欧
州で BI 社が規制当局に急性期脳梗塞患者への Metalyse®使用の承認申請を提出しており、
承認されれば 2024 年に少なくとも欧州 11 か国で、2025 年には他国でも導入される見込み
であることが判明した。