よむ、つかう、まなぶ。
創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会 報告書 (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_39934.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会 報告書の公表について(4/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
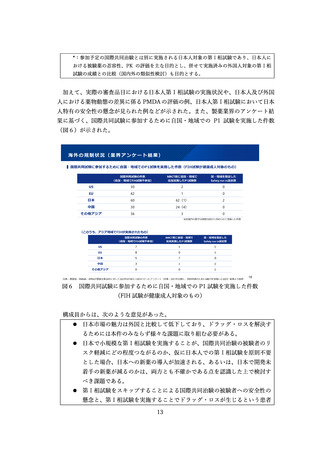
国際共同治験の参加前に日本人第Ⅰ相試験を実施すると、国際共同治験への日本
の参加の遅れ、日本の不参加、さらには日本での開発断念に繋がる場合がある状
況を踏まえ、日本人第Ⅰ相試験の実施に関して、製薬業界からは次のような意見
を受けている。
⚫ 国際共同治験に参加する前に、日本人第Ⅰ相試験の実施が原則として必要
であるとの現在の考え方を変更し、利用可能なデータから安全性・忍容性
のリスクが説明でき許容・管理可能な場合には、日本人第Ⅰ相試験を実施
せずとも、国際共同治験に参加できる考え方を原則としてはどうか。
⚫ 日本人第Ⅰ相試験の要否について PMDA と企業の判断の基準にはギャップ
がある。安全性・忍容性のリスク評価についての観点や考え方を可能な限
り具体的に文書化することで、PMDA や治験実施施設、企業(ベンチャー
を含む)を含めた関係者の共通理解を高めたい。
また、現時点の PMDA の考え方としては、次のような内容が示された。
国際共同治験に日本が遅滞なく参加し、迅速な薬事承認に結びつける観点から、
日本人第Ⅰ相試験*の実施に関して、下記のとおり柔軟に対応している。
⚫ 国際共同治験に参加する前に一律に日本人第Ⅰ相試験の実施を求めてはお
らず、その時点で利用可能な情報を基に、疾患と被験薬の特徴も踏まえ
て、その実施の要否を品目ごとに検討している(実際には、さらに患者数
や国際共同治験のスケジュールも考慮)
。
⚫ 具体的に懸念される民族差がないことが明らかな場合には、日本人第Ⅰ相
試験を実施せずとも、国際共同治験に参加することに問題はない。
⚫ 先行する海外試験の情報、類薬の情報、疾患の特性等から具体的に懸念さ
れる民族差とその差の程度が推定できる場合には、日本人第Ⅰ相試験の実
施が不要と判断できる可能性があるため、差の程度に応じて国際共同治験
に参加することの是非を検討し、「是」の場合は、日本人被験者の安全が
確保される試験デザインなのか、さらに精査する。
⚫ 具体的に懸念される民族差が明らかではない場合(検討していない場合、
検討した範囲では差があるかないか判断できない場合も含む)には、日本
人第Ⅰ相試験を実施する意義の有無(必要性)について検討する。
⚫ 以上の検討のもと、国際共同治験に参加する日本人被験者が他の地域の被
験者に比べてより大きなリスクを負わされている可能性が否定できない場
合は、 Safety run in コホートを設ける等の安全対策を求めている。
⚫ なお、これらの考え方を可能な限り具体的に文書化することに一定の意義
はあるが、開発中の被験薬ごとにその特性や対象疾患、類薬の開発状況、
開発ステージなど様々な要因が異なるため、日本人第Ⅰ相試験の要否につ
いて個別の判断が必要となることに留意が必要。
12
の参加の遅れ、日本の不参加、さらには日本での開発断念に繋がる場合がある状
況を踏まえ、日本人第Ⅰ相試験の実施に関して、製薬業界からは次のような意見
を受けている。
⚫ 国際共同治験に参加する前に、日本人第Ⅰ相試験の実施が原則として必要
であるとの現在の考え方を変更し、利用可能なデータから安全性・忍容性
のリスクが説明でき許容・管理可能な場合には、日本人第Ⅰ相試験を実施
せずとも、国際共同治験に参加できる考え方を原則としてはどうか。
⚫ 日本人第Ⅰ相試験の要否について PMDA と企業の判断の基準にはギャップ
がある。安全性・忍容性のリスク評価についての観点や考え方を可能な限
り具体的に文書化することで、PMDA や治験実施施設、企業(ベンチャー
を含む)を含めた関係者の共通理解を高めたい。
また、現時点の PMDA の考え方としては、次のような内容が示された。
国際共同治験に日本が遅滞なく参加し、迅速な薬事承認に結びつける観点から、
日本人第Ⅰ相試験*の実施に関して、下記のとおり柔軟に対応している。
⚫ 国際共同治験に参加する前に一律に日本人第Ⅰ相試験の実施を求めてはお
らず、その時点で利用可能な情報を基に、疾患と被験薬の特徴も踏まえ
て、その実施の要否を品目ごとに検討している(実際には、さらに患者数
や国際共同治験のスケジュールも考慮)
。
⚫ 具体的に懸念される民族差がないことが明らかな場合には、日本人第Ⅰ相
試験を実施せずとも、国際共同治験に参加することに問題はない。
⚫ 先行する海外試験の情報、類薬の情報、疾患の特性等から具体的に懸念さ
れる民族差とその差の程度が推定できる場合には、日本人第Ⅰ相試験の実
施が不要と判断できる可能性があるため、差の程度に応じて国際共同治験
に参加することの是非を検討し、「是」の場合は、日本人被験者の安全が
確保される試験デザインなのか、さらに精査する。
⚫ 具体的に懸念される民族差が明らかではない場合(検討していない場合、
検討した範囲では差があるかないか判断できない場合も含む)には、日本
人第Ⅰ相試験を実施する意義の有無(必要性)について検討する。
⚫ 以上の検討のもと、国際共同治験に参加する日本人被験者が他の地域の被
験者に比べてより大きなリスクを負わされている可能性が否定できない場
合は、 Safety run in コホートを設ける等の安全対策を求めている。
⚫ なお、これらの考え方を可能な限り具体的に文書化することに一定の意義
はあるが、開発中の被験薬ごとにその特性や対象疾患、類薬の開発状況、
開発ステージなど様々な要因が異なるため、日本人第Ⅰ相試験の要否につ
いて個別の判断が必要となることに留意が必要。
12