よむ、つかう、まなぶ。
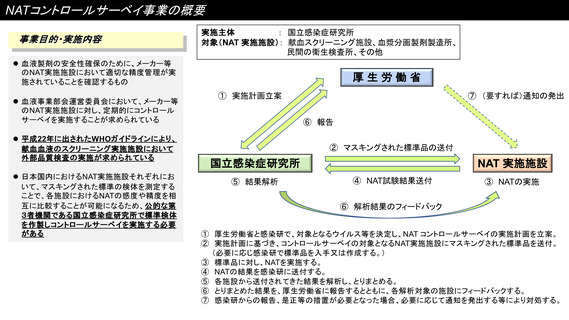
資 料 2 NAT コントロールサーベイ事業 2023 年度 実績報告 (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42777.html |
| 出典情報 | 薬事審議会 血液事業部会 安全技術調査会(令和6年度第1回 8/30)、運営委員会(第2回 8/30)(合同会議)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2) パネルの調製(表2)
材料として、HBV、HCV、HIV-1 および HEV 国内標準品を用いて評価用のパネル
(2 種) を作製した。国内標準品の希釈には、陰性血漿 (HCV 抗体、HBs 抗原、HIV-1/2
抗体、及び HBV、HCV、HIV-1/2、HEV の NAT 全てが陰性)、あるいは 4 ウイルスの
何れかが高濃度 (>3×103 IU /mL) に含まれる陽性血漿を用いた。各標的ウイルスの低
濃度陽性検体として、輸血用血液の NAT で必要とされる検出限界値 (HBV: 100 IU/mL,
HCV: 100 IU/mL, HIV-1: 200 IU/mL, HEV: 未設定) の 1.5 倍あるいは 3 倍濃度にあた
る 300 IU/mL に検体を希釈調製した。陰性対照検体も含めた計 20 検体をブラインド化
したパネルを参加施設に送付した。
スクリーニング試験用パネル:HBV, HCV, HIV-1, HEV の国内標準品を希釈したウイル
ス陽性検体及び陰性血漿検体からなる 11 種類の検体
同定試験用パネル:HBV,HCV,HIV-1 の国内標準品を希釈したウイルス陽性検体及び陰
性血漿検体からなる 9 種類の検体
3) 測定
輸血用血液製剤の NAT 実施施設と研究施設は Procleix UltrioPlex E ABD Assay (グ
リフォルス株式会社) を用いて測定した。この試験法は個別検体のスクリーニング試験
(HBV、HCV、HIV-1/2 を識別せず検出し、同時に HEV を単独で検出する) と HBV、
HCV、HIV-1/2 を識別するための同定試験とから構成されている。参加施設はスクリー
ニング試験と同定試験の両方の試験法を用いて、上記のパネル検体についてそれぞれ日
を変えて 3 回測定した。
4) 結果
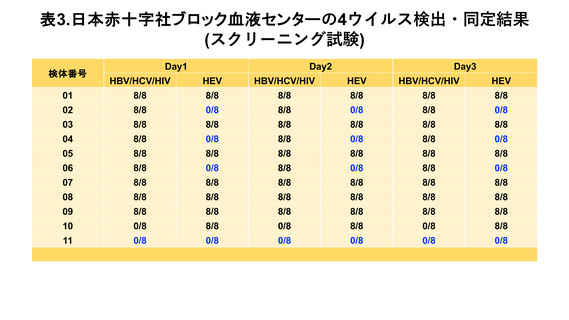
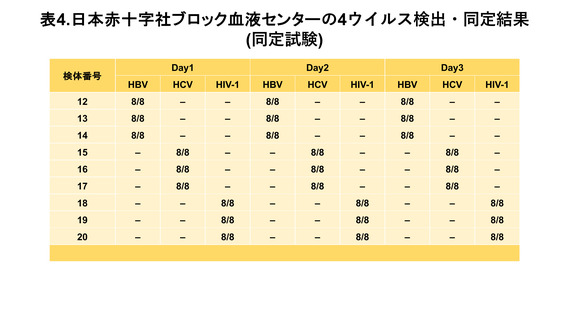
(1) 輸血用血液製剤の NAT(表3および4)
日本赤十字社ブロック血液センター全 8 施設において改正後の NAT ガイドラインに
基づいて実施している NAT 試験は、スクリーニング試験法と同定試験法の両方におい
て HBV、HCV、HIV-1、および HEV に関する精度管理が適切に実施されていた。
全施設において、HBV、HCV、HIV-1 および HEV の低濃度 (300 IU/mL) に希釈さ
れた検体および高濃度の他のウイルスが混在した検体 (>3×103 IU/mL) でも標的のウ
イルスが特異的に検出・同定できることが確認された。陰性対照は全て陰性と判定され
た。
(2) 研究施設における NAT
オブザーバーとして参加した研究施設にて実施されている NAT 試験は HBV、
HCV、
HIV-1 および HEV の低濃度 (300 IU/mL) に希釈された検体および高濃度の他のウイ
ルスが混在した検体 (>3×103 IU/mL) でも標的のウイルスが特異的に検出・同定でき
2
材料として、HBV、HCV、HIV-1 および HEV 国内標準品を用いて評価用のパネル
(2 種) を作製した。国内標準品の希釈には、陰性血漿 (HCV 抗体、HBs 抗原、HIV-1/2
抗体、及び HBV、HCV、HIV-1/2、HEV の NAT 全てが陰性)、あるいは 4 ウイルスの
何れかが高濃度 (>3×103 IU /mL) に含まれる陽性血漿を用いた。各標的ウイルスの低
濃度陽性検体として、輸血用血液の NAT で必要とされる検出限界値 (HBV: 100 IU/mL,
HCV: 100 IU/mL, HIV-1: 200 IU/mL, HEV: 未設定) の 1.5 倍あるいは 3 倍濃度にあた
る 300 IU/mL に検体を希釈調製した。陰性対照検体も含めた計 20 検体をブラインド化
したパネルを参加施設に送付した。
スクリーニング試験用パネル:HBV, HCV, HIV-1, HEV の国内標準品を希釈したウイル
ス陽性検体及び陰性血漿検体からなる 11 種類の検体
同定試験用パネル:HBV,HCV,HIV-1 の国内標準品を希釈したウイルス陽性検体及び陰
性血漿検体からなる 9 種類の検体
3) 測定
輸血用血液製剤の NAT 実施施設と研究施設は Procleix UltrioPlex E ABD Assay (グ
リフォルス株式会社) を用いて測定した。この試験法は個別検体のスクリーニング試験
(HBV、HCV、HIV-1/2 を識別せず検出し、同時に HEV を単独で検出する) と HBV、
HCV、HIV-1/2 を識別するための同定試験とから構成されている。参加施設はスクリー
ニング試験と同定試験の両方の試験法を用いて、上記のパネル検体についてそれぞれ日
を変えて 3 回測定した。
4) 結果
(1) 輸血用血液製剤の NAT(表3および4)
日本赤十字社ブロック血液センター全 8 施設において改正後の NAT ガイドラインに
基づいて実施している NAT 試験は、スクリーニング試験法と同定試験法の両方におい
て HBV、HCV、HIV-1、および HEV に関する精度管理が適切に実施されていた。
全施設において、HBV、HCV、HIV-1 および HEV の低濃度 (300 IU/mL) に希釈さ
れた検体および高濃度の他のウイルスが混在した検体 (>3×103 IU/mL) でも標的のウ
イルスが特異的に検出・同定できることが確認された。陰性対照は全て陰性と判定され
た。
(2) 研究施設における NAT
オブザーバーとして参加した研究施設にて実施されている NAT 試験は HBV、
HCV、
HIV-1 および HEV の低濃度 (300 IU/mL) に希釈された検体および高濃度の他のウイ
ルスが混在した検体 (>3×103 IU/mL) でも標的のウイルスが特異的に検出・同定でき
2