よむ、つかう、まなぶ。
資料1-4「使用上の注意」の改訂について[710KB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53225.html |
| 出典情報 | 薬事審議会 医療機器・再生医療等製品安全対策部会(令和6年度第2回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
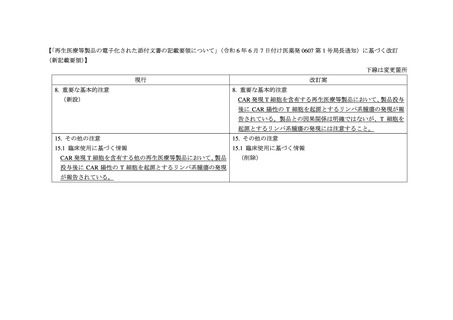
【「再生医療等製品の電子化された添付文書の記載要領について」
(令和 6 年 6 月 7 日付け医薬発 0607 第 1 号局長通知)に基づく改訂
(新記載要領)
】
下線は変更箇所
現行
8. 重要な基本的注意
(新設)
改訂案
8. 重要な基本的注意
CAR 発現 T 細胞を含有する再生医療等製品において、製品投与
後に CAR 陽性の T 細胞を起源とするリンパ系腫瘍の発現が報
告されている。製品との因果関係は明確ではないが、T 細胞を
起源とするリンパ系腫瘍の発現には注意すること。
15. その他の注意
15. その他の注意
15.1 臨床使用に基づく情報
15.1 臨床使用に基づく情報
CAR 発現 T 細胞を含有する他の再生医療等製品において、製品
投与後に CAR 陽性の T 細胞を起源とするリンパ系腫瘍の発現
が報告されている。
(削除)
(令和 6 年 6 月 7 日付け医薬発 0607 第 1 号局長通知)に基づく改訂
(新記載要領)
】
下線は変更箇所
現行
8. 重要な基本的注意
(新設)
改訂案
8. 重要な基本的注意
CAR 発現 T 細胞を含有する再生医療等製品において、製品投与
後に CAR 陽性の T 細胞を起源とするリンパ系腫瘍の発現が報
告されている。製品との因果関係は明確ではないが、T 細胞を
起源とするリンパ系腫瘍の発現には注意すること。
15. その他の注意
15. その他の注意
15.1 臨床使用に基づく情報
15.1 臨床使用に基づく情報
CAR 発現 T 細胞を含有する他の再生医療等製品において、製品
投与後に CAR 陽性の T 細胞を起源とするリンパ系腫瘍の発現
が報告されている。
(削除)