よむ、つかう、まなぶ。
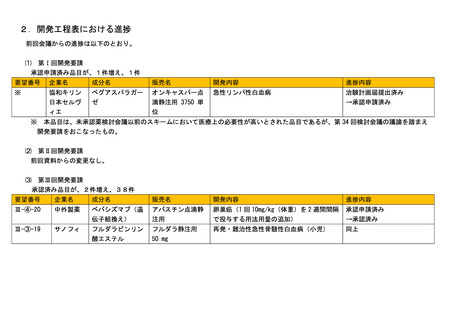
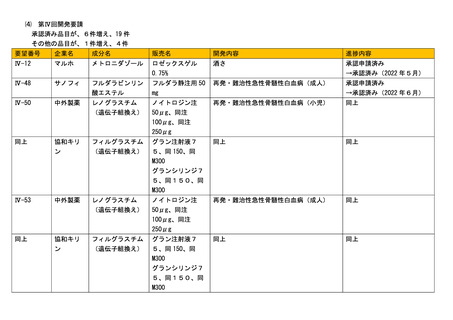
資料5-2 企業から提出された開発工程表における進捗について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00024.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第52回 8/31)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
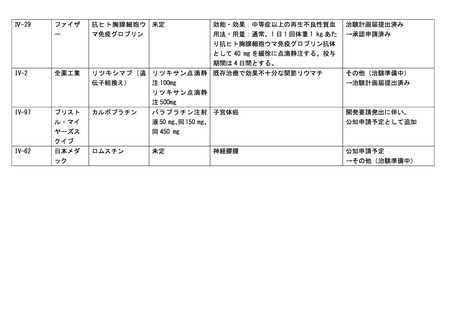
Ⅳ-29
IV-2
ファイザ
抗ヒト胸腺細胞ウ 未定
効能・効果:中等症以上の再生不良性貧血
治験計画届提出済み
ー
マ免疫グロブリン
用法・用量:通常、1 日 1 回体重 1 kg あた
り抗ヒト胸腺細胞ウマ免疫グロブリン抗体
として 40 mg を緩徐に点滴静注する。投与
期間は 4 日間とする。
→承認申請済み
全薬工業
リツキシマブ(遺 リツキサン点滴静 既存治療で効果不十分な関節リウマチ
伝子組換え)
注 100mg
リツキサン点滴静
その他(治験準備中)
→治験計画届提出済み
注 500mg
IV-97
ブリスト
ル・マイ
ヤーズス
クイブ
カルボプラチン
パラプラチン注射 子宮体癌
液 50 mg、同 150 mg、
同 450 mg
開発要請発出に伴い、
公知申請予定として追加
IV-62
日本メダ
ック
ロムスチン
未定
公知申請予定
→その他(治験準備中)
神経膠腫
IV-2
ファイザ
抗ヒト胸腺細胞ウ 未定
効能・効果:中等症以上の再生不良性貧血
治験計画届提出済み
ー
マ免疫グロブリン
用法・用量:通常、1 日 1 回体重 1 kg あた
り抗ヒト胸腺細胞ウマ免疫グロブリン抗体
として 40 mg を緩徐に点滴静注する。投与
期間は 4 日間とする。
→承認申請済み
全薬工業
リツキシマブ(遺 リツキサン点滴静 既存治療で効果不十分な関節リウマチ
伝子組換え)
注 100mg
リツキサン点滴静
その他(治験準備中)
→治験計画届提出済み
注 500mg
IV-97
ブリスト
ル・マイ
ヤーズス
クイブ
カルボプラチン
パラプラチン注射 子宮体癌
液 50 mg、同 150 mg、
同 450 mg
開発要請発出に伴い、
公知申請予定として追加
IV-62
日本メダ
ック
ロムスチン
未定
公知申請予定
→その他(治験準備中)
神経膠腫