よむ、つかう、まなぶ。
参考資料9 「定期の予防接種等による副反応疑いの報告等の取扱いについて」の一部改正について(令和3年12月6日付け健発1206第84号・薬生発1206第2号厚生労働省健康局長及び医薬・生活衛生局長連名通知) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00052.html |
| 出典情報 | 第85回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第14回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(10/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
参考資料9
令和3年 12 月6日
健発 1206 第 84 号
薬生発 1206 第2号
各都道府県知事 殿
厚 生 労 働 省 健 康 局 長
(
公
印
省
略
)
厚生労働省医薬・生活衛生局長
(
公
印
省
略
)
「定期の予防接種等による副反応疑いの報告等の取扱いについて」の一部改正について
予防接種法(昭和 23 年法律第 68 号)第 12 条第1項の規定による報告及び予防接種に係
る医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第
145 号)第 68 条の 10 第2項の規定による報告については、「定期の予防接種等による副反
応疑いの報告等の取扱いについて」(平成 25 年3月 30 日付け健発 0330 第3号・薬食発
0330 第1号厚生労働省健康局長、医薬食品局長連名通知。以下「連名通知」という。
)に
従い、御理解と御協力をいただいているところです。
今般、連名通知の一部を別紙のとおり改正することといたしましたので、貴職におかれ
ましてはこれを十分御了知の上、貴管内市町村(保健所を設置する市及び特別区を含む。)
及び関係機関等に周知をお願いいたします。
なお、公益社団法人日本医師会に対し、本件に係る協力を依頼していることを申し添え
ます。
記
1
改正の概要
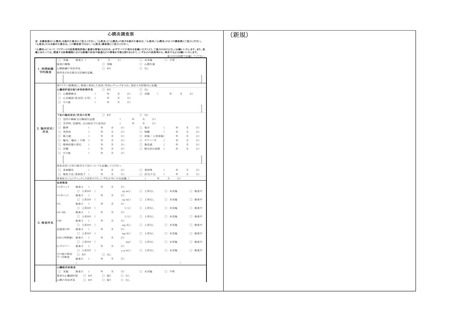
(1)別紙様式1について、新型コロナウイルス感染症に係るワクチンに関する報告基
準として心筋炎及び心膜炎を追加し、かつそれぞれについて報告に係る調査票を追
加。
(2)血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)(TTS)調査
票を独立行政法人医薬品医療機器総合機構に報告する場合に、電子報告システムに
よる報告に対応。
(3)その他所要の改正。
2
適用日
令和3年 12 月6日
令和3年 12 月6日
健発 1206 第 84 号
薬生発 1206 第2号
各都道府県知事 殿
厚 生 労 働 省 健 康 局 長
(
公
印
省
略
)
厚生労働省医薬・生活衛生局長
(
公
印
省
略
)
「定期の予防接種等による副反応疑いの報告等の取扱いについて」の一部改正について
予防接種法(昭和 23 年法律第 68 号)第 12 条第1項の規定による報告及び予防接種に係
る医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第
145 号)第 68 条の 10 第2項の規定による報告については、「定期の予防接種等による副反
応疑いの報告等の取扱いについて」(平成 25 年3月 30 日付け健発 0330 第3号・薬食発
0330 第1号厚生労働省健康局長、医薬食品局長連名通知。以下「連名通知」という。
)に
従い、御理解と御協力をいただいているところです。
今般、連名通知の一部を別紙のとおり改正することといたしましたので、貴職におかれ
ましてはこれを十分御了知の上、貴管内市町村(保健所を設置する市及び特別区を含む。)
及び関係機関等に周知をお願いいたします。
なお、公益社団法人日本医師会に対し、本件に係る協力を依頼していることを申し添え
ます。
記
1
改正の概要
(1)別紙様式1について、新型コロナウイルス感染症に係るワクチンに関する報告基
準として心筋炎及び心膜炎を追加し、かつそれぞれについて報告に係る調査票を追
加。
(2)血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)(TTS)調査
票を独立行政法人医薬品医療機器総合機構に報告する場合に、電子報告システムに
よる報告に対応。
(3)その他所要の改正。
2
適用日
令和3年 12 月6日