よむ、つかう、まなぶ。
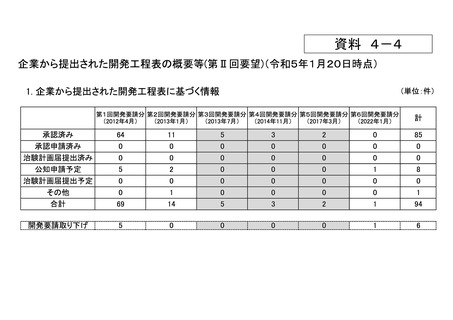
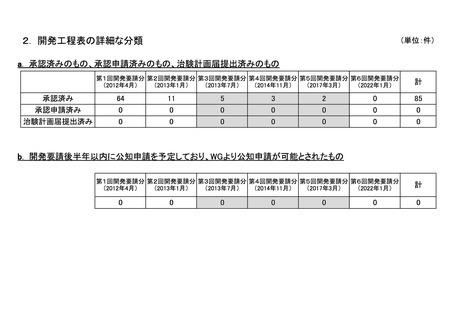
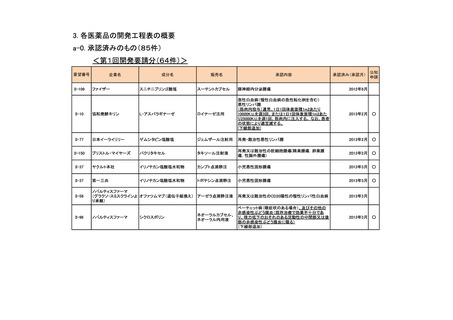
資料4-4 企業から提出された開発工程表の概要等(第II回要望) (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
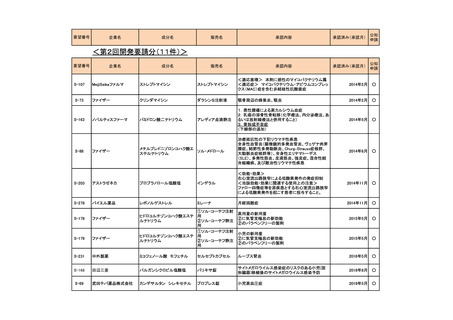
要望番号
企業名
成分名
販売名
承認内容
承認済み(承認月)
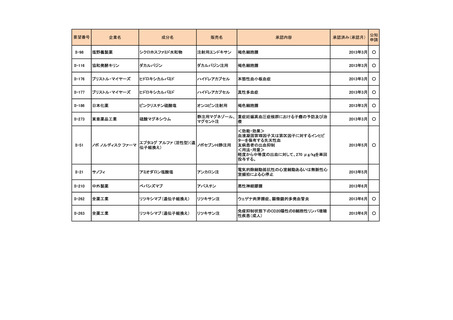
II-81
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
小腸移植後の治療抵抗性の拒絶反応の治療(小児)
ブリン
静注用
り承継)
2014年9月
II-82
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
心移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-83
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
肺移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-84
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
肝臓移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-85
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
膵臓移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-86
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
小腸移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-124
協和発酵キリン
ダルベポエチン アルファ(遺伝
ネスプ注射液
子組換え)
骨髄異形成症候群に伴う貧血
II-276
ユーシービージャパン
レベチラセタム
イーケプラ錠
成人における部分発作(二次性全般化発作を含む)
に対する単独療法
2015年2月
リツキサン注
CD20陽性の低悪性度又は濾胞性のB細胞性非ホジ
キンリンパ腫に関する維持療法の用法・用量の追加
(下記)
維持療法に用いる場合は、通常、成人には、リツキシ
マブ(遺伝子組換え)として1回量375mg/m2を点滴静
注する。投与間隔は8週間を目安とし、最大投与回数
は12回とする。
2015年5月
II-268
全薬工業
リツキシマブ(遺伝子組換え)
2014年12月
公知
申請
企業名
成分名
販売名
承認内容
承認済み(承認月)
II-81
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
小腸移植後の治療抵抗性の拒絶反応の治療(小児)
ブリン
静注用
り承継)
2014年9月
II-82
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
心移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-83
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
肺移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-84
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
肝臓移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-85
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
膵臓移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-86
サノフィ
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
(ジェンザイム・ジャパンよ
小腸移植後の治療抵抗性の拒絶反応の治療(成人)
ブリン
静注用
り承継)
2014年9月
II-124
協和発酵キリン
ダルベポエチン アルファ(遺伝
ネスプ注射液
子組換え)
骨髄異形成症候群に伴う貧血
II-276
ユーシービージャパン
レベチラセタム
イーケプラ錠
成人における部分発作(二次性全般化発作を含む)
に対する単独療法
2015年2月
リツキサン注
CD20陽性の低悪性度又は濾胞性のB細胞性非ホジ
キンリンパ腫に関する維持療法の用法・用量の追加
(下記)
維持療法に用いる場合は、通常、成人には、リツキシ
マブ(遺伝子組換え)として1回量375mg/m2を点滴静
注する。投与間隔は8週間を目安とし、最大投与回数
は12回とする。
2015年5月
II-268
全薬工業
リツキシマブ(遺伝子組換え)
2014年12月
公知
申請