よむ、つかう、まなぶ。
資料2-4 要指導医薬品のリスク評価(イソコナゾール) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和5年3月2日
令和4年度第4回医薬品等安全対策部会
資料2-4
要指導医薬品のリスク評価について
○ 令和4年 12 月 27 日開催の安全対策調査会において、現在要指導医薬品に指定
されているイソコナゾールについて、製造販売後調査期間の終了見込みに伴
い、一般用医薬品としての適切性を確認するためのリスク評価を行った。
成分・含量
イソコナゾール硝酸塩 600mg(1錠中)
薬効分類
抗真菌剤
投与経路
外用
販売名(製造販売業 ①メンソレータムフレディ CC1
者)
②メンソレータムフレディ CC1A
(ロート製薬株式会社)
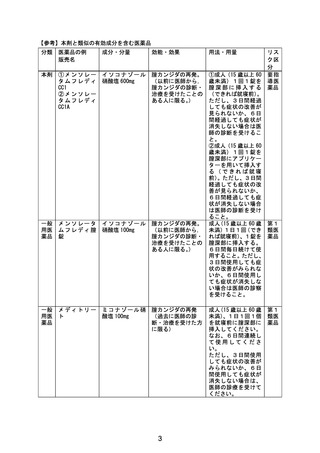
効能・効果
腟カンジダの再発(以前に医師から、膣カンジダの診断・治
療を受けたことのある人に限る。)
用法・用量
①成人(15 歳以上 60 歳未満)1回1錠を膣深部に挿入する
(できれば就寝前)。ただし、3日間経過しても症状の改善
が見られないか、6日間経過しても症状が消失しない場合は
医師の診断を受けること。
②成人(15 歳以上 60 歳未満)1回1錠を膣深部にアプリケ
ーターを用いて挿入する(できれば就寝前)。ただし、3日間
経過しても症状の改善が見られないか、6日間経過しても症
状が消失しない場合は医師の診断を受けること。
承認年月日
2019 年 11 月 27 日
製造販売開始日
2020 年1月 20 日
評価を行う理由
2023 年1月 19 日の製造販売後調査終了見込みに伴い、一般
用医薬品としての販売の可否について判断を行うため
製造販売後調査概要
(中間報告書)
調査期間:2020 年1月 20 日~2022 年8月 30 日
特別調査:1,000 症例
副作用:53 例 107 件(5.3%)
うち重篤な副作用:なし
未知の副作用:月経中間期出血(不正出血)、細菌性外陰
腟炎、腟部異臭、頻尿、不眠症、悪心各
1件
一般調査
副作用:95 例 137 件
うち重篤な副作用:なし
未知の副作用:異物感(7 件)、出血(5 件)、下腹部痛(3
件)、月経障害(2 件)、口渇(2 件)、腹
1
令和4年度第4回医薬品等安全対策部会
資料2-4
要指導医薬品のリスク評価について
○ 令和4年 12 月 27 日開催の安全対策調査会において、現在要指導医薬品に指定
されているイソコナゾールについて、製造販売後調査期間の終了見込みに伴
い、一般用医薬品としての適切性を確認するためのリスク評価を行った。
成分・含量
イソコナゾール硝酸塩 600mg(1錠中)
薬効分類
抗真菌剤
投与経路
外用
販売名(製造販売業 ①メンソレータムフレディ CC1
者)
②メンソレータムフレディ CC1A
(ロート製薬株式会社)
効能・効果
腟カンジダの再発(以前に医師から、膣カンジダの診断・治
療を受けたことのある人に限る。)
用法・用量
①成人(15 歳以上 60 歳未満)1回1錠を膣深部に挿入する
(できれば就寝前)。ただし、3日間経過しても症状の改善
が見られないか、6日間経過しても症状が消失しない場合は
医師の診断を受けること。
②成人(15 歳以上 60 歳未満)1回1錠を膣深部にアプリケ
ーターを用いて挿入する(できれば就寝前)。ただし、3日間
経過しても症状の改善が見られないか、6日間経過しても症
状が消失しない場合は医師の診断を受けること。
承認年月日
2019 年 11 月 27 日
製造販売開始日
2020 年1月 20 日
評価を行う理由
2023 年1月 19 日の製造販売後調査終了見込みに伴い、一般
用医薬品としての販売の可否について判断を行うため
製造販売後調査概要
(中間報告書)
調査期間:2020 年1月 20 日~2022 年8月 30 日
特別調査:1,000 症例
副作用:53 例 107 件(5.3%)
うち重篤な副作用:なし
未知の副作用:月経中間期出血(不正出血)、細菌性外陰
腟炎、腟部異臭、頻尿、不眠症、悪心各
1件
一般調査
副作用:95 例 137 件
うち重篤な副作用:なし
未知の副作用:異物感(7 件)、出血(5 件)、下腹部痛(3
件)、月経障害(2 件)、口渇(2 件)、腹
1