よむ、つかう、まなぶ。
資料3 先進医療Bの試験実施計画の変更について(告示番号66/ jRCTs031220351) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_33355.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第149回 6/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先進医療Bの試験実施計画の変更について
【申請医療機関】
東北大学病院
【先進医療告示番号と名称】
大臣告示番号 B66
術前のゲムシタビン静脈内投与及びナブ―パクリタキセル静脈内投与の併用療法
【適応症】
切除が可能な膵臓がん(七十歳以上八十歳未満の患者に係るものに限る。)
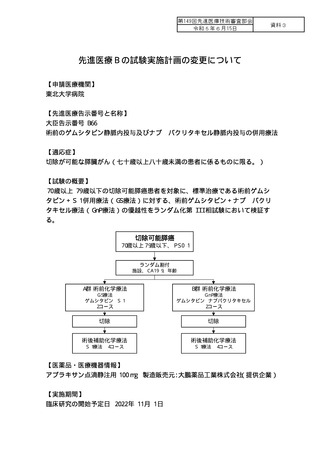
【試験の概要】
70 歳以上 79 歳以下の切除可能膵癌患者を対象に、標準治療である術前ゲムシ
タビン+S-1 併用療法(GS 療法)に対する、術前ゲムシタビン+ナブ―パクリ
タキセル療法(GnP 療法)の優越性をランダム化第 III 相試験において検証す
る。
切除可能膵癌
70歳以上79歳以下、PS0-1
ランダム割付
施設、CA19-9、年齢
A群 術前化学療法
B群 術前化学療法
GS療法
ゲムシタビン+S-1
GnP療法
ゲムシタビン+ナブパクリタキセル
切除
切除
術後補助化学療法
術後補助化学療法
2コース
2コース
S-1療法 4コース
【医薬品・医療機器情報】
アブラキサン点滴静注用 100 mg
S-1療法
4コース
製造販売元:大鵬薬品工業株式会社(提供企業)
【実施期間】
臨床研究の開始予定日 2022 年 11 月 1 日
【申請医療機関】
東北大学病院
【先進医療告示番号と名称】
大臣告示番号 B66
術前のゲムシタビン静脈内投与及びナブ―パクリタキセル静脈内投与の併用療法
【適応症】
切除が可能な膵臓がん(七十歳以上八十歳未満の患者に係るものに限る。)
【試験の概要】
70 歳以上 79 歳以下の切除可能膵癌患者を対象に、標準治療である術前ゲムシ
タビン+S-1 併用療法(GS 療法)に対する、術前ゲムシタビン+ナブ―パクリ
タキセル療法(GnP 療法)の優越性をランダム化第 III 相試験において検証す
る。
切除可能膵癌
70歳以上79歳以下、PS0-1
ランダム割付
施設、CA19-9、年齢
A群 術前化学療法
B群 術前化学療法
GS療法
ゲムシタビン+S-1
GnP療法
ゲムシタビン+ナブパクリタキセル
切除
切除
術後補助化学療法
術後補助化学療法
2コース
2コース
S-1療法 4コース
【医薬品・医療機器情報】
アブラキサン点滴静注用 100 mg
S-1療法
4コース
製造販売元:大鵬薬品工業株式会社(提供企業)
【実施期間】
臨床研究の開始予定日 2022 年 11 月 1 日