よむ、つかう、まなぶ。
医療機器のサイバーセキュリティに関する質疑応答集(Q&A)について (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190382_00016.html |
| 出典情報 | 薬事・食品衛生審議会 医療機器・再生医療等製品安全対策部会(令和5年度第2回 3/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Q4:承認申請・認証申請において基本要件基準第 12 条第 3 項への適合を示す際、試験機関
による JIS T 81001-5-1 への適合証明書を特定することで良いか。
A4:基本要件基準第 12 条第 3 項の適合性の確認のための第三者機関による試験は必須では
ないが、試験機関を活用した場合、申請時においては、適合証明書に加えて、令和5年5
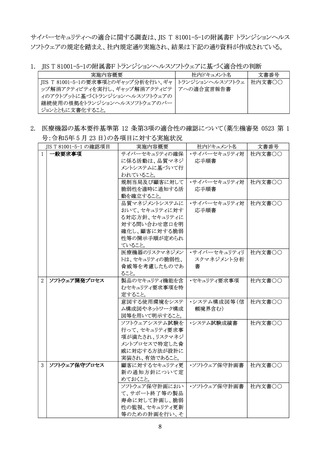
月 23 日付け薬生機審発 0523 第1号厚生労働省医薬・生活衛生局医療機器審査管理課
長通知の「2. JIS に関連する既存通知等の要求事項」に記載されている項目に対する適合
性の確認結果を示すか又は確認結果をまとめた社内文書等を特定すること。
Q5:承認審査の際に要求されるサイバーセキュリティに係る別添資料は、信頼性書面調査(非
臨床)の対象になるのか。もし対象になる場合、提出すべき根拠資料は何か。
A5:令和4年8月8日付薬生機審発 0808 第1号の適合性書面調査実施要領にあるとおり、規則
第 114 条の 19 第1項第1号のロ及びホに規定する資料は、調査対象となる承認申請資料
となっており、サイバーセキュリティに係る別添資料も信頼性調査の対象になり得る。なお、
対象になった場合は、別添資料に添付する社内文書が根拠資料となる。
Q6:医療情報システムを対象とした「医療情報システムの安全管理に関するガイドライン」は、
いわゆる「3省2ガイドライン」と呼ばれているもののひとつであるが、この「医療情報システ
ムの安全管理に関するガイドライン」は医療機器も対象として扱われるガイドラインなのか。
A6:「医療情報システムの安全管理に関するガイドライン」は、医療情報(医療に関する患者情
報(個人識別情報)を含む情報)を取り扱う医療機器(電子カルテ等医療情報を扱うシステ
ムとネットワークがつながっている医療機器も含む)においても対応が必要となる。なお、医
療情報の定義については、医療情報システムの安全管理に関するガイドライン 第 6.0 版
(令和5年5月)用語集を参照すること。
Q7:令和5年5月 23 日付け薬生機審発 0523 第1号厚生労働省医薬・生活衛生局医療機器審
査管理課長通知に「セキュリティ設計のベストプラクティスを考慮した設計」とあるが、具体
的に参考となる資料などはあるか。
A7:セキュリティ設計のベストプラクティスについては、JIS T 81001-5-1 の 5.3.2 及び 5.4.1 に
例示されている。その他、令和5年3月 31 日付け薬生機審発 0331 第 11 号・薬生安発
0331 第4号厚生労働省医薬・生活衛生局医療機器審査管理課長・医薬安全対策課長
連名通知の別添「医療機器のサイバーセキュリティ導入に関する手引書(第2版)」の「5.1
セキュリティ要求事項及びアーキテクチャー設計」も参照すること。
2
による JIS T 81001-5-1 への適合証明書を特定することで良いか。
A4:基本要件基準第 12 条第 3 項の適合性の確認のための第三者機関による試験は必須では
ないが、試験機関を活用した場合、申請時においては、適合証明書に加えて、令和5年5
月 23 日付け薬生機審発 0523 第1号厚生労働省医薬・生活衛生局医療機器審査管理課
長通知の「2. JIS に関連する既存通知等の要求事項」に記載されている項目に対する適合
性の確認結果を示すか又は確認結果をまとめた社内文書等を特定すること。
Q5:承認審査の際に要求されるサイバーセキュリティに係る別添資料は、信頼性書面調査(非
臨床)の対象になるのか。もし対象になる場合、提出すべき根拠資料は何か。
A5:令和4年8月8日付薬生機審発 0808 第1号の適合性書面調査実施要領にあるとおり、規則
第 114 条の 19 第1項第1号のロ及びホに規定する資料は、調査対象となる承認申請資料
となっており、サイバーセキュリティに係る別添資料も信頼性調査の対象になり得る。なお、
対象になった場合は、別添資料に添付する社内文書が根拠資料となる。
Q6:医療情報システムを対象とした「医療情報システムの安全管理に関するガイドライン」は、
いわゆる「3省2ガイドライン」と呼ばれているもののひとつであるが、この「医療情報システ
ムの安全管理に関するガイドライン」は医療機器も対象として扱われるガイドラインなのか。
A6:「医療情報システムの安全管理に関するガイドライン」は、医療情報(医療に関する患者情
報(個人識別情報)を含む情報)を取り扱う医療機器(電子カルテ等医療情報を扱うシステ
ムとネットワークがつながっている医療機器も含む)においても対応が必要となる。なお、医
療情報の定義については、医療情報システムの安全管理に関するガイドライン 第 6.0 版
(令和5年5月)用語集を参照すること。
Q7:令和5年5月 23 日付け薬生機審発 0523 第1号厚生労働省医薬・生活衛生局医療機器審
査管理課長通知に「セキュリティ設計のベストプラクティスを考慮した設計」とあるが、具体
的に参考となる資料などはあるか。
A7:セキュリティ設計のベストプラクティスについては、JIS T 81001-5-1 の 5.3.2 及び 5.4.1 に
例示されている。その他、令和5年3月 31 日付け薬生機審発 0331 第 11 号・薬生安発
0331 第4号厚生労働省医薬・生活衛生局医療機器審査管理課長・医薬安全対策課長
連名通知の別添「医療機器のサイバーセキュリティ導入に関する手引書(第2版)」の「5.1
セキュリティ要求事項及びアーキテクチャー設計」も参照すること。
2