よむ、つかう、まなぶ。
【資料2】創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(概要)(医薬局提出資料)[1.5MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41120.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第16回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会
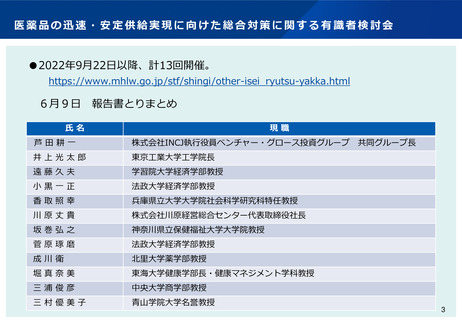
• 昨年から開始された「医薬品の迅速・安定供給実現に向けた総合対策に関する有識者検討会」においては、医薬
品の早期上市や安定供給を図る観点から、幅広い観点で議論がなされ、令和5年6月9日にとりまとめられてお
り、薬事規制のあり方等関係についても課題が指摘されている。
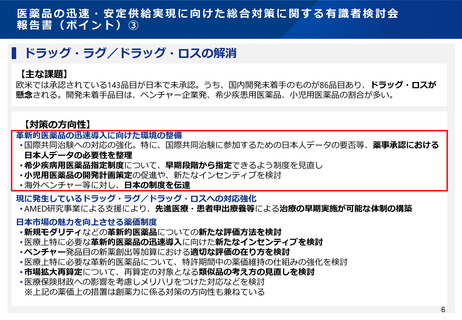
• 具体的には、いわゆるドラッグロス問題の解消や、安定供給の確保、小児医薬品開発の促進等を図るため、薬事
規制のあり方を検討する必要がある。
• このため、本検討会を立ち上げ、これらの論点について議論を行い、令和6年4月24日に報告書をとりまとめた。
スケジュール
検討事項
開発促進
臨床試験
希少疾病用医薬品の指定のあり方について
小児用医薬品の開発促進に資する薬事審査等のあり方について
我が国の承認審査における日本人データの必要性の整理について
治験の更なる効率化(エコシステム)について
市販後
安全対策
製造販売後に実施する使用成績調査等のあり方について
リアルワールドデータの活用のあり方について
品質
医薬品の製造方法等に係る薬事審査等のあり方について
情報発信
令和5年7月10日
希少疾病用医薬品、小児用医薬品
8月7日
日本人第Ⅰ相試験
9月13日
日本人第Ⅰ相試験
10月13日
製造方法等
11月15日
GMP、海外情報発信
12月13日
日本人データ、迅速承認
令和6年1月12日
使用成績調査、RWD
2月8日
日本人データ、迅速承認
3月21日
使用成績調査・RWD、治験エコシステム、
PMDAの体制等
4月24日
報告書とりまとめ
我が国の薬事制度に関する海外への情報発信について
10
• 昨年から開始された「医薬品の迅速・安定供給実現に向けた総合対策に関する有識者検討会」においては、医薬
品の早期上市や安定供給を図る観点から、幅広い観点で議論がなされ、令和5年6月9日にとりまとめられてお
り、薬事規制のあり方等関係についても課題が指摘されている。
• 具体的には、いわゆるドラッグロス問題の解消や、安定供給の確保、小児医薬品開発の促進等を図るため、薬事
規制のあり方を検討する必要がある。
• このため、本検討会を立ち上げ、これらの論点について議論を行い、令和6年4月24日に報告書をとりまとめた。
スケジュール
検討事項
開発促進
臨床試験
希少疾病用医薬品の指定のあり方について
小児用医薬品の開発促進に資する薬事審査等のあり方について
我が国の承認審査における日本人データの必要性の整理について
治験の更なる効率化(エコシステム)について
市販後
安全対策
製造販売後に実施する使用成績調査等のあり方について
リアルワールドデータの活用のあり方について
品質
医薬品の製造方法等に係る薬事審査等のあり方について
情報発信
令和5年7月10日
希少疾病用医薬品、小児用医薬品
8月7日
日本人第Ⅰ相試験
9月13日
日本人第Ⅰ相試験
10月13日
製造方法等
11月15日
GMP、海外情報発信
12月13日
日本人データ、迅速承認
令和6年1月12日
使用成績調査、RWD
2月8日
日本人データ、迅速承認
3月21日
使用成績調査・RWD、治験エコシステム、
PMDAの体制等
4月24日
報告書とりまとめ
我が国の薬事制度に関する海外への情報発信について
10