よむ、つかう、まなぶ。
議題3 参考資料4(先-5) (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42187.html |
| 出典情報 | 先進医療会議(第134回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
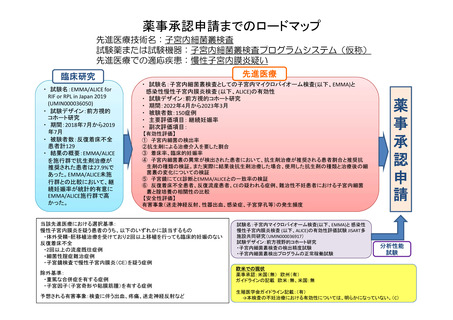
薬事承認申請までのロードマップ
先進医療技術名:子宮内細菌叢検査
試験薬または試験機器:子宮内細菌叢検査プログラムシステム(仮称)
先進医療での適応疾患:慢性子宮内膜炎疑い
先進医療
臨床研究
・ 試験名:EMMA/ALICE for
RIF or RPL in Japan 2019
(UMIN000036050)
・ 試験デザイン:前方視的
コホート研究
・ 期間:2018年7月から2019
年7月
・ 被験者数:反復着床不全
患者計129
・ 結果の概要:EMMA/ALICE
を施行群で抗生剤治療が
推奨された患者は27.9%で
あった。EMMA/ALICE未施
行群との比較において、継
続妊娠率が統計的有意に
EMMA/ALICE施行群で高
かった。
・ 試験名:子宮内細菌叢検査としての子宮内マイクロバイオーム検査(以下、EMMA)と
感染性慢性子宮内膜炎検査 (以下、ALICE)の有効性
・ 試験デザイン:前方視的コホート研究
・ 期間:2022年4月から2023年3月
・ 被験者数:150症例
・ 主要評価項目: 継続妊娠率
・ 副次評価項目:
【有効性評価】
① 子宮内細菌の検出率
②抗生剤による治療介入を要した割合
③ 着床率、臨床的妊娠率
④ 子宮内細菌叢の異常が検出された患者において、抗生剤治療が推奨される患者割合と推奨抗
生剤の種類の検証。また実際に結果後抗生剤治療した場合、使用した抗生剤の種類と治療後の細
菌叢の変化についての検証
⑤ 子宮鏡にてCE診断とEMMA/ALICEとの一致率の検証
⑥ 反復着床不全患者、反復流産患者、CEの疑われる症例、難治性不妊患者における子宮内細菌
叢と腟培養の相関性の比較
【安全性評価】
有害事象(迷走神経反射、性器出血、感染症、子宮穿孔等)の発生頻度
当該先進医療における選択基準:
慢性子宮内膜炎を疑う患者のうち、以下のいずれかに該当するもの
・体外受精-胚移植治療を受けており2回以上移植を行っても臨床的妊娠のない
反復着床不全
・2回以上の流産既往症例
・細菌性腟症難治症例
・子宮鏡検査で慢性子宮内膜炎(CE)を疑う症例
試験名:子宮内マイクロバイオーム検査(以下、EMMA)と 感染性
慢性子宮内膜炎検査 (以下、ALICE)の有効性評価試験 JISART多
施設共同研究(UMIN000036917)
試験デザイン:前方視野的コホート研究
・子宮内細菌叢検査の検出精度試験
・子宮内細菌叢検出プログラムの正常稼働試験
薬
事
承
認
申
請
分析性能
試験
欧米での現状
薬事承認:米国(無) 欧州(有)
ガイドラインの記載 欧米:無、米国:無
除外基準:
・重篤な合併症を有する症例
・子宮因子(子宮奇形や粘膜筋腫)を有する症例
予想される有害事象:検査に伴う出血、疼痛、迷走神経反射など
12
生殖医学会ガイドライン記載:(有)
→本検査の不妊治療における有効性については、明らかになっていない。(C)
先進医療技術名:子宮内細菌叢検査
試験薬または試験機器:子宮内細菌叢検査プログラムシステム(仮称)
先進医療での適応疾患:慢性子宮内膜炎疑い
先進医療
臨床研究
・ 試験名:EMMA/ALICE for
RIF or RPL in Japan 2019
(UMIN000036050)
・ 試験デザイン:前方視的
コホート研究
・ 期間:2018年7月から2019
年7月
・ 被験者数:反復着床不全
患者計129
・ 結果の概要:EMMA/ALICE
を施行群で抗生剤治療が
推奨された患者は27.9%で
あった。EMMA/ALICE未施
行群との比較において、継
続妊娠率が統計的有意に
EMMA/ALICE施行群で高
かった。
・ 試験名:子宮内細菌叢検査としての子宮内マイクロバイオーム検査(以下、EMMA)と
感染性慢性子宮内膜炎検査 (以下、ALICE)の有効性
・ 試験デザイン:前方視的コホート研究
・ 期間:2022年4月から2023年3月
・ 被験者数:150症例
・ 主要評価項目: 継続妊娠率
・ 副次評価項目:
【有効性評価】
① 子宮内細菌の検出率
②抗生剤による治療介入を要した割合
③ 着床率、臨床的妊娠率
④ 子宮内細菌叢の異常が検出された患者において、抗生剤治療が推奨される患者割合と推奨抗
生剤の種類の検証。また実際に結果後抗生剤治療した場合、使用した抗生剤の種類と治療後の細
菌叢の変化についての検証
⑤ 子宮鏡にてCE診断とEMMA/ALICEとの一致率の検証
⑥ 反復着床不全患者、反復流産患者、CEの疑われる症例、難治性不妊患者における子宮内細菌
叢と腟培養の相関性の比較
【安全性評価】
有害事象(迷走神経反射、性器出血、感染症、子宮穿孔等)の発生頻度
当該先進医療における選択基準:
慢性子宮内膜炎を疑う患者のうち、以下のいずれかに該当するもの
・体外受精-胚移植治療を受けており2回以上移植を行っても臨床的妊娠のない
反復着床不全
・2回以上の流産既往症例
・細菌性腟症難治症例
・子宮鏡検査で慢性子宮内膜炎(CE)を疑う症例
試験名:子宮内マイクロバイオーム検査(以下、EMMA)と 感染性
慢性子宮内膜炎検査 (以下、ALICE)の有効性評価試験 JISART多
施設共同研究(UMIN000036917)
試験デザイン:前方視野的コホート研究
・子宮内細菌叢検査の検出精度試験
・子宮内細菌叢検出プログラムの正常稼働試験
薬
事
承
認
申
請
分析性能
試験
欧米での現状
薬事承認:米国(無) 欧州(有)
ガイドラインの記載 欧米:無、米国:無
除外基準:
・重篤な合併症を有する症例
・子宮因子(子宮奇形や粘膜筋腫)を有する症例
予想される有害事象:検査に伴う出血、疼痛、迷走神経反射など
12
生殖医学会ガイドライン記載:(有)
→本検査の不妊治療における有効性については、明らかになっていない。(C)