よむ、つかう、まなぶ。
資 料 1 感染症安全対策体制整備事業(令和5年度)実績報告 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42777.html |
| 出典情報 | 薬事審議会 血液事業部会 安全技術調査会(令和6年度第1回 8/30)、運営委員会(第2回 8/30)(合同会議)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
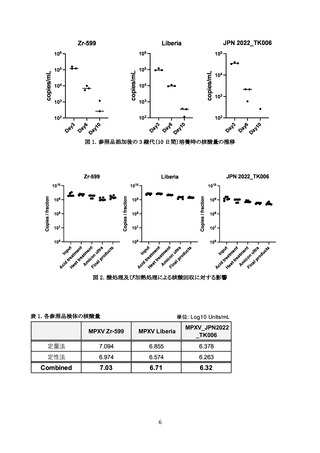
3-3. 国内参照品を用いた相対評価による施設間差の改善
共同測定に参加した各施設における MPXV_JPN2022_TK006、MPXV Zr-599、MPXV Liberia の
核酸量の絶対評価値を図 4 左側のヒストグラムに⽰した(数値は施設番号)。さらに、参照品に定め
た MPXV_JPN2022_TK006 の値を元に相対的に算出した MPXV Zr-599、MPXV Liberia の核酸量
を図 4 右側のヒストグラムに⽰した。いずれの検体においても相対評価によりヒストグラムの横幅
が縮⼩し、施設間差の改善が認められ、参照品整備の有⽤性が⽰された。
4.
考察と課題
MPXV の核酸検査のための国内参照品の整備
本事業において、令和 5 年度は 2022 年に世界的で大流行した MPXV_JPN2022_TK006 株(クレード 2b)
の国内参照品、および、参照パネルとして MPXV Zr-599 株(クレード 1a)と MPXV Liberia 株(クレード 2a)
の計 3 種を整備した。Mpox の輸血感染リスクについては、(ⅰ) これまでに輸血による Mpox 感染事例の報
告はないこと、(ⅱ) ウイルス血症の持続期間については明らかになっておらず、血液からウイルス核酸が検
出される場合でも感染性を有するウイルスは分離されていないこと、(ⅲ) 日本では MSM の献血は出来ない
こと、(ⅳ) 新しいパートナーとの性的行為後 3 ヶ月の献血延期期間が設けられていること、(v) 海外から帰
国された方の 4 週間の献血延期措置が設定されていることなどを総合的に考慮すると、現在のところ輸血
による Mpox 感染のリスクは低いと考えられる。しかし、今後新たな株の出現等によりアウトブレイクが起こる
可能性はあり、感染症のアウトブレイクの際には、新型コロナウイルス感染症の時のように複数の施設で
PCR を実施することが考えられる。現在の技術レベルにおいて、アッセイごとに検出できる核酸量に大きな
差はないと考えられるが、測定キット等により、測定に必要な検体量、抽出量、PCR 反応に用いる検体量が
異なるため、採取検体中から検出できる最低ウイルス量も異なると考えられる。共同測定で算出した各施設
の核酸絶対量は、図 3 左のヒストグラムに示すように約 100 倍の開きがあるが、図 3 右のヒストグラムに示す
ように、国内参照品として定めた MPXV_JPN2022_TK006 を用いて相対的に MPXV Zr-599 と MPXV Liberia
の核酸量を算出すると、施設間差はハーフログ程度に縮小されることが認められた。このことから、国内参
照品を整備しておくことの有用性が改めて示唆され、血液の安全性の確保や公衆衛生の維持に有用であ
ると考えられた。今後は必要に応じて、国立感染症研究所への依頼により次世代生物学的製剤研究セン
ターから参照品を提供できるしくみを整えると共に、MPXV の国際標準品が出来た際には、再評価を実施
して IU/mL の核酸量を付与し、他国とも比較できるように準備する予定である。
5.
海外における血液安全に関する情報の収集および交換
WHO の血液製剤に関する各種会合に定期的に参加し、感染症リスクの早期察知および評価に基づく安
全対策の検討を行った。また、国立感染症研究所の病原体関連部署と連携し、情報の収集や交換を行っ
た。
6.
結論
本事業では、血液を介して感染し得る病原体に関する情報を継続して収集し、日本にリスクのある病原
体については必要に応じて核酸検査のための国内参照品を整備し、我が国での新興・再興感染症の流行
やアウトブレイクに備えた体制整備に貢献する。令和 5 年度は、MPXV の国内参照品を整備し、共同測定
により核酸量(U/mL)を付与した。いずれの施設で実施する核酸検査であっても国内外のキットを用いて検
出感度を比較できる体制が整った。今後も血液を介して感染する新たな病原体等について常に注視して
3
共同測定に参加した各施設における MPXV_JPN2022_TK006、MPXV Zr-599、MPXV Liberia の
核酸量の絶対評価値を図 4 左側のヒストグラムに⽰した(数値は施設番号)。さらに、参照品に定め
た MPXV_JPN2022_TK006 の値を元に相対的に算出した MPXV Zr-599、MPXV Liberia の核酸量
を図 4 右側のヒストグラムに⽰した。いずれの検体においても相対評価によりヒストグラムの横幅
が縮⼩し、施設間差の改善が認められ、参照品整備の有⽤性が⽰された。
4.
考察と課題
MPXV の核酸検査のための国内参照品の整備
本事業において、令和 5 年度は 2022 年に世界的で大流行した MPXV_JPN2022_TK006 株(クレード 2b)
の国内参照品、および、参照パネルとして MPXV Zr-599 株(クレード 1a)と MPXV Liberia 株(クレード 2a)
の計 3 種を整備した。Mpox の輸血感染リスクについては、(ⅰ) これまでに輸血による Mpox 感染事例の報
告はないこと、(ⅱ) ウイルス血症の持続期間については明らかになっておらず、血液からウイルス核酸が検
出される場合でも感染性を有するウイルスは分離されていないこと、(ⅲ) 日本では MSM の献血は出来ない
こと、(ⅳ) 新しいパートナーとの性的行為後 3 ヶ月の献血延期期間が設けられていること、(v) 海外から帰
国された方の 4 週間の献血延期措置が設定されていることなどを総合的に考慮すると、現在のところ輸血
による Mpox 感染のリスクは低いと考えられる。しかし、今後新たな株の出現等によりアウトブレイクが起こる
可能性はあり、感染症のアウトブレイクの際には、新型コロナウイルス感染症の時のように複数の施設で
PCR を実施することが考えられる。現在の技術レベルにおいて、アッセイごとに検出できる核酸量に大きな
差はないと考えられるが、測定キット等により、測定に必要な検体量、抽出量、PCR 反応に用いる検体量が
異なるため、採取検体中から検出できる最低ウイルス量も異なると考えられる。共同測定で算出した各施設
の核酸絶対量は、図 3 左のヒストグラムに示すように約 100 倍の開きがあるが、図 3 右のヒストグラムに示す
ように、国内参照品として定めた MPXV_JPN2022_TK006 を用いて相対的に MPXV Zr-599 と MPXV Liberia
の核酸量を算出すると、施設間差はハーフログ程度に縮小されることが認められた。このことから、国内参
照品を整備しておくことの有用性が改めて示唆され、血液の安全性の確保や公衆衛生の維持に有用であ
ると考えられた。今後は必要に応じて、国立感染症研究所への依頼により次世代生物学的製剤研究セン
ターから参照品を提供できるしくみを整えると共に、MPXV の国際標準品が出来た際には、再評価を実施
して IU/mL の核酸量を付与し、他国とも比較できるように準備する予定である。
5.
海外における血液安全に関する情報の収集および交換
WHO の血液製剤に関する各種会合に定期的に参加し、感染症リスクの早期察知および評価に基づく安
全対策の検討を行った。また、国立感染症研究所の病原体関連部署と連携し、情報の収集や交換を行っ
た。
6.
結論
本事業では、血液を介して感染し得る病原体に関する情報を継続して収集し、日本にリスクのある病原
体については必要に応じて核酸検査のための国内参照品を整備し、我が国での新興・再興感染症の流行
やアウトブレイクに備えた体制整備に貢献する。令和 5 年度は、MPXV の国内参照品を整備し、共同測定
により核酸量(U/mL)を付与した。いずれの施設で実施する核酸検査であっても国内外のキットを用いて検
出感度を比較できる体制が整った。今後も血液を介して感染する新たな病原体等について常に注視して
3