よむ、つかう、まなぶ。
薬-1令和7年度薬価改定に係る薬価算定基準の見直しについて(案) (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_48695.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第234回 1/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和7年度薬価改定については、令和6年度薬価改定において、同項の対象とされた品目のうち、その市場
実勢価格の薬価に対する乖離率が全ての既収載品の平均乖離率の 1.0 倍を超える後発品(令和6年 10
月以降に新規に薬価基準に収載された品目を除く。)を同項の対象とする。
3 組成、剤形区分及び規格が同一である既収載品群の価格帯の特例
(1)対象企業
別表 12 に基づきA区分と分類された企業
(2) (略)
(3)適用条件
以下の条件の全てを満たすこと。ただし、令和 7 年度薬価改定においては、イの「全ての既収載後発品の中
で最も高い価格帯となるものであること」とあるのは、「全ての既収載後発品(改定の対象範囲外の品目を含む。)
の中で最も高い価格帯となるものであること」と読み替える。
イ 全ての既収載後発品の中で最も高い価格帯となるものであること
ロ及びハ (略)
別表 12
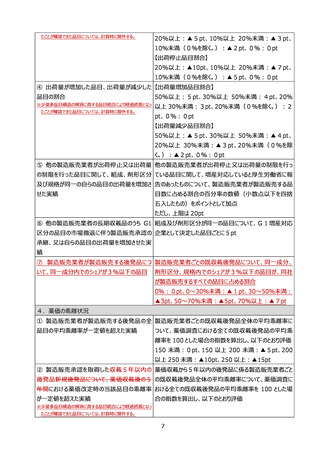
後発品を製造販売する企業の評価
1 評価指標及び評価方法
次の表の評価指標ごとに、右欄に掲げるポイントを合計したポイントを企業指標に基づくポイントとする。ただし、令和
6年度薬価改定においては、評価指標の1.及び2.の各項目並びに3.①の項目は適用しない。
評価指標
評価方法
1.後発品の安定供給に関連する情報の公表等
① 製造販売する品目の製造業者名の公表
「後発品の安定供給に関連する情報の公表等に関す
るガイドライン」の様式1について、製造業者名を記
載していない場合▲5pt
② 製造販売する品目の原薬の製造国の公表
「後発品の安定供給に関連する情報の公表等に関す
るガイドライン」の様式1について、原薬の製造国を
記載していない場合▲5pt
③ 他の製造販売業者と共同開発して承認され 「後発品の安定供給に関連する情報の公表等に関す
た品目における共同開発先の製造販売業者名 るガイドライン」の様式1について、共同開発先企業
の公表
④ 厚生労働省のウェブサイトの「安定供給体制
等を指標とした情報提供項目に関する情報提供
ページ」における安定供給体制等に関する情報の
掲載
⑤ 日本製薬団体連合会が作成した「ジェネリック
医薬品供給ガイドライン」に準拠した内容である
安定供給に係る文書の作成と運用
を記載していない場合▲5pt
厚生労働省のウェブサイトの「安定供給体制等を指
標とした情報提供項目に関する情報提供ページ」に
様式2を公表していない場合に▲10pt
厚生労働省のウェブサイトの「安定供給体制等を指
標とした情報提供項目に関する情報提供ページ」に
5
実勢価格の薬価に対する乖離率が全ての既収載品の平均乖離率の 1.0 倍を超える後発品(令和6年 10
月以降に新規に薬価基準に収載された品目を除く。)を同項の対象とする。
3 組成、剤形区分及び規格が同一である既収載品群の価格帯の特例
(1)対象企業
別表 12 に基づきA区分と分類された企業
(2) (略)
(3)適用条件
以下の条件の全てを満たすこと。ただし、令和 7 年度薬価改定においては、イの「全ての既収載後発品の中
で最も高い価格帯となるものであること」とあるのは、「全ての既収載後発品(改定の対象範囲外の品目を含む。)
の中で最も高い価格帯となるものであること」と読み替える。
イ 全ての既収載後発品の中で最も高い価格帯となるものであること
ロ及びハ (略)
別表 12
後発品を製造販売する企業の評価
1 評価指標及び評価方法
次の表の評価指標ごとに、右欄に掲げるポイントを合計したポイントを企業指標に基づくポイントとする。ただし、令和
6年度薬価改定においては、評価指標の1.及び2.の各項目並びに3.①の項目は適用しない。
評価指標
評価方法
1.後発品の安定供給に関連する情報の公表等
① 製造販売する品目の製造業者名の公表
「後発品の安定供給に関連する情報の公表等に関す
るガイドライン」の様式1について、製造業者名を記
載していない場合▲5pt
② 製造販売する品目の原薬の製造国の公表
「後発品の安定供給に関連する情報の公表等に関す
るガイドライン」の様式1について、原薬の製造国を
記載していない場合▲5pt
③ 他の製造販売業者と共同開発して承認され 「後発品の安定供給に関連する情報の公表等に関す
た品目における共同開発先の製造販売業者名 るガイドライン」の様式1について、共同開発先企業
の公表
④ 厚生労働省のウェブサイトの「安定供給体制
等を指標とした情報提供項目に関する情報提供
ページ」における安定供給体制等に関する情報の
掲載
⑤ 日本製薬団体連合会が作成した「ジェネリック
医薬品供給ガイドライン」に準拠した内容である
安定供給に係る文書の作成と運用
を記載していない場合▲5pt
厚生労働省のウェブサイトの「安定供給体制等を指
標とした情報提供項目に関する情報提供ページ」に
様式2を公表していない場合に▲10pt
厚生労働省のウェブサイトの「安定供給体制等を指
標とした情報提供項目に関する情報提供ページ」に
5