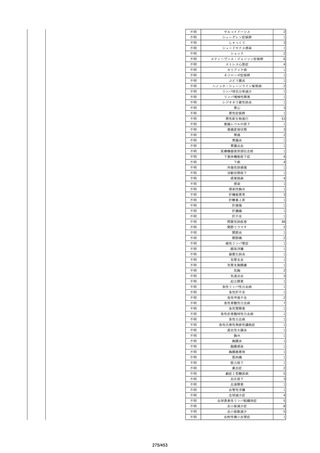
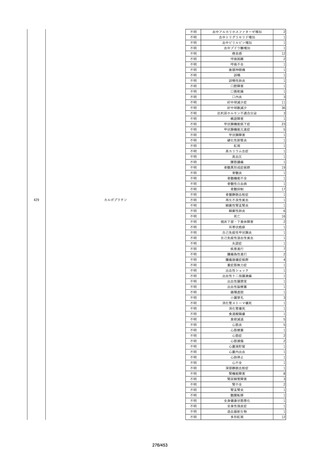
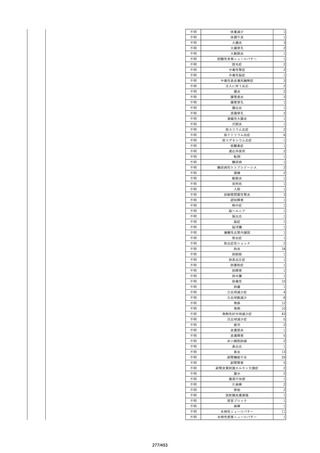
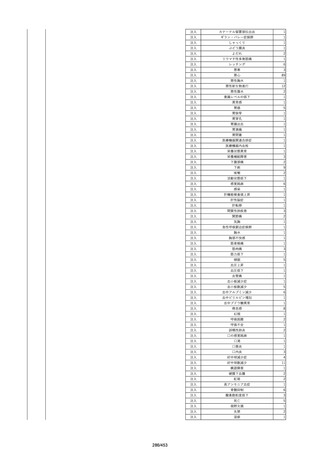
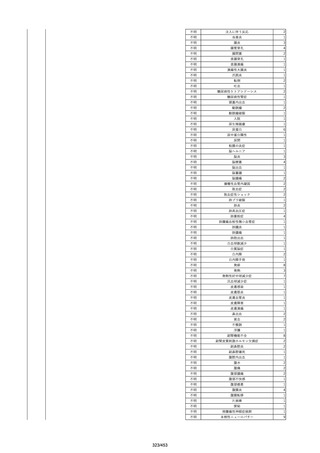
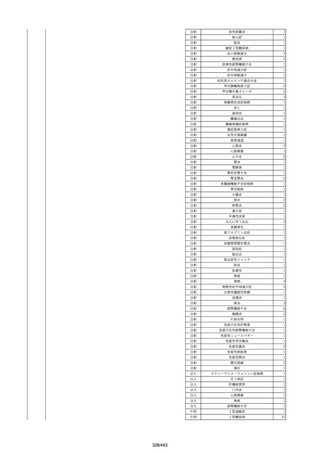
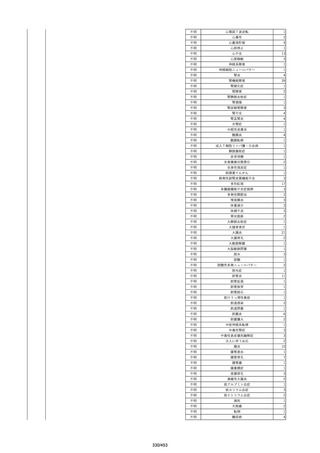
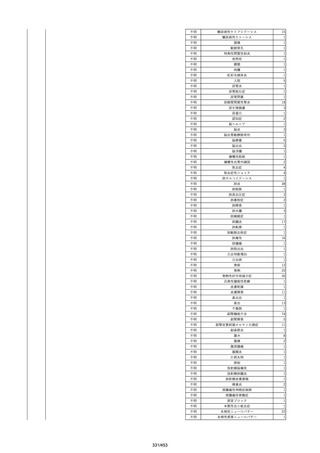
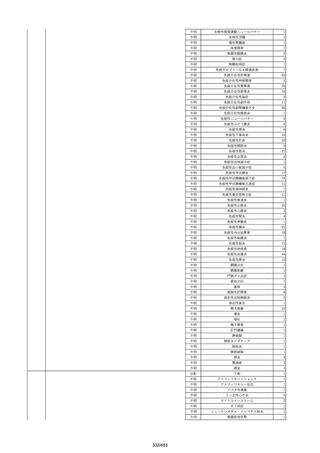
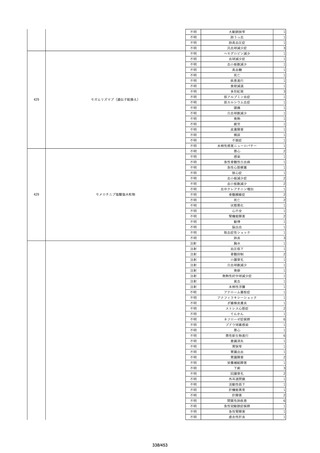
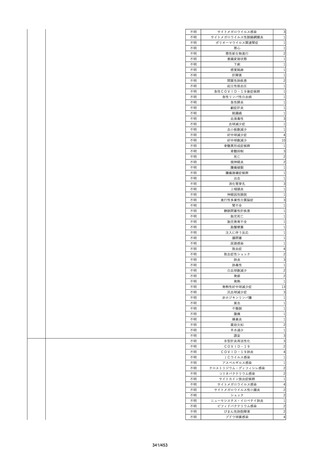
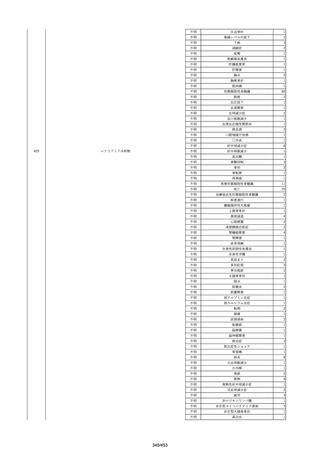
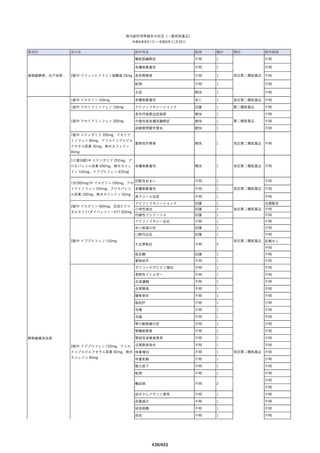
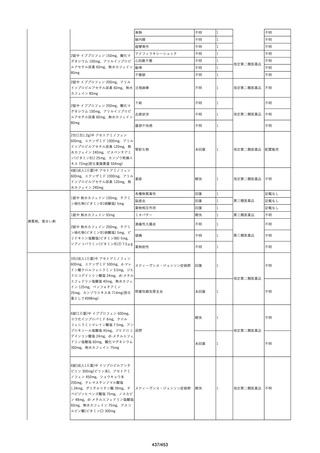
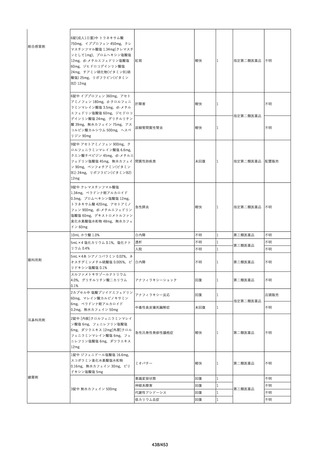
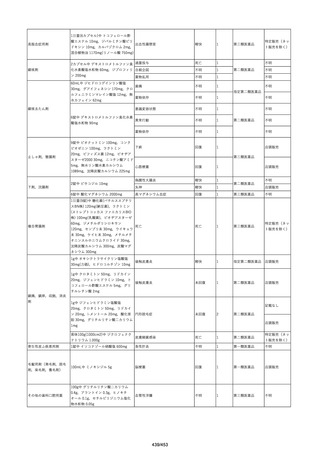
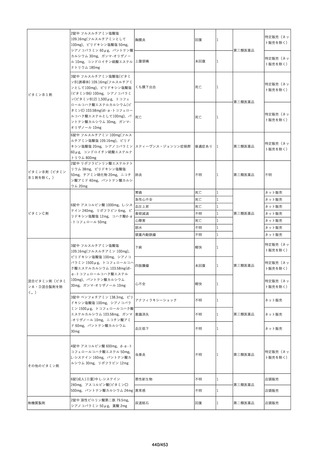
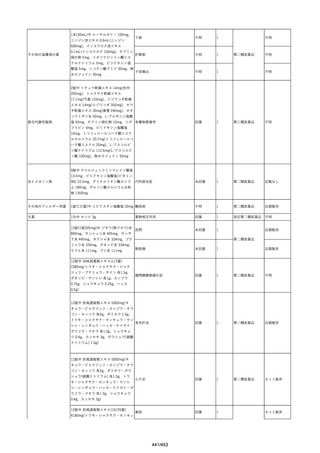
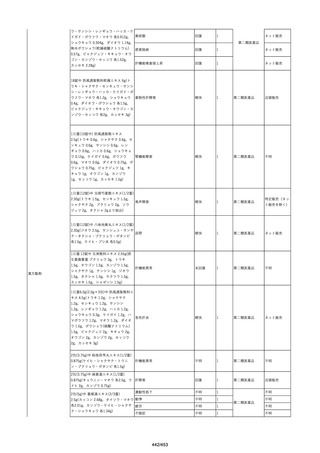
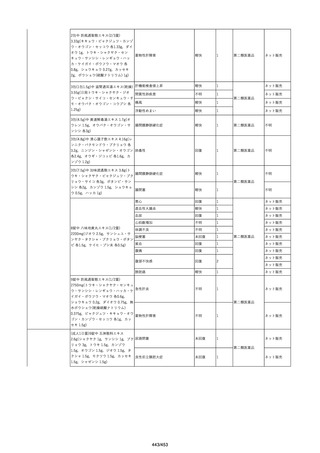
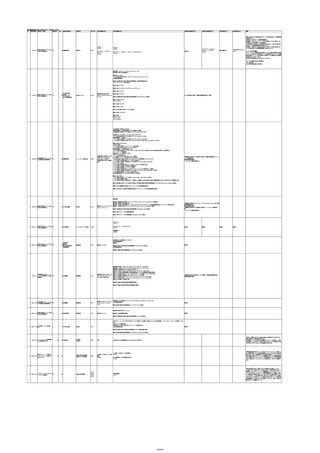
資料2-2 製造販売業者からの国内副作用等報告の状況[9.1MB] (454 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
No.
報告受領日 販売名(一般名)
患者性別
年代
原疾患(簡略名)
感染症名
投与年月
投与前検査(年月)
HBsAg(-)
(24/02)
1
2024/8/1
照射赤血球液-LR(人赤血
男
球液(放射線照射))
70 循環器疾患
B型肝炎
24/03
HBV-DNA(-)、HBsAb(-)、
HBcAb(-)
(24/03)
投与後検査(年月)
企業投与前検査(年月)
HBsAg(+)
(24/06)
(検体なし)
HBV-DNA(+)、HBsAg(+)、HBcAb(+)、IgM-HBcAb(+)
(24/07)
企業投与後検査(年月)
HBV-DNA(+)、HBsAg(-)、
HBsAb(-)、HBcAb(+)
(24/08)
受血者個別NAT
献血者個別NAT
備考
輸血に使用された血液の献血者1名は、その後の献血時にHBV関連検査
が陽性であった。
当該献血 2024年3月 HBV関連検査陰性
次回献血 2024年7月 スクリーニングNAT陽性(HBV-NAT 陰性)、HBs
抗原陰性、HBs抗体陽性、HBc抗体陽性
その他の輸血に使用された血液の献血者6名のうち、1名はその後に献
血があり、HBV関連検査結果に異常はなかった。
併用薬として報告された血液の献血者11名は全てその後に献血があり、
いずれの献血者もHBV関連検査結果に異常はなかった。
陽性(輸血後)
7名の個別NATはHBVDNA(-)
【ウイルス相同性確認】
スクリーニングNAT陽転献血時の検体(HBV-DNA 検査(9重測定)を実施
したところ、9回のうち1回で陽性となった)と患者検体中のウイルスの塩基
配列を検査したところ、両者は検査した範囲(PreS/S領域を含むP領域の
前半部940 bp)で全て一致した。
献血者株及び患者株のHBVはGenotype Cであった。
【HBV-DNA陽性献血者に係る情報】
・同一採血番号
1本の原料血漿を製造。使用済み。
輸血開始。BT 36.4℃、BP 149/81 mmHg、HR 71 /min。
輸血開始1時間7分後 輸血終了。
輸血翌日 BT 38.6℃。
バイタル測定5時間37分後 BT 40.2℃、BP 192/122 mmHg、HR 113 /min。
血液培養検査実施。
輸血2日後 輸血翌日実施の患者血液培養検査より酵母様真菌を検出。
ミカファンギンナトリウム投与開始。
輸血4日後 BT 38.4℃。
輸血5日後 BT 36.8℃、BP 126/78 mmHg、HR 89 /min。
輸血6日後 BT 36.7℃。
2
その他の疾患
糖尿病
60
その他の疾患
腎・泌尿器系疾患
照射赤血球液-LR(人赤血
2024/8/6
女
球液(放射線照射))
全身性カンジダ
24/08
輸血開始4時間52分前 BT
輸血8日後 BT 36.9℃。
36.9℃、BP 123/49 mmHg、HR
85 /min。
輸血9日後 輸血翌日実施の患者血液培養検査よりCandida albicans を検出。
同一採血番号の血漿にて細菌培養試験を実施し、陰性。
-
-
当該輸血用血液と同一採血番号の血漿にて細菌培養試験及びエンドト
キシン試験を実施。
細菌培養試験:陰性。
エンドトキシン試験:基準値以下。
-
当該輸血用血液のセグメントチューブにてKlebsiella oxytoca に対する細
菌培養試験を実施。
細菌培養試験:陰性。
当該輸血用血液と同一採血番号の血漿にてエンドトキシン試験を実
施。
エンドトキシン試験:基準値以下。
-
調査中
調査中
調査中
調査中
-
-
当該輸血用血液の使用済みバッグ内残渣にて細菌培養試験を実施。
細菌培養試験:陰性。
-
-
調査中
-
-
調査中
-
-
調査中
-
-
輸血11日後 BT 40.3℃。
夕方 BT 36.5℃。
輸血12日後 BT 36.5℃。
輸血13日後 BT 42℃。
輸血14日後-輸血18日後 BT 36.5℃を推移。
輸血19日後 夕方 39.2℃。
輸血20日後
朝方 BT 36.5℃。
正午 BT 38℃。
夕方 BT 36.5℃。
PC輸血開始1時間後 ECMO抜去。
胸部X線検査にて、肺野透過性低下あり(術直後より改善)。
PC輸血開始7時間後 BT 36℃台前半、BP 100 mmHg台、SpO2 98%。
輸血翌日 BT 37℃台前半、BP 120 mmHg台、SpO2 97%。
バイタル測定6時間後 BT 36℃台後半、BP 120 mmHg台、SpO2 98%。
胸部X線検査にて、著変なし。
バイタル測定12時間後 BT 37℃台後半、BP 120 mmHg台、SpO2 95%。
バイタル測定16時間後 血圧低下あり。BP 80 mmHg台。SvO2低下あり。SpO2 96%、SvO2 59%。
3
照射濃厚血小板-LR(人血
2024/9/24
男
小板濃厚液(放射線照射))
80 循環器疾患
シュードモナス性敗血症
24/08
PC輸血開始1時間前 BT 36℃
台後半、BP 100 mmHg台、
SpO2 99%(人工呼吸)。
PC輸血開始30分前 RBC輸血
施行。
輸血2日後 BP 80 mmHg台。
血圧低下持続。
バイタル測定1時間後 ノルアドレナリン5 mg投与開始。
バイタル測定3時間30分後 アドレナリン2 mg投与。
胸部X線検査にて、肺野透過性低下あり。
バイタル測定5時間後 BT 35℃台、BP 80 mmHg台、SpO2 94%。白血球数 1000台で重症感染症を疑う。血圧変動あり。
ベアーハガーにて保温開始。
炭酸水素ナトリウム静注20 mL投与。
BP 50 mmHg台まで低下。
バイタル測定7時間40分後 アドレナリン2 mg投与。
SvO2改善。アドレナリン投与開始するもECMO挿入。
ECMO挿入後から血圧は上昇したが、high PEEP下で1回換気量 150 mL以上入らず。
バイタル測定13時間後 造影CTにて、明らかな起因なし。
バイタル測定13時間後-14時間後 BT 36℃台後半、BP 120 mmHg台、SpO2 92%。
アドレナリン2 mg投与。
バイタル測定14時間後 塩化カリウム注投与。メロペネム水和物1 g投与。
バイタル測定16時間後-17時間後 心房細動あり。
バイタル測定18時間後 アドレナリン2 mg投与。
バイタル測定19時間後 高カリウム血症、アシドーシスにてCHDF再開するも、改善なし。
バイタル測定21時間後-22時間後 BT 37℃台前半、BP 80 mmHg台、SpO2 98%(人工呼吸)。
バイタル測定22時間後 メロペネム水和物1 g投与。
血液培養検査実施(バイタル測定10時間後、20時間後)。
輸血3日後 HR低下。
バイタル測定1時間後 BT 37℃台前半、BP 80 mmHg台、SpO2 96%(人工呼吸)。
バイタル測定3時間後 心停止。
バイタル測定12時間5分後 敗血症にて、患者死亡。剖検あり(所見:肺胞出血多量、腸管粘膜微小出血)。副作用と死亡との関連性不明。
輸血4日後 輸血2日後(バイタル測定10時間後、20時間後)実施の患者血液培養検査よりいずれもPseudomonas aeruginosa を検出。
輸血25日後 当該輸血用血液のセグメントチューブの血液培養検査実施。
輸血33日後 院内にて実施の当該輸血用血液のセグメントチューブの血液培養検査は陰性。
輸血開始。
4
2024/10/8
照射赤血球液-LR(人赤血
女
球液(放射線照射))
60 その他の腫瘍
敗血症
24/10
輸血前 BT 37.4℃、BP 134/77
mmHg、HR 79 /min。
輸血翌日 輸血開始4時間後 BT 36.7℃、BP 94/61 mmHg、HR 70 /min、SpO2 97%。輸血終了。
輸血終了6時間30分後 悪寒出現。
輸血終了7時間30分後 発熱あり。BT 38.5℃、BP 92/63 mmHg、HR 92 /min。血液培養検査実施。アセトアミノフェン静注液投与。
輸血終了14時間50分後 BT 37.1℃、BP 97/56 mmHg、HR 76 /min、SpO2 94%。解熱。
輸血2日後 輸血翌日実施の患者血液培養検査よりKlebsiella oxytoca を検出。
輸血3日後 CVカテーテル先培養検査実施。
輸血5日後 CVカテーテル先培養検査よりKlebsiella oxytoca を検出。
CMV-Ag(+)
(24/07)
5
2024/10/11
照射赤血球液-LR(人赤血
女
球液(放射線照射))
70 消化器疾患
サイトメガロウイルス感染
24/06
-
CMV-IgM-Ab(-)、CMV-IgG-Ab(+)
(24/07)
調査中
組織検査(+)
(24/09)
6
血液疾患
糖尿病
80
腎・泌尿器系疾患
循環器疾患
照射赤血球液-LR(人赤血
2024/10/15
男
球液(放射線照射))
輸血開始15分後 発熱あり。BT 38.6℃。
血液培養検査実施。
輸血終了。
細菌感染
24/10
輸血前 BT 37.2℃。
輸血翌日 輸血日実施の患者血液培養検査よりEscherichia coli を検出。
尿培養検査実施。
輸血翌日実施の患者尿培養検査よりEscherichia coli を検出。
7
照射濃厚血小板HLA-LR
2024/11/1 (人血小板濃厚液HLA(放射 男
線照射))
70 血液腫瘍
細菌感染
24/11
輸血開始3分後 BT 36.8℃、BP 142/61 mmHg、HR 65 /min、SpO2 98%。
輸血開始17分後 BT 36.9℃、BP 128/60 mmHg、HR 68 /min、SpO2 97%。
輸血開始1時間後 震えるような寒さあり。輸血中止。
輸血中止3分後 BT 36.2℃、BP 208/108 mmHg、HR 100 /min、SpO2 96%。
輸血中止15分後 血液培養検査、尿培養検査実施。セフェピム塩酸塩水和物投与開始。
輸血中止1時間30分後 BT 37.9℃、SpO2 90%。O2 1 L/min開始。ふらつき、息切れあり。
輸血開始2分前 BT 36.8℃、BP
輸血中止2時間後 症状軽快。SpO2 100%。O2 0.5 L/minに変更。
138/72 mmHg、HR 66 /min、
輸血中止3時間45分後 BT 36.7℃、BP 117/63 mmHg、HR 75 /min、SpO2 99%。
SpO2 96%。息切れあり。
輸血中止3時間50分後 BT 36.9℃、BP 120/55 mmHg、HR 75 /min、SpO2 99%。
輸血中止4時間後 HCU臨時入院。
輸血翌日 輸血日実施の患者尿培養検査は陰性。
輸血6日後 輸血日実施の患者血液培養検査は陰性。
8
照射濃厚血小板-LR(人血
2024/11/26
男
小板濃厚液(放射線照射))
70 血液腫瘍
細菌感染
24/11
輸血前 BT 36.8℃、BP 121/81
mmHg、HR 84 /min、SpO2
97%。
輸血開始15分後 発熱あり。BT 37.5℃、BP 126/82 mmHg、HR 80 /min、SpO2 97%。
血液培養検査実施。
輸血日実施の患者血液培養検査よりコリネバクテリウムを検出。
輸血開始4時間35分後 BT 38.7℃。
9
2024/11/26
照射赤血球液-LR(人赤血
女
球液(放射線照射))
80 呼吸器疾患
真菌感染
24/11
輸血前 BT 37.5℃。
輸血翌日 血液培養検査実施。
輸血3日後 輸血翌日実施の患者血液培養検査よりカンジダを検出。
10
2024/11/29
赤血球液-LR(人赤血球
液)
女
0 その他の疾患
菌血症
24/11
-
院内のクリーンベンチ内でRBC1単位の元バッグに輸血セットを接続し、輸血セットと三方活栓を接続し、そこにスクリュー式シリンジを接続し、五分
割。
分割した2バッグ輸血施行。
敗血症性ショックあり。活気不良、アシドーシス、血球減少あり。
血液培養検査実施。
輸血翌日 輸血日実施の患者血液培養検査よりグラム陽性球菌を検出。
輸血日実施の患者血液培養検査よりStaphylococcus epidermidis を検出。
11
12
13
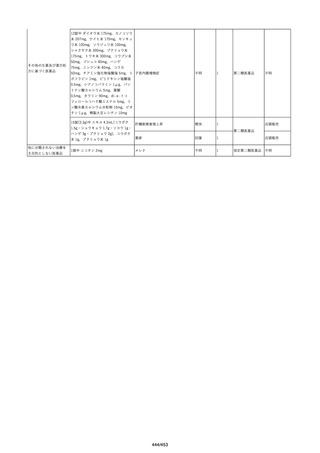
2024/10/2
コンコエイト-HT(乾燥濃縮
人血液凝固第8因子)
献血グロベニン-I(乾燥ポリ
2024/10/25 エチレングリコール処理人免
疫グロブリン)
アブラキサン(パクリタキセル
2024/11/29
男
(アルブミン懸濁型))
男
女
60 血液疾患
40 -
60 -
HIV感染
C型肝炎
B型肝炎表面抗原陽性
B型肝炎コア抗体陽性
B型肝炎抗原陽性
不明
不明
不明
HBs抗原、HBs抗体、 HBc抗体陰性。
HBs抗原、HBs抗体、 HBc抗体 (23/02)
陰性。
(不明)
HBs抗原陽性、HBc抗体陽性を認める。
(24/09)
21/1222/05
24/0224/10
-
血友病Aに対する血液製剤投与によりHIV及びHCVに感染した。
-
-
B型抗原陽性。
(24/10)
-
453/453
-
-
-
-
-
-
-
文献からの情報。投与された製剤は過去の血液製剤であると考えられ、
現在の製剤による感染症報告ではない。
使用薬剤についての自他社等の確認を行ったところ、担当医より、「使用
が相当前のことであるのと、当院での使用ではないため、医薬品名に関し
ては不明。」とのことであった。使用製剤は不明である。
-
当該製品は製造工程でエタノール分画、ポリエチレングリコール処理、イ
オン交換体処理、ウイルス除去膜処理によりウイルスの不活化や除去処
理が行われており、医薬発第1047号 血漿分画製剤のウイルスに対する
安全性確保に関するガイドライン、医薬審第329号 ヒト又は動物細胞株を
用いて製造されるバイオテクノロジー応用医薬品のウイルス安全性評価
に従い評価されたウイルスクリアランス指数は9以上であることを確認して
いる。
本剤の添加物である人血清アルブミンの原料となる血漿については、
HBs抗原、抗HCV抗体、抗HIV-1抗体及び抗HIV-2抗体が陰性であること
を確認している。さらに、プールした試験血漿については、HBV-DNA、
HCV-RNA及びHIV-1-RNAについて核酸増幅検査(NAT)を実施し、適合
した血漿を本剤の製造に使用しているが、当該NATの検出限界以下のウ
イルスが混入している可能性が常に存在する。人血清アルブミンの製造
工程である、Cohn低温エタノール分画法及び60±0.5℃ 10~11時間の液
状加熱処理は、HIVをはじめとする各種ウイルスに対し、除去・不活化効
果を有することが確認されている。