よむ、つかう、まなぶ。
○新規技術(11月受理分)の先進医療A又は先進医療Bへの振り分けについて(案)別紙3 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00016.html |
| 出典情報 | 先進医療会議(第81回 7/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
レ
当該医薬品・医療機器・再生医療等製品について、薬事承認の申請時及び
取得時において、申請企業から情報提供がなされることとなっている。
注1)医薬品医療機器法承認又は認証上の使用目的、効能及び効果を記入すること。
注2)医薬品医療機器法において適応外使用に該当する場合は「適応外」、医薬品医療機器法で承認された適
応の範囲内の使用の場合は「適応内」と記載すること。
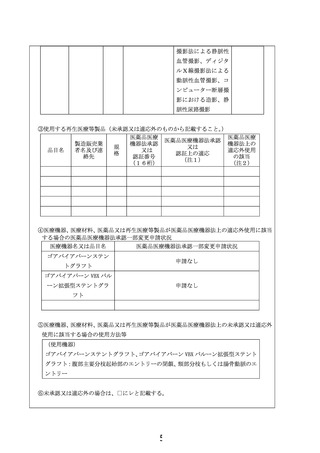
2-2.海外での承認に関する情報
米国での薬事承認の状況
腸骨動脈と浅大腿動脈における血流改善、
及び人工血管内シャントの吻合部狭窄・閉塞への適応。
保険適用に関しては、
「手技に対する対価」となり「デバイス毎への保険適用」とはならない。
欧州での薬事承認の状況
末梢動脈と末梢静脈の血流改善が適応となる(幅広い適応)。保険適用は、欧州各国ごとに異な
る。例えば、米国同様、ドイツでも実施手技に対して保険が適応されるが、デバイスそのものに
対して保険収載されているわけではない。
6
当該医薬品・医療機器・再生医療等製品について、薬事承認の申請時及び
取得時において、申請企業から情報提供がなされることとなっている。
注1)医薬品医療機器法承認又は認証上の使用目的、効能及び効果を記入すること。
注2)医薬品医療機器法において適応外使用に該当する場合は「適応外」、医薬品医療機器法で承認された適
応の範囲内の使用の場合は「適応内」と記載すること。
2-2.海外での承認に関する情報
米国での薬事承認の状況
腸骨動脈と浅大腿動脈における血流改善、
及び人工血管内シャントの吻合部狭窄・閉塞への適応。
保険適用に関しては、
「手技に対する対価」となり「デバイス毎への保険適用」とはならない。
欧州での薬事承認の状況
末梢動脈と末梢静脈の血流改善が適応となる(幅広い適応)。保険適用は、欧州各国ごとに異な
る。例えば、米国同様、ドイツでも実施手技に対して保険が適応されるが、デバイスそのものに
対して保険収載されているわけではない。
6