よむ、つかう、まなぶ。
オミクロン株対応ワクチンの効能・効果、用法・用量の一部変更承認について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27929.html |
| 出典情報 | オミクロン株対応ワクチンの効能・効果、用法・用量の一部変更承認について(9/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
表2 本剤接種群のコミナティ筋注(起源株)接種群に対するSARS-CoV-2オミ
た。その他の全身性の事象は接種翌日(中央値)に発現し、持続期間は1日(中
央値)であった5)。
クロン株BA.1血清中和抗体応答率の差
本剤接種群
測定例数
コミナティ筋注(起源株)接種群
na)(抗体応答率[%]
)
[両側95%信頼区間] 測定例数
(接種後1ヵ月)
表5 主な副反応の発現状況
差(%)
na)(抗体応答率[%]
)[両側95%信頼区
[両側95%信頼区間]
間]b)
(接種後1ヵ月)
発現例数(発現割合[%])
コミナティ筋注(起源株)接種群
プラセボ接種群
接種
回数
評価
例数a)
1
4093
3186(77.8) 28(0.7)
4090
488(11.9)
2(0.0)
2
3758
2730(72.6) 33(0.9)
3749
372(9.9)
0(-)
1
4093
1700(41.5) 35(0.9)
4090
2
3758
2086(55.5) 143(3.8)
3749
756(20.2) 16(0.4)
1
4093
1413(34.5) 25(0.6)
4090
1100(26.9) 22(0.5)
びGrade 3以上)は表3のとおりであった。注射部位疼痛は接種翌日(中央値)
2
3758
1732(46.1) 76(2.0)
3749
735(19.6) 19(0.5)
に発現し、持続期間は2日(中央値)であった。その他の全身性の事象は接
1
4093
738(18.0) 14(0.3)
4090
398(9.7)
5(0.1)
2
3758
1260(33.5) 63(1.7)
3749
260(6.9)
4(0.1)
1
4093
9(0.2)
4090
203(5.0)
3(0.1)
2
3758
1114(29.6) 62(1.6)
3749
125(3.3)
0(-)
1
4093
406(9.9)
7(0.2)
4090
247(6.0)
1(0.0)
2
3758
772(20.5) 27(0.7)
3749
170(4.5)
5(0.1)
1
4093
111(2.7)
8(0.2)
4090
27(0.7)
7(0.2)
2
3758
512(13.6) 32(0.9)
3749
14(0.4)
3(0.1)
121(71.6)
[64.2, 78.3]
169
149
85(57.0)
[48.7, 65.1]
14.6
[4.0, 24.9]
注射部位疼
痛
a)抗体価が本剤接種前(SARS-CoV-2ワクチンとして4回目接種前)のベースライン値(ベー
スライン値が定量下限(LLOQ)未満の場合はLLOQ値)から4倍以上上昇した治験参加者数
b)非劣性マージン:抗体応答率の差(本剤-コミナティ筋注(起源株))の両側95%信頼区
間下限>-5%
疲労
305例を対象に本剤接種後の安全性を評価した。治験薬接種後7日間、電子日
誌により副反応の発現状況を評価した。主な副反応の発現状況(事象全体及
頭痛
筋肉痛
3)
種翌日(中央値)に発現し、持続期間は1~2日(中央値)であった 。
表3 主な副反応の発現状況
悪寒
発現例数(発現割合[%]
)
本剤接種群
コミナティ筋注(起源株)接種群
接種
回数a)
評価
例数b)
注射部位疼痛
1
301
175(58.1) 1(0.3)
298
179(60.1) 1(0.3)
疲労
1
301
148(49.2) 5(1.7)
298
135(45.3) 1(0.3)
事象全体
Grade 3
以上c)
評価
例数b)
事象全体
関節痛
Grade 3
以上c)
発熱
c)
事象全体
Grade 3
以上b)
434(10.6)
評価
例数a)
事象全体
Grade 3
以上b)
1172(28.7) 14(0.3)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
頭痛
1
301
101(33.6) 1(0.3)
298
79(26.5)
1(0.3)
筋肉痛
1
301
67(22.3)
0(―)
298
59(19.8)
0(―)
悪寒
1
301
39(13.0)
0(―)
298
49(16.4)
0(―)
関節痛
1
301
34(11.3)
0(―)
298
27(9.1)
0(―)
注(起源株)接種群:1005例、プラセボ接種群:978例)を対象に「SARS-CoV-2
発熱d)
1
301
15(5.0)
4(1.3)
298
11(3.7)
0(―)
感染歴がない参加者での2回目接種後7日以降のSARS-CoV-2による感染症に
(2)12~15歳の参加者
12~15歳の参加者における有効性を追加で評価した。1983例(コミナティ筋
a)SARS-CoV-2ワクチンとして4回目接種
b)電子日誌により評価した例数
c)重症度が「高度(日常活動を妨げる)」以上として報告された事象
d)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
対するコミナティ筋注(起源株)の有効性[ワクチン有効性1(VE1)]」を、
2229例(コミナティ筋注(起源株)接種群:1119例、プラセボ接種群:1110例)
を対象に「SARS-CoV-2感染歴の有無を問わない参加者での2回目接種後7日
以降のSARS-CoV-2による感染症に対するコミナティ筋注(起源株)の有効
17.1.2 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート(参考:
性(VE2)」を評価した。解析結果は表6のとおりであった。
コミナティ筋注(起源株))
表6 SARS-CoV-2による感染症に対する有効性
SARS-CoV-2ワクチン未接種の12歳以上の健康な参加者を対象に、コミナ
ティ筋注(起源株)30µgを19~23日間隔で2回接種したときの有効性及び安
解析対象例数
SARS-CoV-2
による感染症
確定例数
コミナティ筋 注
(起源株)接種群
1005
0
プラセボ接種群
978
16
コミナティ筋 注
(起源株)接種群
1119
0
プラセボ接種群
1110
18
全性を検討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。さらに、本試験でコミナティ筋注(起源株)30µgを2回接種済み
の18~55歳の参加者にコミナティ筋注(起源株)30µgを1回接種したときの
VE1a)
免疫原性及び安全性も検討した。
(1)16歳以上の参加者
36523例(コミナティ筋注(起源株)接種群:18198例、プラセボ接種群:
VE2a)
18325例)を対象に、1つ目の主要有効性評価項目である「SARS-CoV-2感染
歴がない参加者での2回目接種後7日以降のSARS-CoV-2による感染症に対す
ワクチン有効性
[95%信頼区間](%)
100.0[75.3, 100.0]
100.0[78.1, 100.0]
a)VE1及びVE2の2回目接種後の追跡期間(中央値)はいずれも62日であった。また、VE1
及びVE2の解析には接種間隔19~38日間の参加者が含まれ、その内訳はVE1とVE2でそれ
ぞれ19~23日間の参加者は95.9%(1902例)と95.8%(2136例)
、24~38日間の参加者は4.1%
(81例)と4.2%(93例)であった
るコミナティ筋注(起源株)の有効性[ワクチン有効性1(VE1)
]」を評価し
た。40137例(コミナティ筋注(起源株)接種群:19965例、プラセボ接種群:
20172例)を対象に、2つ目の主要有効性評価項目である「SARS-CoV-2感染
歴の有無を問わない参加者での2回目接種後7日以降のSARS-CoV-2による感
2つの年齢群から無作為に抽出したSARS-CoV-2感染歴がない360例(12~15
染症に対するコミナティ筋注(起源株)の有効性(VE2)」を評価した。解析
歳群:190例、16~25歳群:170例)を対象に、副次免疫原性評価項目としてコ
結果は表4のとおりであった4)。
ミナティ筋注(起源株)2回目接種後1ヵ月のSARS-CoV-2血清中和抗体価を評
価した結果、表7のとおり12~15歳群の16~25歳群に対する非劣性が示された。
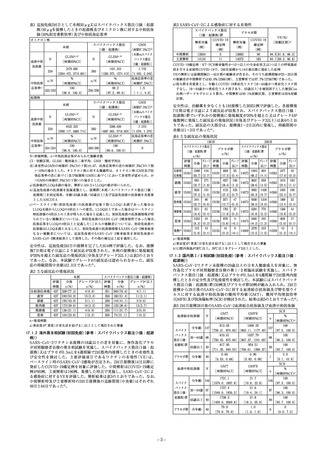
表4 SARS-CoV-2による感染症に対する有効性
解析対象例数
SARS-CoV-2
による感染症
確定例数
VE1a)
コミナティ筋 注
(起源株)接種群
18198
8
プラセボ接種群
18325
162
VE2a)
コミナティ筋 注
(起源株)接種群
19965
9
プラセボ接種群
20172
169
表7 12~15歳群の16~25歳群に対するSARS-CoV-2血清中和抗体価(50%中和
ワクチン有効性
[95%信用区間](%)
抗体価)の幾何平均比
12~15歳群
95.0[90.3, 97.6]
94.6[89.9, 97.3]
16~25歳群
測定例数
GMT[両側95%
信頼区間]a)
(2回目接種後1ヵ月)
測定例数
190
1239.5
[1095.5, 1402.5]
170
GMR[両側95%
GMT[両側95%
信頼区間]b)
信頼区間]a)
(2回目接種後1ヵ月)
705.1
[621.4, 800.2]
1.76
[1.47, 2.10]
GMR:幾何平均比、GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)非劣性マージン:GMR(12~15歳/16~25歳)の両側95%信頼区間下限>0.67
a)VE1及びVE2の2回目接種後の追跡期間(中央値)はそれぞれ57日と55日であった。また、
VE1及びVE2の解析には接種間隔19~42日間の参加者が含まれ、その内訳はVE1とVE2で
それぞれ19~23日間の参加者は96.5%(35248例)と96.3%(38665例)
、24~42日間の参
加者は3.5%(1275例)と3.7%(1472例)であった5)
12~15歳の2260例(コミナティ筋注(起源株)接種群:1131例、プラセボ接
種群:1129例)を対象にコミナティ筋注(起源株)接種後の安全性を評価した。
16歳以上の43448例(コミナティ筋注(起源株)接種群:21720例、プラセボ
治験薬接種後7日間、電子日誌により副反応の発現状況を評価した。主な副
接種群:21728例)を対象にコミナティ筋注(起源株)接種後の安全性を評
反応の発現状況(事象全体及びGrade 3以上)は表8のとおりであった。注射
価した。一部の参加者(解析対象例数:1回目接種後8183例、2回目接種後
部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)であった。
7507例)で治験薬接種後7日間、電子日誌により副反応の発現状況を評価した。
その他の全身性の事象は2~3日(中央値)に発現し、持続期間は1~2日(中
主な副反応の発現状況(事象全体及びGrade 3以上)は表5のとおりであった4)。
央値)であった5)。
注射部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)であっ
3
た。その他の全身性の事象は接種翌日(中央値)に発現し、持続期間は1日(中
央値)であった5)。
クロン株BA.1血清中和抗体応答率の差
本剤接種群
測定例数
コミナティ筋注(起源株)接種群
na)(抗体応答率[%]
)
[両側95%信頼区間] 測定例数
(接種後1ヵ月)
表5 主な副反応の発現状況
差(%)
na)(抗体応答率[%]
)[両側95%信頼区
[両側95%信頼区間]
間]b)
(接種後1ヵ月)
発現例数(発現割合[%])
コミナティ筋注(起源株)接種群
プラセボ接種群
接種
回数
評価
例数a)
1
4093
3186(77.8) 28(0.7)
4090
488(11.9)
2(0.0)
2
3758
2730(72.6) 33(0.9)
3749
372(9.9)
0(-)
1
4093
1700(41.5) 35(0.9)
4090
2
3758
2086(55.5) 143(3.8)
3749
756(20.2) 16(0.4)
1
4093
1413(34.5) 25(0.6)
4090
1100(26.9) 22(0.5)
びGrade 3以上)は表3のとおりであった。注射部位疼痛は接種翌日(中央値)
2
3758
1732(46.1) 76(2.0)
3749
735(19.6) 19(0.5)
に発現し、持続期間は2日(中央値)であった。その他の全身性の事象は接
1
4093
738(18.0) 14(0.3)
4090
398(9.7)
5(0.1)
2
3758
1260(33.5) 63(1.7)
3749
260(6.9)
4(0.1)
1
4093
9(0.2)
4090
203(5.0)
3(0.1)
2
3758
1114(29.6) 62(1.6)
3749
125(3.3)
0(-)
1
4093
406(9.9)
7(0.2)
4090
247(6.0)
1(0.0)
2
3758
772(20.5) 27(0.7)
3749
170(4.5)
5(0.1)
1
4093
111(2.7)
8(0.2)
4090
27(0.7)
7(0.2)
2
3758
512(13.6) 32(0.9)
3749
14(0.4)
3(0.1)
121(71.6)
[64.2, 78.3]
169
149
85(57.0)
[48.7, 65.1]
14.6
[4.0, 24.9]
注射部位疼
痛
a)抗体価が本剤接種前(SARS-CoV-2ワクチンとして4回目接種前)のベースライン値(ベー
スライン値が定量下限(LLOQ)未満の場合はLLOQ値)から4倍以上上昇した治験参加者数
b)非劣性マージン:抗体応答率の差(本剤-コミナティ筋注(起源株))の両側95%信頼区
間下限>-5%
疲労
305例を対象に本剤接種後の安全性を評価した。治験薬接種後7日間、電子日
誌により副反応の発現状況を評価した。主な副反応の発現状況(事象全体及
頭痛
筋肉痛
3)
種翌日(中央値)に発現し、持続期間は1~2日(中央値)であった 。
表3 主な副反応の発現状況
悪寒
発現例数(発現割合[%]
)
本剤接種群
コミナティ筋注(起源株)接種群
接種
回数a)
評価
例数b)
注射部位疼痛
1
301
175(58.1) 1(0.3)
298
179(60.1) 1(0.3)
疲労
1
301
148(49.2) 5(1.7)
298
135(45.3) 1(0.3)
事象全体
Grade 3
以上c)
評価
例数b)
事象全体
関節痛
Grade 3
以上c)
発熱
c)
事象全体
Grade 3
以上b)
434(10.6)
評価
例数a)
事象全体
Grade 3
以上b)
1172(28.7) 14(0.3)
a)電子日誌により評価した例数
b)重症度が「高度(日常活動を妨げる)」以上として報告された事象
c)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
頭痛
1
301
101(33.6) 1(0.3)
298
79(26.5)
1(0.3)
筋肉痛
1
301
67(22.3)
0(―)
298
59(19.8)
0(―)
悪寒
1
301
39(13.0)
0(―)
298
49(16.4)
0(―)
関節痛
1
301
34(11.3)
0(―)
298
27(9.1)
0(―)
注(起源株)接種群:1005例、プラセボ接種群:978例)を対象に「SARS-CoV-2
発熱d)
1
301
15(5.0)
4(1.3)
298
11(3.7)
0(―)
感染歴がない参加者での2回目接種後7日以降のSARS-CoV-2による感染症に
(2)12~15歳の参加者
12~15歳の参加者における有効性を追加で評価した。1983例(コミナティ筋
a)SARS-CoV-2ワクチンとして4回目接種
b)電子日誌により評価した例数
c)重症度が「高度(日常活動を妨げる)」以上として報告された事象
d)38.0℃以上。38.9℃を超えた場合に、重症度が高度(Grade 3)以上とした
対するコミナティ筋注(起源株)の有効性[ワクチン有効性1(VE1)]」を、
2229例(コミナティ筋注(起源株)接種群:1119例、プラセボ接種群:1110例)
を対象に「SARS-CoV-2感染歴の有無を問わない参加者での2回目接種後7日
以降のSARS-CoV-2による感染症に対するコミナティ筋注(起源株)の有効
17.1.2 海外第Ⅰ/Ⅱ/Ⅲ相試験(C4591001試験)第Ⅱ/Ⅲ相パート(参考:
性(VE2)」を評価した。解析結果は表6のとおりであった。
コミナティ筋注(起源株))
表6 SARS-CoV-2による感染症に対する有効性
SARS-CoV-2ワクチン未接種の12歳以上の健康な参加者を対象に、コミナ
ティ筋注(起源株)30µgを19~23日間隔で2回接種したときの有効性及び安
解析対象例数
SARS-CoV-2
による感染症
確定例数
コミナティ筋 注
(起源株)接種群
1005
0
プラセボ接種群
978
16
コミナティ筋 注
(起源株)接種群
1119
0
プラセボ接種群
1110
18
全性を検討することを目的として、プラセボ対照無作為化多施設共同試験を
実施した。さらに、本試験でコミナティ筋注(起源株)30µgを2回接種済み
の18~55歳の参加者にコミナティ筋注(起源株)30µgを1回接種したときの
VE1a)
免疫原性及び安全性も検討した。
(1)16歳以上の参加者
36523例(コミナティ筋注(起源株)接種群:18198例、プラセボ接種群:
VE2a)
18325例)を対象に、1つ目の主要有効性評価項目である「SARS-CoV-2感染
歴がない参加者での2回目接種後7日以降のSARS-CoV-2による感染症に対す
ワクチン有効性
[95%信頼区間](%)
100.0[75.3, 100.0]
100.0[78.1, 100.0]
a)VE1及びVE2の2回目接種後の追跡期間(中央値)はいずれも62日であった。また、VE1
及びVE2の解析には接種間隔19~38日間の参加者が含まれ、その内訳はVE1とVE2でそれ
ぞれ19~23日間の参加者は95.9%(1902例)と95.8%(2136例)
、24~38日間の参加者は4.1%
(81例)と4.2%(93例)であった
るコミナティ筋注(起源株)の有効性[ワクチン有効性1(VE1)
]」を評価し
た。40137例(コミナティ筋注(起源株)接種群:19965例、プラセボ接種群:
20172例)を対象に、2つ目の主要有効性評価項目である「SARS-CoV-2感染
歴の有無を問わない参加者での2回目接種後7日以降のSARS-CoV-2による感
2つの年齢群から無作為に抽出したSARS-CoV-2感染歴がない360例(12~15
染症に対するコミナティ筋注(起源株)の有効性(VE2)」を評価した。解析
歳群:190例、16~25歳群:170例)を対象に、副次免疫原性評価項目としてコ
結果は表4のとおりであった4)。
ミナティ筋注(起源株)2回目接種後1ヵ月のSARS-CoV-2血清中和抗体価を評
価した結果、表7のとおり12~15歳群の16~25歳群に対する非劣性が示された。
表4 SARS-CoV-2による感染症に対する有効性
解析対象例数
SARS-CoV-2
による感染症
確定例数
VE1a)
コミナティ筋 注
(起源株)接種群
18198
8
プラセボ接種群
18325
162
VE2a)
コミナティ筋 注
(起源株)接種群
19965
9
プラセボ接種群
20172
169
表7 12~15歳群の16~25歳群に対するSARS-CoV-2血清中和抗体価(50%中和
ワクチン有効性
[95%信用区間](%)
抗体価)の幾何平均比
12~15歳群
95.0[90.3, 97.6]
94.6[89.9, 97.3]
16~25歳群
測定例数
GMT[両側95%
信頼区間]a)
(2回目接種後1ヵ月)
測定例数
190
1239.5
[1095.5, 1402.5]
170
GMR[両側95%
GMT[両側95%
信頼区間]b)
信頼区間]a)
(2回目接種後1ヵ月)
705.1
[621.4, 800.2]
1.76
[1.47, 2.10]
GMR:幾何平均比、GMT:幾何平均抗体価
a)抗体価が定量下限(LLOQ)未満の場合、解析には0.5×LLOQの値が用いられた
b)非劣性マージン:GMR(12~15歳/16~25歳)の両側95%信頼区間下限>0.67
a)VE1及びVE2の2回目接種後の追跡期間(中央値)はそれぞれ57日と55日であった。また、
VE1及びVE2の解析には接種間隔19~42日間の参加者が含まれ、その内訳はVE1とVE2で
それぞれ19~23日間の参加者は96.5%(35248例)と96.3%(38665例)
、24~42日間の参
加者は3.5%(1275例)と3.7%(1472例)であった5)
12~15歳の2260例(コミナティ筋注(起源株)接種群:1131例、プラセボ接
種群:1129例)を対象にコミナティ筋注(起源株)接種後の安全性を評価した。
16歳以上の43448例(コミナティ筋注(起源株)接種群:21720例、プラセボ
治験薬接種後7日間、電子日誌により副反応の発現状況を評価した。主な副
接種群:21728例)を対象にコミナティ筋注(起源株)接種後の安全性を評
反応の発現状況(事象全体及びGrade 3以上)は表8のとおりであった。注射
価した。一部の参加者(解析対象例数:1回目接種後8183例、2回目接種後
部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)であった。
7507例)で治験薬接種後7日間、電子日誌により副反応の発現状況を評価した。
その他の全身性の事象は2~3日(中央値)に発現し、持続期間は1~2日(中
主な副反応の発現状況(事象全体及びGrade 3以上)は表5のとおりであった4)。
央値)であった5)。
注射部位疼痛は接種当日(中央値)に発現し、持続期間は2日(中央値)であっ
3