よむ、つかう、まなぶ。
資料4-6 企業から提出された開発工程表の概要等(第IV回要望) (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00025.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第53回 12/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
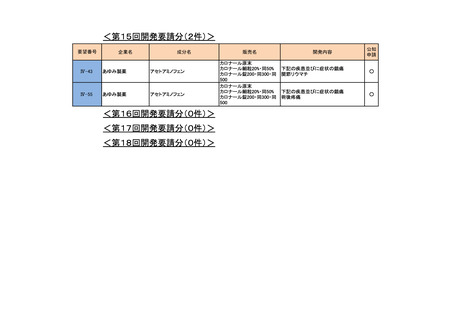
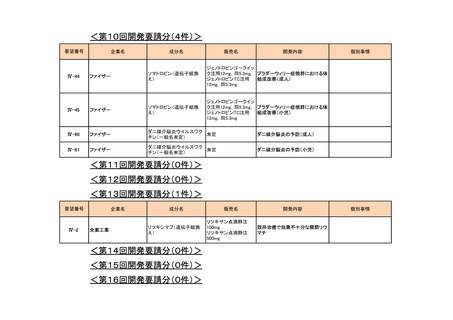
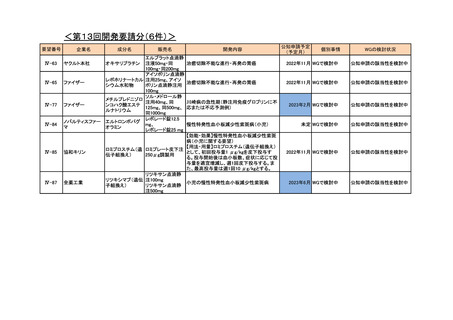
<第13回開発要請分(6件)>
要望番号
Ⅳ-63
Ⅳ-65
Ⅳ-77
Ⅳ-84
企業名
成分名
販売名
エルプラット点滴静
注液50mg・同
100mg・同200mg
アイソボリン点滴静
レボホリナートカル 注用25mg、アイソ
ファイザー
シウム水和物
ボリン点滴静注用
100mg
ソル・メドロール静
メチルプレドニゾロ
注用40mg、同
ファイザー
ンコハク酸エステ
125mg、同500mg、
ルナトリウム
同1000mg
レボレード錠12.5
ノバルティスファー エルトロンボパグ
mg、
マ
オラミン
レボレード錠25 mg
ヤクルト本社
Ⅳ-85
協和キリン
Ⅳ-87
全薬工業
オキサリプラチン
開発内容
公知申請予定
(予定月)
個別事情
WGの検討状況
治癒切除不能な進行・再発の胃癌
2022年11月 WGで検討中
公知申請の該当性を検討中
治癒切除不能な進行・再発の胃癌
2022年11月 WGで検討中
公知申請の該当性を検討中
2023年2月 WGで検討中
公知申請の該当性を検討中
未定 WGで検討中
公知申請の該当性を検討中
2022年11月 WGで検討中
公知申請の該当性を検討中
2023年6月 WGで検討中
公知申請の該当性を検討中
川崎病の急性期(静注用免疫グロブリンに不
応または不応予測例)
慢性特発性血小板減少性紫斑病(小児)
【効能・効果】慢性特発性血小板減少性紫斑
病(小児に関する要望)
【用法・用量】ロミプロスチム(遺伝子組換え)
ロミプロスチム(遺 ロミプレート皮下注
として、初回投与量1 μg/kgを皮下投与す
伝子組換え)
250μg調製用
る。投与開始後は血小板数、症状に応じて投
与量を適宜増減し、週1回皮下投与する。ま
た、最高投与量は週1回10 μg/kgとする。
リツキサン点滴静
リツキシマブ(遺伝 注100mg
小児の慢性特発性血小板減少性紫斑病
子組換え)
リツキサン点滴静
注500mg
要望番号
Ⅳ-63
Ⅳ-65
Ⅳ-77
Ⅳ-84
企業名
成分名
販売名
エルプラット点滴静
注液50mg・同
100mg・同200mg
アイソボリン点滴静
レボホリナートカル 注用25mg、アイソ
ファイザー
シウム水和物
ボリン点滴静注用
100mg
ソル・メドロール静
メチルプレドニゾロ
注用40mg、同
ファイザー
ンコハク酸エステ
125mg、同500mg、
ルナトリウム
同1000mg
レボレード錠12.5
ノバルティスファー エルトロンボパグ
mg、
マ
オラミン
レボレード錠25 mg
ヤクルト本社
Ⅳ-85
協和キリン
Ⅳ-87
全薬工業
オキサリプラチン
開発内容
公知申請予定
(予定月)
個別事情
WGの検討状況
治癒切除不能な進行・再発の胃癌
2022年11月 WGで検討中
公知申請の該当性を検討中
治癒切除不能な進行・再発の胃癌
2022年11月 WGで検討中
公知申請の該当性を検討中
2023年2月 WGで検討中
公知申請の該当性を検討中
未定 WGで検討中
公知申請の該当性を検討中
2022年11月 WGで検討中
公知申請の該当性を検討中
2023年6月 WGで検討中
公知申請の該当性を検討中
川崎病の急性期(静注用免疫グロブリンに不
応または不応予測例)
慢性特発性血小板減少性紫斑病(小児)
【効能・効果】慢性特発性血小板減少性紫斑
病(小児に関する要望)
【用法・用量】ロミプロスチム(遺伝子組換え)
ロミプロスチム(遺 ロミプレート皮下注
として、初回投与量1 μg/kgを皮下投与す
伝子組換え)
250μg調製用
る。投与開始後は血小板数、症状に応じて投
与量を適宜増減し、週1回皮下投与する。ま
た、最高投与量は週1回10 μg/kgとする。
リツキサン点滴静
リツキシマブ(遺伝 注100mg
小児の慢性特発性血小板減少性紫斑病
子組換え)
リツキサン点滴静
注500mg