よむ、つかう、まなぶ。
資料1-1薬機法改正関係 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30193.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和4年度第2回 1/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
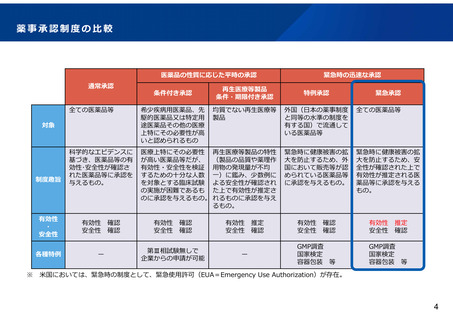
新たな制度による迅速化事例のイメージ
○ 緊急承認制度の効果は、個々の医薬品等の性質等に応じて異なる。想定される典型的な
事例としては、以下のとおり。
<海外で開発されたワクチン>
ケース
・海外で大規模治験(第Ⅲ相)
を実施
・国内治験が未実施
現行(確認)
新たな制度(推定)
×
・人種差・地域差等がないことの確
認のために国内治験が必要
○
・顕著な有効性があり、人種差・地域差の懸念があっても
高いベネフィットがあると推定できる場合、承認可能
例:日本以外の複数の国、人種において著しい有効性が確認さ
れ、日本人での有効性について特段の懸念材料がない場合に、
承認の判断を行うことができる可能性
例:抗体価が著しく上昇すること等が確認でき、それまでの限
られた知見ではあるが、その水準の抗体価であれば、発症予防
効果が期待できる場合に、承認の判断を行うことができる可能
性
※米国の緊急使用許可制度(EUA)でも、大規模な治験(第Ⅲ相)を実施。
※ファイザー社の新型コロナワクチンについて、海外データのみで評価を行った場合、承認の時期は2ヶ月程度早くなった可能性。
<国内で開発された治療薬>
ケース
現行(確認)
新たな制度(推定)
・比較的小規模な治験(第Ⅰ相+
第Ⅱ相)で一定の有効性が期待
される結果
・大規模な検証試験(第Ⅲ相)は
未実施
×
・第Ⅱ相までで一定の有効性が期待
される結果が出ているが、大規模
な試験での有効性を確認する必要
があることから、承認判断には第
Ⅲ相が必要
○
・第Ⅱ相までで一定の有効性があり、ベネフィットがあ
ると推定できる場合は、大規模な試験(第Ⅲ相)なしで
承認の判断が可能
※条件付き承認制度では、第Ⅱ相治験までで十分な結果が得られ、有効性が確認されれば、第Ⅲ相治験を省略可能。
ただし、そのほかの承認時に必要なGMP調査等を省略できず、結果的に承認までに時間がかかる可能性が高い。
5
○ 緊急承認制度の効果は、個々の医薬品等の性質等に応じて異なる。想定される典型的な
事例としては、以下のとおり。
<海外で開発されたワクチン>
ケース
・海外で大規模治験(第Ⅲ相)
を実施
・国内治験が未実施
現行(確認)
新たな制度(推定)
×
・人種差・地域差等がないことの確
認のために国内治験が必要
○
・顕著な有効性があり、人種差・地域差の懸念があっても
高いベネフィットがあると推定できる場合、承認可能
例:日本以外の複数の国、人種において著しい有効性が確認さ
れ、日本人での有効性について特段の懸念材料がない場合に、
承認の判断を行うことができる可能性
例:抗体価が著しく上昇すること等が確認でき、それまでの限
られた知見ではあるが、その水準の抗体価であれば、発症予防
効果が期待できる場合に、承認の判断を行うことができる可能
性
※米国の緊急使用許可制度(EUA)でも、大規模な治験(第Ⅲ相)を実施。
※ファイザー社の新型コロナワクチンについて、海外データのみで評価を行った場合、承認の時期は2ヶ月程度早くなった可能性。
<国内で開発された治療薬>
ケース
現行(確認)
新たな制度(推定)
・比較的小規模な治験(第Ⅰ相+
第Ⅱ相)で一定の有効性が期待
される結果
・大規模な検証試験(第Ⅲ相)は
未実施
×
・第Ⅱ相までで一定の有効性が期待
される結果が出ているが、大規模
な試験での有効性を確認する必要
があることから、承認判断には第
Ⅲ相が必要
○
・第Ⅱ相までで一定の有効性があり、ベネフィットがあ
ると推定できる場合は、大規模な試験(第Ⅲ相)なしで
承認の判断が可能
※条件付き承認制度では、第Ⅱ相治験までで十分な結果が得られ、有効性が確認されれば、第Ⅲ相治験を省略可能。
ただし、そのほかの承認時に必要なGMP調査等を省略できず、結果的に承認までに時間がかかる可能性が高い。
5