よむ、つかう、まなぶ。
資料2-3 ワクチンの安全性に関する評価について[170KB] (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
スパイクバックス筋注
(2価:起源株/オミクロ
5件
0件
6件
0件
3件
0件
ン株 BA.1)
スパイクバックス筋注
(2価:起源株/オミクロ
ン株 BA.4-5)
ヌバキソビッド筋注
2 新型コロナワクチンの副反応への対応について
(令和5年9月 14 日及び同9月 21 日開催合同部会)
令和5年9月14日及び同9月21日に開催された合同部会においては、新規に接種が開始
されるコミナティRTU筋注(1価:XBB.1.5)、コミナティ筋注5~11歳用(1価:XBB.1.5)、
コミナティ筋注6ヵ月~4歳用(1価:XBB.1.5)及びスパイクバックス筋注(1価:XBB.1.5)
の副反応疑い報告基準について、現時点において臨時接種の対象となっている全ての新型
コロナワクチンと同様に、アナフィラキシー、血小板減少を伴う血栓症(TTS)、心筋炎、
心膜炎、熱性けいれん、その他の反応を副反応疑い報告基準として扱うことが副反応検討
部会委員によって議決された。
3 各ワクチンの報告状況(令和5年7月 28 日及び同 10 月 27 日開催合同部会)
(1) 麻しん、風しん、おたふくかぜ、水痘、帯状疱疹、23 価肺炎球菌、HPV、百
日せき、ジフテリア、破傷風、不活化ポリオ、肺炎球菌(13 価)、肺炎球菌
(15 価)
、ヒブ、BCG、日本脳炎、B 型肝炎、ロタウイルス各ワクチンの報告
状況
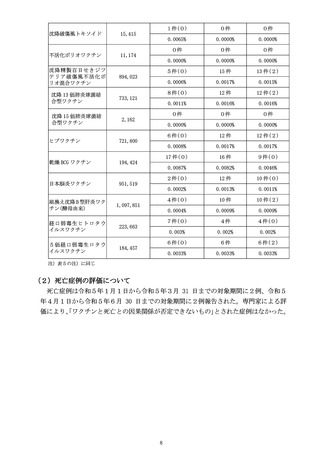
令和5年1月1日から令和5年3月 31 日までの報告状況は表5、令和5年4月1
日から令和5年6月 30 日までの報告状況は表6のとおり。これまでに報告されている
各ワクチンの報告状況と比べて大きな変化はなく、新たな措置をとる必要はないとさ
れた。
表5 各ワクチンの副反応疑い報告状況(R5.1.1~R5.3.31)
製造販売業者からの報告
接種可能のべ人数
【下段は報告頻度】
乾燥弱毒生麻しん風し
ん混合ワクチン
461,233
乾燥弱毒生麻しんワク
チン
11,767
5
( )内は死亡
医療機関からの報告
【下段は報告頻度】
報告数
うち重篤
1件(0)
4件
2件(0)
0.0002%
0.0009%
0.0004%
1件(0)
0件
0件
0.0085%
0.0000%
0.0000%
(2価:起源株/オミクロ
5件
0件
6件
0件
3件
0件
ン株 BA.1)
スパイクバックス筋注
(2価:起源株/オミクロ
ン株 BA.4-5)
ヌバキソビッド筋注
2 新型コロナワクチンの副反応への対応について
(令和5年9月 14 日及び同9月 21 日開催合同部会)
令和5年9月14日及び同9月21日に開催された合同部会においては、新規に接種が開始
されるコミナティRTU筋注(1価:XBB.1.5)、コミナティ筋注5~11歳用(1価:XBB.1.5)、
コミナティ筋注6ヵ月~4歳用(1価:XBB.1.5)及びスパイクバックス筋注(1価:XBB.1.5)
の副反応疑い報告基準について、現時点において臨時接種の対象となっている全ての新型
コロナワクチンと同様に、アナフィラキシー、血小板減少を伴う血栓症(TTS)、心筋炎、
心膜炎、熱性けいれん、その他の反応を副反応疑い報告基準として扱うことが副反応検討
部会委員によって議決された。
3 各ワクチンの報告状況(令和5年7月 28 日及び同 10 月 27 日開催合同部会)
(1) 麻しん、風しん、おたふくかぜ、水痘、帯状疱疹、23 価肺炎球菌、HPV、百
日せき、ジフテリア、破傷風、不活化ポリオ、肺炎球菌(13 価)、肺炎球菌
(15 価)
、ヒブ、BCG、日本脳炎、B 型肝炎、ロタウイルス各ワクチンの報告
状況
令和5年1月1日から令和5年3月 31 日までの報告状況は表5、令和5年4月1
日から令和5年6月 30 日までの報告状況は表6のとおり。これまでに報告されている
各ワクチンの報告状況と比べて大きな変化はなく、新たな措置をとる必要はないとさ
れた。
表5 各ワクチンの副反応疑い報告状況(R5.1.1~R5.3.31)
製造販売業者からの報告
接種可能のべ人数
【下段は報告頻度】
乾燥弱毒生麻しん風し
ん混合ワクチン
461,233
乾燥弱毒生麻しんワク
チン
11,767
5
( )内は死亡
医療機関からの報告
【下段は報告頻度】
報告数
うち重篤
1件(0)
4件
2件(0)
0.0002%
0.0009%
0.0004%
1件(0)
0件
0件
0.0085%
0.0000%
0.0000%