よむ、つかう、まなぶ。
14参考資料2-2_23 価肺炎球菌莢膜ポリサッカライドワクチン(肺炎球菌ワクチン)ファクトシート (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36952.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会(第58回 12/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
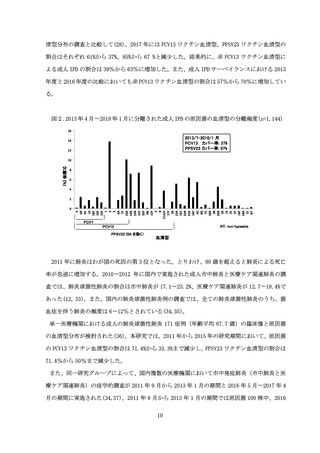
年 5 月〜2017 年 4 月の期間の調査では、原因菌 171 株の血清型分布が解析された。この異なる
研究期間において、PCV13 ワクチン血清型の割合は 54%から 32%に減少し、PPSV23 ワクチン血清
型の割合は 67%から 49%に減少した。
2.予防接種の目的と導入により期待される効果、安全性
(1)予防接種の目的
2 歳以上肺炎球菌による重篤疾患に罹患する危険が高い次のような個人および患者における
肺炎球菌による感染症の予防が目的である。すなわち、脾摘患者における肺炎球菌による感染症
の発症予防、鎌状赤血球疾患、あるいはその他の原因で脾機能不全である患者、心・呼吸器の慢
性疾患、腎不全、肝機能障害、糖尿病、慢 性髄液漏等の基礎疾患のある患者、高齢者、あるい
は免疫抑制作用を有する治療が予定されている者で治療開始まで少なくとも 14 日以上の余裕
のある患者における肺炎球菌による感染症の予防である。
(2)ワクチン製剤について
本剤は、肺炎球菌中で高頻度にみられる 23 種類の莢膜型(1、2、3、4、5、6B、7F、8、9N、9V、
10A、11A、12F、14、15B、17F、18C、19A、19F、20、22F、23F、33F)の 肺炎球菌を血清型別に
培養し、殺菌後にそれぞれの血清型の菌から莢膜ポリサッカライドを抽出、精製したものを混合
した液剤である。本剤は肺炎球菌の莢膜由来成分からなる不活化ワクチンである。 一 回当たり
0.5 ml を筋肉内又は皮下接種する、製剤 0.5 ml 中にはポリサッカライドを各型あたり 25μg ず
つ(総計 575μg)含有する。
(3)有効性の観点
成人においては PPSV23 の初回接種により血清中に特異抗体応答が認められる。しかしなが
ら、PPSV23 にはメモリーB 細胞を誘導できないために PPSV23 の 2 回目以降の接種による特異抗
体のブースター効果はない (38)。
①
PPSV23 初回接種の免疫原性
海外およびわが国における 65 歳以上の肺炎球菌ワクチン未接種の高齢者における PPSV23 と
PCV13(もしくは PCV7)の単回接種 1 ヶ月後の血清オプソニン活性の比較検討から、PPSV23 のワ
クチン血清型に対する免疫原性は PCV13 のそれと同等もしくは劣っていたと結論されている
(39-41)。
11
研究期間において、PCV13 ワクチン血清型の割合は 54%から 32%に減少し、PPSV23 ワクチン血清
型の割合は 67%から 49%に減少した。
2.予防接種の目的と導入により期待される効果、安全性
(1)予防接種の目的
2 歳以上肺炎球菌による重篤疾患に罹患する危険が高い次のような個人および患者における
肺炎球菌による感染症の予防が目的である。すなわち、脾摘患者における肺炎球菌による感染症
の発症予防、鎌状赤血球疾患、あるいはその他の原因で脾機能不全である患者、心・呼吸器の慢
性疾患、腎不全、肝機能障害、糖尿病、慢 性髄液漏等の基礎疾患のある患者、高齢者、あるい
は免疫抑制作用を有する治療が予定されている者で治療開始まで少なくとも 14 日以上の余裕
のある患者における肺炎球菌による感染症の予防である。
(2)ワクチン製剤について
本剤は、肺炎球菌中で高頻度にみられる 23 種類の莢膜型(1、2、3、4、5、6B、7F、8、9N、9V、
10A、11A、12F、14、15B、17F、18C、19A、19F、20、22F、23F、33F)の 肺炎球菌を血清型別に
培養し、殺菌後にそれぞれの血清型の菌から莢膜ポリサッカライドを抽出、精製したものを混合
した液剤である。本剤は肺炎球菌の莢膜由来成分からなる不活化ワクチンである。 一 回当たり
0.5 ml を筋肉内又は皮下接種する、製剤 0.5 ml 中にはポリサッカライドを各型あたり 25μg ず
つ(総計 575μg)含有する。
(3)有効性の観点
成人においては PPSV23 の初回接種により血清中に特異抗体応答が認められる。しかしなが
ら、PPSV23 にはメモリーB 細胞を誘導できないために PPSV23 の 2 回目以降の接種による特異抗
体のブースター効果はない (38)。
①
PPSV23 初回接種の免疫原性
海外およびわが国における 65 歳以上の肺炎球菌ワクチン未接種の高齢者における PPSV23 と
PCV13(もしくは PCV7)の単回接種 1 ヶ月後の血清オプソニン活性の比較検討から、PPSV23 のワ
クチン血清型に対する免疫原性は PCV13 のそれと同等もしくは劣っていたと結論されている
(39-41)。
11