よむ、つかう、まなぶ。
【資料2-3】プレパンデミックワクチンの開発体制について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40300.html |
| 出典情報 | 厚生科学審議会 感染症部会(第85回 5/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
現在のプレパンデミックワクチンの開発体制について
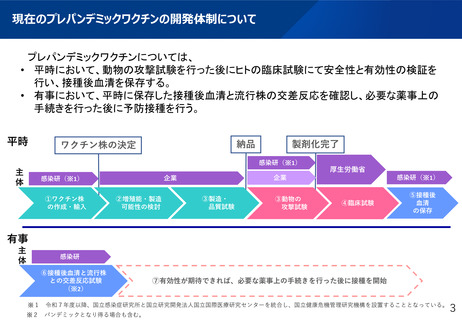
プレパンデミックワクチンについては、
• 平時において、動物の攻撃試験を行った後にヒトの臨床試験にて安全性と有効性の検証を
行い、接種後血清を保存する。
• 有事において、平時に保存した接種後血清と流行株の交差反応を確認し、必要な薬事上の
手続きを行った後に予防接種を行う。
平時
納品
ワクチン株の決定
製剤化完了
感染研(※1)
主
体
企業
感染研(※1)
①ワクチン株
の作成・輸入
②増殖能・製造
可能性の検討
厚生労働省
感染研(※1)
企業
③製造・
品質試験
③動物の
攻撃試験
④臨床試験
⑤接種後
血清
の保存
有事
主
体
感染研
⑥接種後血清と流行株
との交差反応試験
(※2)
⑦有効性が期待できれば、必要な薬事上の手続きを行った後に接種を開始
※1 令和7年度以降、国立感染症研究所と国立研究開発法人国立国際医療研究センターを統合し、国立健康危機管理研究機構を設置することとなっている。
※2
パンデミックとなり得る場合も含む。
3
プレパンデミックワクチンについては、
• 平時において、動物の攻撃試験を行った後にヒトの臨床試験にて安全性と有効性の検証を
行い、接種後血清を保存する。
• 有事において、平時に保存した接種後血清と流行株の交差反応を確認し、必要な薬事上の
手続きを行った後に予防接種を行う。
平時
納品
ワクチン株の決定
製剤化完了
感染研(※1)
主
体
企業
感染研(※1)
①ワクチン株
の作成・輸入
②増殖能・製造
可能性の検討
厚生労働省
感染研(※1)
企業
③製造・
品質試験
③動物の
攻撃試験
④臨床試験
⑤接種後
血清
の保存
有事
主
体
感染研
⑥接種後血清と流行株
との交差反応試験
(※2)
⑦有効性が期待できれば、必要な薬事上の手続きを行った後に接種を開始
※1 令和7年度以降、国立感染症研究所と国立研究開発法人国立国際医療研究センターを統合し、国立健康危機管理研究機構を設置することとなっている。
※2
パンデミックとなり得る場合も含む。
3