よむ、つかう、まなぶ。
資料2-28 ロタウイルスワクチンに係る腸重積症に関する報告[1.2MB] (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00106.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第102回 7/29)医薬品等安全対策部会安全対策調査会(令和6年度第4回 7/29)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
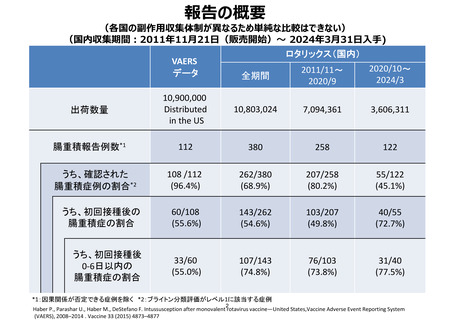
報告の概要
(各国の副作⽤収集体制が異なるため単純な⽐較はできない)
(国内収集期間︓2011年11月21⽇(販売開始)〜 2024年3月31日入手)
ロタリックス(国内)
VAERS
データ
全期間
2011/11~
2020/9
2020/10~
2024/3
出荷数量
10,900,000
Distributed
in the US
10,803,024
7,094,361
3,606,311
腸重積報告例数*1
112
380
258
122
うち、確認された
腸重積症例の割合*2
108 /112
(96.4%)
262/380
(68.9%)
207/258
(80.2%)
55/122
(45.1%)
うち、初回接種後の
腸重積症の割合
60/108
(55.6%)
143/262
(54.6%)
103/207
(49.8%)
40/55
(72.7%)
うち、初回接種後
0-6日以内の
腸重積症の割合
33/60
(55.0%)
107/143
(74.8%)
76/103
(73.8%)
31/40
(77.5%)
*1:因果関係が否定できる症例を除く *2:ブライトン分類評価がレベル1に該当する症例
2
Haber P., Parashar U., Haber M., DeStefano F. Intussusception after monovalent rotavirus vaccine—United States,Vaccine Adverse Event Reporting System
(VAERS), 2008–2014 . Vaccine 33 (2015) 4873–4877
(各国の副作⽤収集体制が異なるため単純な⽐較はできない)
(国内収集期間︓2011年11月21⽇(販売開始)〜 2024年3月31日入手)
ロタリックス(国内)
VAERS
データ
全期間
2011/11~
2020/9
2020/10~
2024/3
出荷数量
10,900,000
Distributed
in the US
10,803,024
7,094,361
3,606,311
腸重積報告例数*1
112
380
258
122
うち、確認された
腸重積症例の割合*2
108 /112
(96.4%)
262/380
(68.9%)
207/258
(80.2%)
55/122
(45.1%)
うち、初回接種後の
腸重積症の割合
60/108
(55.6%)
143/262
(54.6%)
103/207
(49.8%)
40/55
(72.7%)
うち、初回接種後
0-6日以内の
腸重積症の割合
33/60
(55.0%)
107/143
(74.8%)
76/103
(73.8%)
31/40
(77.5%)
*1:因果関係が否定できる症例を除く *2:ブライトン分類評価がレベル1に該当する症例
2
Haber P., Parashar U., Haber M., DeStefano F. Intussusception after monovalent rotavirus vaccine—United States,Vaccine Adverse Event Reporting System
(VAERS), 2008–2014 . Vaccine 33 (2015) 4873–4877