よむ、つかう、まなぶ。
【資料1】改正再生医療等安全性確保法におけるワクチンの扱いについて (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41827.html |
| 出典情報 | 厚生科学審議会 感染症部会(第88回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
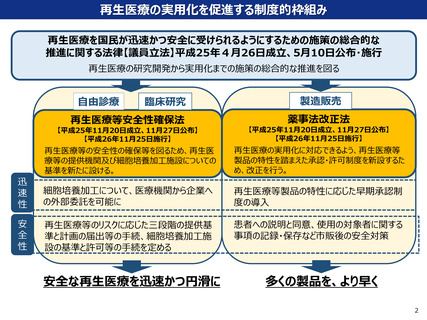
再生医療の実用化を促進する制度的枠組み
再生医療を国民が迅速かつ安全に受けられるようにするための施策の総合的な
推進に関する法律【議員立法】平成25年4月26日成立、5月10日公布・施行
再生医療の研究開発から実用化までの施策の総合的な推進を図る
自由診療
臨床研究
再生医療等安全性確保法
製造販売
薬事法改正法
【平成25年11月20日成立、11月27日公布】
【平成26年11月25日施行】
【平成25年11月20日成立、11月27日公布】
【平成26年11月25日施行】
再生医療等の安全性の確保等を図るため、再生医
療等の提供機関及び細胞培養加工施設についての
基準を新たに設ける。
再生医療の実用化に対応できるよう、再生医療等
製品の特性を踏まえた承認・許可制度を新設するた
め、改正を行う。
迅
速
性
細胞培養加工について、医療機関から企業へ
の外部委託を可能に
再生医療等製品の特性に応じた早期承認制
度の導入
安
全
性
再生医療等のリスクに応じた三段階の提供基
準と計画の届出等の手続、細胞培養加工施
設の基準と許可等の手続を定める
患者への説明と同意、使用の対象者に関する
事項の記録・保存など市販後の安全対策
安全な再生医療を迅速かつ円滑に
多くの製品を、より早く
2
再生医療を国民が迅速かつ安全に受けられるようにするための施策の総合的な
推進に関する法律【議員立法】平成25年4月26日成立、5月10日公布・施行
再生医療の研究開発から実用化までの施策の総合的な推進を図る
自由診療
臨床研究
再生医療等安全性確保法
製造販売
薬事法改正法
【平成25年11月20日成立、11月27日公布】
【平成26年11月25日施行】
【平成25年11月20日成立、11月27日公布】
【平成26年11月25日施行】
再生医療等の安全性の確保等を図るため、再生医
療等の提供機関及び細胞培養加工施設についての
基準を新たに設ける。
再生医療の実用化に対応できるよう、再生医療等
製品の特性を踏まえた承認・許可制度を新設するた
め、改正を行う。
迅
速
性
細胞培養加工について、医療機関から企業へ
の外部委託を可能に
再生医療等製品の特性に応じた早期承認制
度の導入
安
全
性
再生医療等のリスクに応じた三段階の提供基
準と計画の届出等の手続、細胞培養加工施
設の基準と許可等の手続を定める
患者への説明と同意、使用の対象者に関する
事項の記録・保存など市販後の安全対策
安全な再生医療を迅速かつ円滑に
多くの製品を、より早く
2