よむ、つかう、まなぶ。
資料1-3 ワクチンの安全性に関する評価について[241KB] (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ダイチロナ筋注
(1価:オミクロン株
0件
0件
0件
0件
XBB.1.5)
ヌバキソビッド筋注
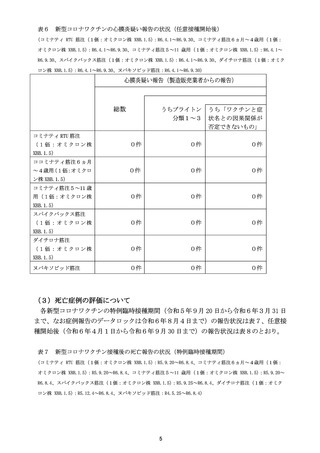
(4)新型コロナワクチンの副反応疑い報告の速報(令和6年 10 月1日から令和
6年 11 月 30 日報告分まで)
令和7年1月 24 日の合同部会では、令和6年 10 月1日から開始された新型コロナワ
クチンの定期接種に係る副反応疑い報告について、令和6年 11 月 30 日報告分までの症例
一覧を速報として報告した(医療機関からの報告について重篤症例 14 例、非重篤症例 14
例、製造販売業者からの報告 60 例)
。これらの報告については重複の確認や専門家評価な
どの整理が行われておらず、暫定的な評価ではあるものの、本速報において特定の副反応
の集積はみられておらず、引き続き、情報収集及び評価を進めることとされた。
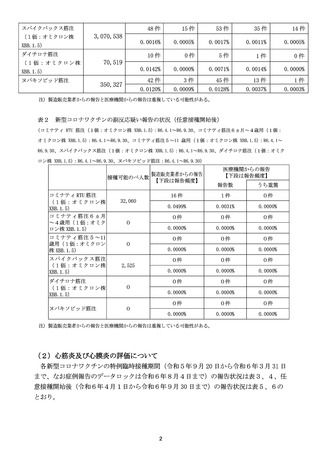
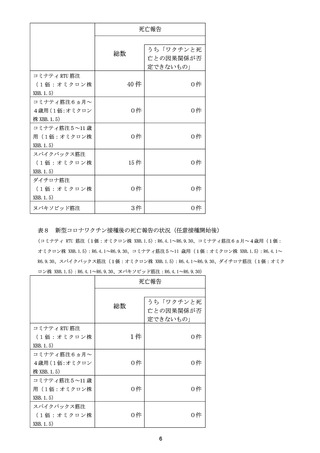
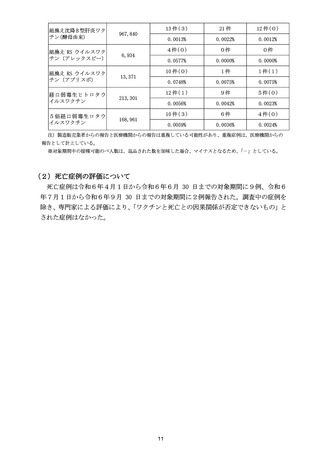
また、Meiji Seika ファルマ社のレプリコンワクチンであるコスタイベ筋注用につい
て、参考資料として、市販直後調査の中間報告(3ヵ月時点:令和6年9月 30 日~12 月
29 日)を提示した。重篤な症例が7例8件報告、うち死亡例が2例報告されているが、
死亡例はいずれも接種後から 20 日以上後の死亡であるなど、詳細評価を待つ必要はある
ものの、現時点で、重大な懸念があるとは考えられない、と評価された。
今後、医療機関や製造販売業者から報告された副反応疑い報告について、必要な整理を
行った上で、次回以降の合同部会での評価を行う予定である。
2 各ワクチンの報告状況(令和6年 10 月 25 日及び令和7年1月 24 日開催合同
部会)
(1) 麻しん、風しん、おたふくかぜ、水痘、帯状疱疹、肺炎球菌(23 価)
、HPV、
百日せき、ジフテリア、破傷風、不活化ポリオ、肺炎球菌(13 価)、肺炎球
菌(20 価)肺炎球菌(15 価)
、ヒブ、BCG、日本脳炎、B 型肝炎、RS ウイル
ス、ロタウイルス各ワクチンの報告状況
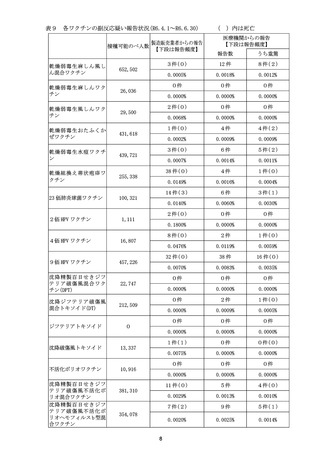
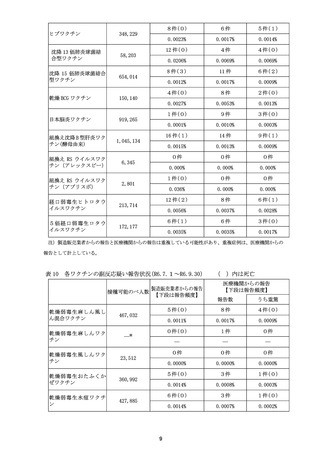
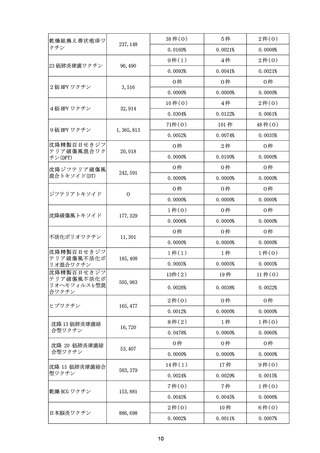
令和6年4月1日から令和6年6月 30 日までの報告状況は表9、令和6年7月1
日から令和6年9月 30 日までの報告状況は表 10 のとおり。これまでに報告されてい
る各ワクチンの報告状況と比べて大きな変化はなく、新たな措置をとる必要はないと
された。なお、令和7年1月 24 日開催の合同部会より沈降 20 価肺炎球菌結合型ワク
チンが審議対象として追加された。
7
(1価:オミクロン株
0件
0件
0件
0件
XBB.1.5)
ヌバキソビッド筋注
(4)新型コロナワクチンの副反応疑い報告の速報(令和6年 10 月1日から令和
6年 11 月 30 日報告分まで)
令和7年1月 24 日の合同部会では、令和6年 10 月1日から開始された新型コロナワ
クチンの定期接種に係る副反応疑い報告について、令和6年 11 月 30 日報告分までの症例
一覧を速報として報告した(医療機関からの報告について重篤症例 14 例、非重篤症例 14
例、製造販売業者からの報告 60 例)
。これらの報告については重複の確認や専門家評価な
どの整理が行われておらず、暫定的な評価ではあるものの、本速報において特定の副反応
の集積はみられておらず、引き続き、情報収集及び評価を進めることとされた。
また、Meiji Seika ファルマ社のレプリコンワクチンであるコスタイベ筋注用につい
て、参考資料として、市販直後調査の中間報告(3ヵ月時点:令和6年9月 30 日~12 月
29 日)を提示した。重篤な症例が7例8件報告、うち死亡例が2例報告されているが、
死亡例はいずれも接種後から 20 日以上後の死亡であるなど、詳細評価を待つ必要はある
ものの、現時点で、重大な懸念があるとは考えられない、と評価された。
今後、医療機関や製造販売業者から報告された副反応疑い報告について、必要な整理を
行った上で、次回以降の合同部会での評価を行う予定である。
2 各ワクチンの報告状況(令和6年 10 月 25 日及び令和7年1月 24 日開催合同
部会)
(1) 麻しん、風しん、おたふくかぜ、水痘、帯状疱疹、肺炎球菌(23 価)
、HPV、
百日せき、ジフテリア、破傷風、不活化ポリオ、肺炎球菌(13 価)、肺炎球
菌(20 価)肺炎球菌(15 価)
、ヒブ、BCG、日本脳炎、B 型肝炎、RS ウイル
ス、ロタウイルス各ワクチンの報告状況
令和6年4月1日から令和6年6月 30 日までの報告状況は表9、令和6年7月1
日から令和6年9月 30 日までの報告状況は表 10 のとおり。これまでに報告されてい
る各ワクチンの報告状況と比べて大きな変化はなく、新たな措置をとる必要はないと
された。なお、令和7年1月 24 日開催の合同部会より沈降 20 価肺炎球菌結合型ワク
チンが審議対象として追加された。
7