よむ、つかう、まなぶ。
資料2-8 サリドマイド登録システム(SMUD)年次報告書の公開について(報告)[1.9MB] (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_33888.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第1回 6/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
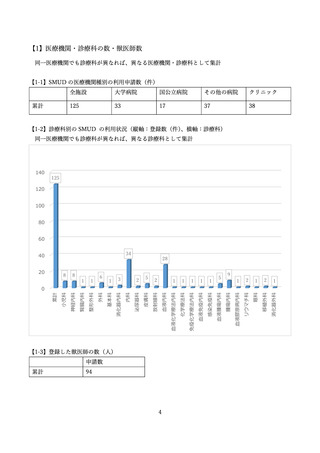
【6-2D】疾患別の投与期間による副作用の疑いの報告に関する集計(2)
【6-1】および【6-2A】に示したアンケート結果から、投与期間による副作用の疑いの報告に関する
集計を行った。
【6-2D】では、治療終了した患者のうち、副作用の疑いが報告された患者数を 180 日
で区分した結果を示す。
180 日未満
180 日以上
(N=215)
(N=328)
52
92
副作用の疑いの報告患者数
合計
144
縦軸:件数、横軸:副作用の疑い
26
17
30
21
15
9
2
20
4
0
1
0
4
1
1
2
2
0
0
0
1
0
0
0
1
0
0
0
0
0
1
0
0
1
2
甲状腺機能低下症
息切れ
徐脈
白血球減少
血小板減少
口渇
発熱
その他
0
頭痛
0
吐気
1
浮腫
0
4
1
0
振戦
0
2
運動失調
0
2
1
0
抑うつ
0
0
皮疹
0
0
めまい
0
0
眠気
5
0
5
0
倦怠感
2
0
4
2
10
5
4 9
末梢神経障害
静脈血栓症
便秘
0
180日未満
180日以上
23
合計
【6-1】および【6-2A】に示したアンケート結果から、投与期間による副作用の疑いの報告に関する
集計を行った。
【6-2D】では、治療終了した患者のうち、副作用の疑いが報告された患者数を 180 日
で区分した結果を示す。
180 日未満
180 日以上
(N=215)
(N=328)
52
92
副作用の疑いの報告患者数
合計
144
縦軸:件数、横軸:副作用の疑い
26
17
30
21
15
9
2
20
4
0
1
0
4
1
1
2
2
0
0
0
1
0
0
0
1
0
0
0
0
0
1
0
0
1
2
甲状腺機能低下症
息切れ
徐脈
白血球減少
血小板減少
口渇
発熱
その他
0
頭痛
0
吐気
1
浮腫
0
4
1
0
振戦
0
2
運動失調
0
2
1
0
抑うつ
0
0
皮疹
0
0
めまい
0
0
眠気
5
0
5
0
倦怠感
2
0
4
2
10
5
4 9
末梢神経障害
静脈血栓症
便秘
0
180日未満
180日以上
23
合計