よむ、つかう、まなぶ。
資料2-4 市販後安全性情報に関する報告(製造販売業者の公表資料)[1.6MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34889.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和5年度第6回 8/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
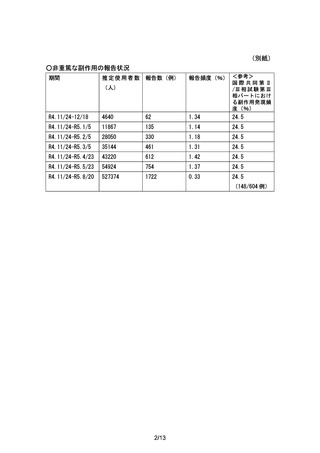
ゾコーバ錠 市販後の「副作用収集状況」報告
推定使用患者数:
推定
527,374 登録センター登録患者数+納入数量より算出した患者数(一般流通品)
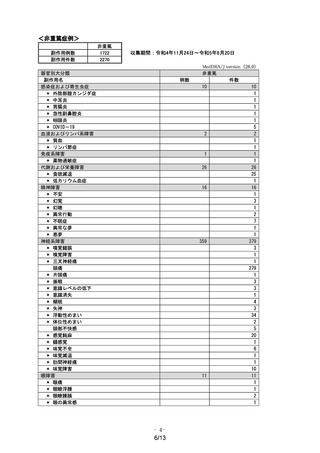
<重篤症例>
副作用例数
副作用件数
重篤
22
27
収集期間:令和4年11月24日~令和5年8月20日
器官別大分類
副作用名
良性、悪性および詳細不明の新生物(嚢胞およびポリープを含む)
* びまん性大細胞型 B 細胞性リンパ腫
免疫系障害
アナフィラキシー反応
* アナフィラキシーショック
代謝および栄養障害
* 低血糖
神経系障害
頭痛
* 意識消失
* てんかん
血管障害
* 低血圧
胃腸障害
* 血便排泄
* メレナ
下痢
* 麻痺性イレウス
悪心
嘔吐
肝胆道系障害
* 胆嚢炎
* 劇症肝炎
皮膚および皮下組織障害
* 急性汎発性発疹性膿疱症
腎および尿路障害
* 急性腎障害
妊娠、産褥および周産期の状態
* 流産
一般・全身障害および投与部位の状態
* 低体温
* 全身性浮腫
臨床検査
* アラニンアミノトランスフェラーゼ増加
* アスパラギン酸アミノトランスフェラーゼ増加
* 肝機能検査異常
MedDRA/J version(26.0)
重篤
例数
件数
1
1
1
3
3
2
1
1
1
1
3
3
1
1
1
1
1
1
6
8
1
1
2
1
1
2
2
2
1
1
1
1
1
1
1
1
1
1
1
2
2
1
1
2
3
1
1
1
(ご注意)
*印は「使用上の注意」から予測できない副作用を示します。因果関係が不明のものも副作用としてカウント
しています。
本報告書の「重篤」の件数には、「医師等から重篤と報告いただいたもの」もしくは「医師等からの報告では
- 24/13
推定使用患者数:
推定
527,374 登録センター登録患者数+納入数量より算出した患者数(一般流通品)
<重篤症例>
副作用例数
副作用件数
重篤
22
27
収集期間:令和4年11月24日~令和5年8月20日
器官別大分類
副作用名
良性、悪性および詳細不明の新生物(嚢胞およびポリープを含む)
* びまん性大細胞型 B 細胞性リンパ腫
免疫系障害
アナフィラキシー反応
* アナフィラキシーショック
代謝および栄養障害
* 低血糖
神経系障害
頭痛
* 意識消失
* てんかん
血管障害
* 低血圧
胃腸障害
* 血便排泄
* メレナ
下痢
* 麻痺性イレウス
悪心
嘔吐
肝胆道系障害
* 胆嚢炎
* 劇症肝炎
皮膚および皮下組織障害
* 急性汎発性発疹性膿疱症
腎および尿路障害
* 急性腎障害
妊娠、産褥および周産期の状態
* 流産
一般・全身障害および投与部位の状態
* 低体温
* 全身性浮腫
臨床検査
* アラニンアミノトランスフェラーゼ増加
* アスパラギン酸アミノトランスフェラーゼ増加
* 肝機能検査異常
MedDRA/J version(26.0)
重篤
例数
件数
1
1
1
3
3
2
1
1
1
1
3
3
1
1
1
1
1
1
6
8
1
1
2
1
1
2
2
2
1
1
1
1
1
1
1
1
1
1
1
2
2
1
1
2
3
1
1
1
(ご注意)
*印は「使用上の注意」から予測できない副作用を示します。因果関係が不明のものも副作用としてカウント
しています。
本報告書の「重篤」の件数には、「医師等から重篤と報告いただいたもの」もしくは「医師等からの報告では
- 24/13