よむ、つかう、まなぶ。
【資料1】医薬品の製造方法等に係る薬事審査等のあり方について (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35743.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第4回 10/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
日米欧で事前承認に要する審査期間
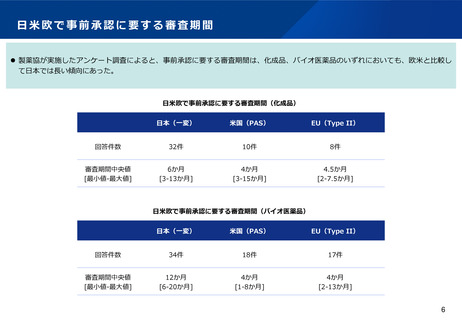
⚫ 製薬協が実施したアンケート調査によると、事前承認に要する審査期間は、化成品、バイオ医薬品のいずれにおいても、欧米と比較し
て日本では長い傾向にあった。
日米欧で事前承認に要する審査期間(化成品)
日本(一変)
米国(PAS)
EU(Type II)
回答件数
32件
10件
8件
審査期間中央値
[最小値-最大値]
6か月
[3-13か月]
4か月
[3-15か月]
4.5か月
[2-7.5か月]
日米欧で事前承認に要する審査期間(バイオ医薬品)
日本(一変)
米国(PAS)
EU(Type II)
回答件数
34件
18件
17件
審査期間中央値
[最小値-最大値]
12か月
[6-20か月]
4か月
[1-8か月]
4か月
[2-13か月]
6
⚫ 製薬協が実施したアンケート調査によると、事前承認に要する審査期間は、化成品、バイオ医薬品のいずれにおいても、欧米と比較し
て日本では長い傾向にあった。
日米欧で事前承認に要する審査期間(化成品)
日本(一変)
米国(PAS)
EU(Type II)
回答件数
32件
10件
8件
審査期間中央値
[最小値-最大値]
6か月
[3-13か月]
4か月
[3-15か月]
4.5か月
[2-7.5か月]
日米欧で事前承認に要する審査期間(バイオ医薬品)
日本(一変)
米国(PAS)
EU(Type II)
回答件数
34件
18件
17件
審査期間中央値
[最小値-最大値]
12か月
[6-20か月]
4か月
[1-8か月]
4か月
[2-13か月]
6