よむ、つかう、まなぶ。
03 資料1_海外製インフルエンザワクチンの製造株選定に伴う薬事関係の具体的なスケジュール等について (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37873.html |
| 出典情報 | 厚生科学審議会予防接種・ワクチン分科会研究開発及び生産・流通部会(第34回 2/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
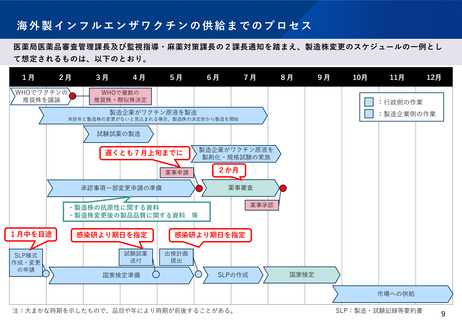
海外製インフルエンザワクチンの供給までのプロセス
医薬局医薬品審査管理課長及び監視指導・麻薬対策課長の2課長通知を踏まえ、製造株変更のスケジュールの一例とし
て想定されるものは、以下のとおり。
1月
2月
WHOでワクチンの
推奨株を議論
3月
4月
5月
6月
7月
8月
WHOで複数の
推奨株・類似株決定
9月
10月
11月
12月
:行政側の作業
製造企業がワクチン原液を製造
:製造企業側の作業
※前年と製造株の変更がないと見込まれる場合、製造株の決定前から製造を開始
試験試薬の製造
遅くとも7月上旬までに
薬事申請
製造企業がワクチン原液を
製剤化・規格試験の実施
2か月
薬事審査
承認事項一部変更申請の準備
薬事承認
・製造株の抗原性に関する資料
・製造株変更後の製品品質に関する資料 等
1月中を目途
SLP様式
作成・変更
の申請
感染研より期日を指定
試験試薬
送付
国家検定準備
感染研より期日を指定
出検計画
提出
SLPの作成
国家検定
市場への供給
注:大まかな時期を示したもので、品目や年により時期が前後することがある。
SLP:製造・試験記録等要約書
9
医薬局医薬品審査管理課長及び監視指導・麻薬対策課長の2課長通知を踏まえ、製造株変更のスケジュールの一例とし
て想定されるものは、以下のとおり。
1月
2月
WHOでワクチンの
推奨株を議論
3月
4月
5月
6月
7月
8月
WHOで複数の
推奨株・類似株決定
9月
10月
11月
12月
:行政側の作業
製造企業がワクチン原液を製造
:製造企業側の作業
※前年と製造株の変更がないと見込まれる場合、製造株の決定前から製造を開始
試験試薬の製造
遅くとも7月上旬までに
薬事申請
製造企業がワクチン原液を
製剤化・規格試験の実施
2か月
薬事審査
承認事項一部変更申請の準備
薬事承認
・製造株の抗原性に関する資料
・製造株変更後の製品品質に関する資料 等
1月中を目途
SLP様式
作成・変更
の申請
感染研より期日を指定
試験試薬
送付
国家検定準備
感染研より期日を指定
出検計画
提出
SLPの作成
国家検定
市場への供給
注:大まかな時期を示したもので、品目や年により時期が前後することがある。
SLP:製造・試験記録等要約書
9