よむ、つかう、まなぶ。
総ー1高額医薬品(認知症薬)に対する対応 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43713.html |
| 出典情報 | 中央社会保険医療協議会 総会(第595回 9/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ケサンラの最適使用推進ガイドラインについて(イメージ)
〇 本剤は認知症に対する新規作用機序の医薬品であり、臨床試験における有効性及び安全性を踏ま
え、適切な患者選択や投与判断、重篤な副作用発現(特に、アミロイド関連画像異常(ARIA)の発
現)の際の迅速な安全対策等を確保した上で、最適な薬物療法を提供できるように進めていく必要
があることから、添付文書に加えて、最適使用推進ガイドラインを作成することとしている。
〇 ガイドラインでは、投与開始にあたり、患者要件(投与開始にあたり禁忌に該当しないことの確
認、認知症のスコア評価、アミロイドβ病理を示唆する所見の確認など)とともに、医師・施設の要
件(診断やARIAの画像所見の判断等ができる医師、必要なスコア評価やARIA判断等ができるチーム
体制や検査体制等を有する施設)を定める予定。
〇 また、投与開始後は、
・ 有効性の確認として、6か月に1回、臨床症状の確認を行い、投与継続の可否を判断
・ 安全性の確認として、本剤 2 回目の投与前、増量前(通常 4 回目の投与前)、及び 7 回目の投
与前、並びにそれ以降も定期的にMRI検査を実施し、ARIAの有無を確認
・ 安全性上の理由等で本剤 1400mg に増量できない場合は、漫然と投与を継続しない
・ 本剤投与後12か月を目安にアミロイドPET検査又は同等の診断法を実施し、アミロイドβプラー
クの除去を評価し、本剤の投与終了の可否を検討
することを求める予定。
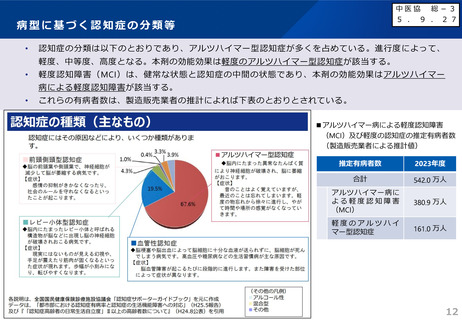
〇 したがって、「アルツハイマー病による軽度認知障害及び軽度の認知症」の推定有病者数は多い
ものの、現時点のガイドラインを踏まえると、本剤の投与対象となる患者数は限定的になる見込み
である。
6
〇 本剤は認知症に対する新規作用機序の医薬品であり、臨床試験における有効性及び安全性を踏ま
え、適切な患者選択や投与判断、重篤な副作用発現(特に、アミロイド関連画像異常(ARIA)の発
現)の際の迅速な安全対策等を確保した上で、最適な薬物療法を提供できるように進めていく必要
があることから、添付文書に加えて、最適使用推進ガイドラインを作成することとしている。
〇 ガイドラインでは、投与開始にあたり、患者要件(投与開始にあたり禁忌に該当しないことの確
認、認知症のスコア評価、アミロイドβ病理を示唆する所見の確認など)とともに、医師・施設の要
件(診断やARIAの画像所見の判断等ができる医師、必要なスコア評価やARIA判断等ができるチーム
体制や検査体制等を有する施設)を定める予定。
〇 また、投与開始後は、
・ 有効性の確認として、6か月に1回、臨床症状の確認を行い、投与継続の可否を判断
・ 安全性の確認として、本剤 2 回目の投与前、増量前(通常 4 回目の投与前)、及び 7 回目の投
与前、並びにそれ以降も定期的にMRI検査を実施し、ARIAの有無を確認
・ 安全性上の理由等で本剤 1400mg に増量できない場合は、漫然と投与を継続しない
・ 本剤投与後12か月を目安にアミロイドPET検査又は同等の診断法を実施し、アミロイドβプラー
クの除去を評価し、本剤の投与終了の可否を検討
することを求める予定。
〇 したがって、「アルツハイマー病による軽度認知障害及び軽度の認知症」の推定有病者数は多い
ものの、現時点のガイドラインを踏まえると、本剤の投与対象となる患者数は限定的になる見込み
である。
6