よむ、つかう、まなぶ。
薬-参考 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46579.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第230回 12/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和6年薬価制度改革
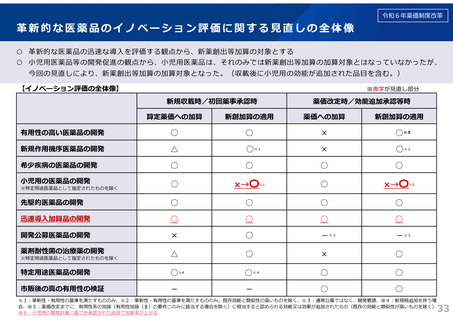
革新的な医薬品のイノベーション評価に関する見直しの全体像
○ 革新的な医薬品の迅速な導入を評価する観点から、新薬創出等加算の対象とする
○ 小児用医薬品等の開発促進の観点から、小児用医薬品は、それのみでは新薬創出等加算の加算対象とはなっていなかったが、
今回の見直しにより、新薬創出等加算の加算対象となった。(収載後に小児用の効能が追加された品目を含む。)
【イノベーション評価の全体像】
※赤字が見直し部分
新規収載時/初回薬事承認時
薬価改定時/効能追加承認等時
算定薬価への加算
新創加算の適用
薬価への加算
新創加算の適用
有用性の高い医薬品の開発
○
○
×
○※5
新規作用機序医薬品の開発
△
○※1
×
○※2
希少疾病の医薬品の開発
○
○
○
○
小児用の医薬品の開発
※特定用途医薬品として指定されたものを除く
○
×→〇
○
×→〇※6
先駆的医薬品の開発
○
○
○
○
迅速導入加算品の開発
○
○
○
○
開発公募医薬品の開発
×
○
-※3
-※3
薬剤耐性菌の治療薬の開発
※特定用途医薬品として指定されたものを除く
△
○
×
○
特定用途医薬品の開発
○※4
○※4
○
○
市販後の真の有用性の検証
-
-
○
○
※6
※1:革新性・有用性の基準を満たすもののみ、※2:革新性・有用性の基準を満たすもののみ。既存効能と類似性の高いものを除く、※3:通常公募ではなく、開発要請、※4:新規格追加を伴う場
合、※5:薬価改定までに、有用性系の加算(有用性加算(Ⅱ)の要件ニのみに該当する場合を除く)に相当すると認められる効能又は効果が追加されたもの(既存の効能と類似性が高いものを除く)
※6:小児用の開発計画に基づき承認された品目で加算率が上がる
33
革新的な医薬品のイノベーション評価に関する見直しの全体像
○ 革新的な医薬品の迅速な導入を評価する観点から、新薬創出等加算の対象とする
○ 小児用医薬品等の開発促進の観点から、小児用医薬品は、それのみでは新薬創出等加算の加算対象とはなっていなかったが、
今回の見直しにより、新薬創出等加算の加算対象となった。(収載後に小児用の効能が追加された品目を含む。)
【イノベーション評価の全体像】
※赤字が見直し部分
新規収載時/初回薬事承認時
薬価改定時/効能追加承認等時
算定薬価への加算
新創加算の適用
薬価への加算
新創加算の適用
有用性の高い医薬品の開発
○
○
×
○※5
新規作用機序医薬品の開発
△
○※1
×
○※2
希少疾病の医薬品の開発
○
○
○
○
小児用の医薬品の開発
※特定用途医薬品として指定されたものを除く
○
×→〇
○
×→〇※6
先駆的医薬品の開発
○
○
○
○
迅速導入加算品の開発
○
○
○
○
開発公募医薬品の開発
×
○
-※3
-※3
薬剤耐性菌の治療薬の開発
※特定用途医薬品として指定されたものを除く
△
○
×
○
特定用途医薬品の開発
○※4
○※4
○
○
市販後の真の有用性の検証
-
-
○
○
※6
※1:革新性・有用性の基準を満たすもののみ、※2:革新性・有用性の基準を満たすもののみ。既存効能と類似性の高いものを除く、※3:通常公募ではなく、開発要請、※4:新規格追加を伴う場
合、※5:薬価改定までに、有用性系の加算(有用性加算(Ⅱ)の要件ニのみに該当する場合を除く)に相当すると認められる効能又は効果が追加されたもの(既存の効能と類似性が高いものを除く)
※6:小児用の開発計画に基づき承認された品目で加算率が上がる
33