よむ、つかう、まなぶ。
○1 患者申出療養の中間報告について別紙2 (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00020.html |
| 出典情報 | 患者申出療養評価会議(第33回 9/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙2
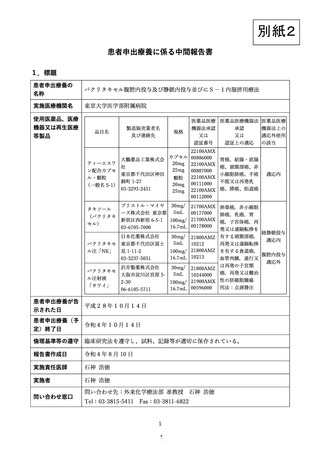
患者申出療養に係る中間報告書
1.標題
患者申出療養の
名称
パクリタキセル腹腔内投与及び静脈内投与並びにS-1内服併用療法
実施医療機関名
東京大学医学部附属病院
使用医薬品、医療
機器又は再生医療
等製品
医薬品医療 医薬品医療機器法 医薬品医療
品目名
製造販売業者名
及び連絡先
規格
機器法承認
又は
承認
又は
認証番号
認証上の適応
22100AMX
カプセル 00886000
ティーエスワ
20mg 22100AMX
社
25mg 00887000
ン配合カプセ
東京都千代田区神田
22100AMX
ル・顆粒
顆粒
錦町 1-27
20mg 00111000
(一般名 S-1)
03-3293-2451
25mg 22100AMX
00112000
大鵬薬品工業株式会
ブリストル・マイヤ
30mg/
ーズ株式会社 東京都 5mL
(パクリタキ
新宿区西新宿 6-5-1 100mg/
セル)
16.7mL
03-6705-7000
タキソール
日本化薬株式会社
パクリタキセ 東京都千代田区富士
ル注「NK」
見 1-11-2
03-3237-5051
沢井製薬株式会社
21800AMZ
10212
100mg/ 21800AMZ
16.7mL 10213
30mg/
5mL
癌、頭頸部癌、非
小細胞肺癌、手術
患者申出療養(予
定)終了日
癌、膵癌、胆道癌
有する頭頸部癌,
再発又は遠隔転移
を有する食道癌,
血管肉腫,進行又
は再発の子宮頸
平成28年10月14日
令和4年10月14日
倫理基準等の遵守
臨床研究法を遵守し、試料、記録等が適切に保存されている。
報告書作成日
令和4年 8 月 10 日
実施責任医師
石神 浩徳
実施者
石神 浩徳
問い合わせ窓口
問い合わせ先:外来化学療法部 准教授 石神 浩徳
Tel:03-3815-5411
Fax:03-3811-6822
1
1
適応内
不能又は再発乳
21800AMZ
パクリタキセ
癌,再発又は難治
大阪市淀川区宮原 510244000
ル注射液
2-30
100mg/ 21900AMX 性の胚細胞腫瘍
「サワイ」
用法:点滴静注
16.7mL 00596000
06-6105-5711
患者申出療養が告
示された日
の該当
胃癌、結腸・直腸
21700AMX 卵巣癌,非小細胞
00177000
肺癌,乳癌,胃
21700AMX 癌,子宮体癌,再
00178000
発又は遠隔転移を
30mg/
5mL
機器法上の
適応外使用
経静脈投与
適応内
腹腔内投与
適応外
患者申出療養に係る中間報告書
1.標題
患者申出療養の
名称
パクリタキセル腹腔内投与及び静脈内投与並びにS-1内服併用療法
実施医療機関名
東京大学医学部附属病院
使用医薬品、医療
機器又は再生医療
等製品
医薬品医療 医薬品医療機器法 医薬品医療
品目名
製造販売業者名
及び連絡先
規格
機器法承認
又は
承認
又は
認証番号
認証上の適応
22100AMX
カプセル 00886000
ティーエスワ
20mg 22100AMX
社
25mg 00887000
ン配合カプセ
東京都千代田区神田
22100AMX
ル・顆粒
顆粒
錦町 1-27
20mg 00111000
(一般名 S-1)
03-3293-2451
25mg 22100AMX
00112000
大鵬薬品工業株式会
ブリストル・マイヤ
30mg/
ーズ株式会社 東京都 5mL
(パクリタキ
新宿区西新宿 6-5-1 100mg/
セル)
16.7mL
03-6705-7000
タキソール
日本化薬株式会社
パクリタキセ 東京都千代田区富士
ル注「NK」
見 1-11-2
03-3237-5051
沢井製薬株式会社
21800AMZ
10212
100mg/ 21800AMZ
16.7mL 10213
30mg/
5mL
癌、頭頸部癌、非
小細胞肺癌、手術
患者申出療養(予
定)終了日
癌、膵癌、胆道癌
有する頭頸部癌,
再発又は遠隔転移
を有する食道癌,
血管肉腫,進行又
は再発の子宮頸
平成28年10月14日
令和4年10月14日
倫理基準等の遵守
臨床研究法を遵守し、試料、記録等が適切に保存されている。
報告書作成日
令和4年 8 月 10 日
実施責任医師
石神 浩徳
実施者
石神 浩徳
問い合わせ窓口
問い合わせ先:外来化学療法部 准教授 石神 浩徳
Tel:03-3815-5411
Fax:03-3811-6822
1
1
適応内
不能又は再発乳
21800AMZ
パクリタキセ
癌,再発又は難治
大阪市淀川区宮原 510244000
ル注射液
2-30
100mg/ 21900AMX 性の胚細胞腫瘍
「サワイ」
用法:点滴静注
16.7mL 00596000
06-6105-5711
患者申出療養が告
示された日
の該当
胃癌、結腸・直腸
21700AMX 卵巣癌,非小細胞
00177000
肺癌,乳癌,胃
21700AMX 癌,子宮体癌,再
00178000
発又は遠隔転移を
30mg/
5mL
機器法上の
適応外使用
経静脈投与
適応内
腹腔内投与
適応外