よむ、つかう、まなぶ。
参考資料4:「人を対象とする生命科学・医学系研究に関する倫理指針の一部を改正する件(概要)」パブリック・コメント意見一覧 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30490.html |
| 出典情報 | 生命科学・医学系研究等における個人情報の取扱い等に関する合同会議(第8回 1/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
25
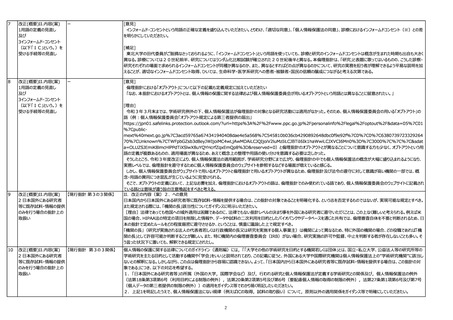
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保
有している既存試料・情報を研
究に用いる場合
【現行指針 第8の1⑵関係】
26
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保 「適切な同意」は取得できるが「IC手続を行うことが困難」というのは、どのような場合かを明確にする必要がある。
有している既存試料・情報を研
現行指針の第8の1(2)ア(ア)〇3の「インフォームド・コンセントを受けることが困難な場合」について、ガイダンスの7は12を指示している。ガイダンスの12では「研究対象者
究に用いる場合
等からインフォームド・コンセント及び適切な同意を受けることが困難である」場合として、個情法18条3項2号?4号を挙げられている。しかし、これらは「適切な同意」を受けることも困難
【現行指針 第8の1⑵関係】 である場合である。インフォームド・コンセントを受けることが困難であるが、適切な同意を受けることができる場合を、少なくともガイダンスにおいて明確にする必要がある。
27
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保
有している既存試料・情報を研
究に用いる場合
【現行指針 第8の1⑵関係】
28
29
30
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
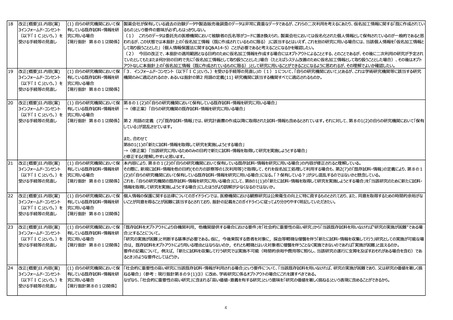
II. 改正の内容(案)3.(1)まる3への意見
「社会的に重要性の高い研究」イコール「当該既存試料を用いなければ研究の実施が困難な場合」であることの根拠として挙げられている旧疫学指針の抜粋に疑義がある。
また、同時に、「特段の理由」との関係性についても明示いただきたい。
[理由]旧疫学指針の細則(3)「当該方法によらなければ、実際上、当該疫学研究を実施できず、又は当該疫学研究の価値を著しく損ねること。」とあるが、(3)とは別に
(5)として「当該疫学研究が社会的に重要性が高いと認められるものであること。」とあり、「社会的に重要性の高い研究」と「当該既存試料を用いなければ研究の実施が困難な場
合」は別の観点なのではないか。
「特段の理由」についても、どういった場合がそれに該当するか解釈が曖昧である。
「3.インフォームド・コンセント(以下「IC」という。)を受ける手続等の見直し」の(1) 4への意見
「ICを受ける手続きを行うことが困難な場合」の項で、
倫理指針ガイダンス84P 12の個情法ガイドラインQ&Aに記載の、
「同意を取得するための時間的余裕や費用等に照らし、本人の同意を得ることにより当該研究の遂行に支障を及ぼすおそれがある場合等」について。
「同意を取得するための時間的余裕や費用等…」の判断基準は明示されないのか。
学術研究機関等に該当しない研究機関(民間病院)の研究者にとって、研究計画時にネックとなっており、施設倫理審査委員会でも仮の判断基準を設けているが、倫理指針で判
断基準が明示されるとありがたい。
(2) 他の研究機関に既存試料・ ガイダンスP105 「2「当該試料・情報の提供に関する記録」を作成し?」の4行目の【下表1】掲載されていないため、掲載をお願いしたい。
情報を提供しようとする場合
【現行指針 第8の1⑶関係】
(2) 他の研究機関に既存試料・ 現行指針第8の1(3)及び(5)におけるICを受ける手続の簡略化に関する規定の削除には賛成する。しかし、その場合でも、現行指針第8の9インフォームド・コンセントの手続き等の
情報を提供しようとする場合 【現 簡略化の規定を使えるようにすべきである。具体的には、第8の9の「1または4の規定に基づきインフォームド・コンセントの手続き等の簡略化を行うことができる」という規定は、以前の
行指針第8の1⑶関係】
「当該研究の実施について研究機関の長の許可を受けた研究計画書に定めるところにより、1及び4の規定による手続きの一部を簡略化することができる。」に戻すとともに、第8の9に
学術例外等の例外要件を定めるべきである。さらに、第8の9の規定を以前の規定に戻すことで、第8の1(1)イ(イ)②(i)や(6)の簡略化規定も削除してよいと考える。
(3) 既存試料・情報の提供を受 なぜなら、既存試料・情報の授受を伴う研究についても悉皆的な研究を行う余地を残すべきであると同時に、簡略化規程は例外的に指針第8の9に規定すればよく、第8の1に規
けて研究を実施しようとする場合 定する必要はないと考えるから。
【現行指針第8の1⑸関係】
(4) 外国にある者へ試料・情報 要配慮個人情報の取得時や外国の第三者への提供時には本人同意が必要であるにもかかわらず、新規取得の場合にも関わらず簡略化を認めるよう改めるのか、資料からだけでは理
を提供する場合 【現行指針第 解できなかった。研究結果にバイアスが生じる可能性がある等の研究である場合や悉皆性を求めるような研究である場合には、個情法違反にはならない、という事か。
8の1⑹関係】
5
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保
有している既存試料・情報を研
究に用いる場合
【現行指針 第8の1⑵関係】
26
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保 「適切な同意」は取得できるが「IC手続を行うことが困難」というのは、どのような場合かを明確にする必要がある。
有している既存試料・情報を研
現行指針の第8の1(2)ア(ア)〇3の「インフォームド・コンセントを受けることが困難な場合」について、ガイダンスの7は12を指示している。ガイダンスの12では「研究対象者
究に用いる場合
等からインフォームド・コンセント及び適切な同意を受けることが困難である」場合として、個情法18条3項2号?4号を挙げられている。しかし、これらは「適切な同意」を受けることも困難
【現行指針 第8の1⑵関係】 である場合である。インフォームド・コンセントを受けることが困難であるが、適切な同意を受けることができる場合を、少なくともガイダンスにおいて明確にする必要がある。
27
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
(1) 自らの研究機関において保
有している既存試料・情報を研
究に用いる場合
【現行指針 第8の1⑵関係】
28
29
30
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
改正(概要)II.内容(案)
3インフォームド・コンセント
(以下「IC」という。)を
受ける手続等の見直し
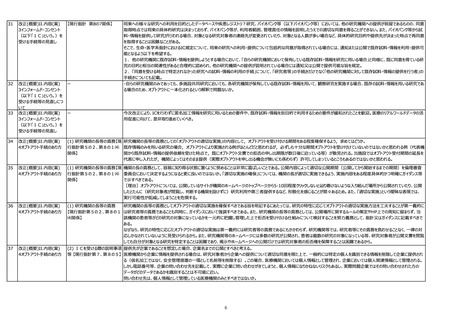
II. 改正の内容(案)3.(1)まる3への意見
「社会的に重要性の高い研究」イコール「当該既存試料を用いなければ研究の実施が困難な場合」であることの根拠として挙げられている旧疫学指針の抜粋に疑義がある。
また、同時に、「特段の理由」との関係性についても明示いただきたい。
[理由]旧疫学指針の細則(3)「当該方法によらなければ、実際上、当該疫学研究を実施できず、又は当該疫学研究の価値を著しく損ねること。」とあるが、(3)とは別に
(5)として「当該疫学研究が社会的に重要性が高いと認められるものであること。」とあり、「社会的に重要性の高い研究」と「当該既存試料を用いなければ研究の実施が困難な場
合」は別の観点なのではないか。
「特段の理由」についても、どういった場合がそれに該当するか解釈が曖昧である。
「3.インフォームド・コンセント(以下「IC」という。)を受ける手続等の見直し」の(1) 4への意見
「ICを受ける手続きを行うことが困難な場合」の項で、
倫理指針ガイダンス84P 12の個情法ガイドラインQ&Aに記載の、
「同意を取得するための時間的余裕や費用等に照らし、本人の同意を得ることにより当該研究の遂行に支障を及ぼすおそれがある場合等」について。
「同意を取得するための時間的余裕や費用等…」の判断基準は明示されないのか。
学術研究機関等に該当しない研究機関(民間病院)の研究者にとって、研究計画時にネックとなっており、施設倫理審査委員会でも仮の判断基準を設けているが、倫理指針で判
断基準が明示されるとありがたい。
(2) 他の研究機関に既存試料・ ガイダンスP105 「2「当該試料・情報の提供に関する記録」を作成し?」の4行目の【下表1】掲載されていないため、掲載をお願いしたい。
情報を提供しようとする場合
【現行指針 第8の1⑶関係】
(2) 他の研究機関に既存試料・ 現行指針第8の1(3)及び(5)におけるICを受ける手続の簡略化に関する規定の削除には賛成する。しかし、その場合でも、現行指針第8の9インフォームド・コンセントの手続き等の
情報を提供しようとする場合 【現 簡略化の規定を使えるようにすべきである。具体的には、第8の9の「1または4の規定に基づきインフォームド・コンセントの手続き等の簡略化を行うことができる」という規定は、以前の
行指針第8の1⑶関係】
「当該研究の実施について研究機関の長の許可を受けた研究計画書に定めるところにより、1及び4の規定による手続きの一部を簡略化することができる。」に戻すとともに、第8の9に
学術例外等の例外要件を定めるべきである。さらに、第8の9の規定を以前の規定に戻すことで、第8の1(1)イ(イ)②(i)や(6)の簡略化規定も削除してよいと考える。
(3) 既存試料・情報の提供を受 なぜなら、既存試料・情報の授受を伴う研究についても悉皆的な研究を行う余地を残すべきであると同時に、簡略化規程は例外的に指針第8の9に規定すればよく、第8の1に規
けて研究を実施しようとする場合 定する必要はないと考えるから。
【現行指針第8の1⑸関係】
(4) 外国にある者へ試料・情報 要配慮個人情報の取得時や外国の第三者への提供時には本人同意が必要であるにもかかわらず、新規取得の場合にも関わらず簡略化を認めるよう改めるのか、資料からだけでは理
を提供する場合 【現行指針第 解できなかった。研究結果にバイアスが生じる可能性がある等の研究である場合や悉皆性を求めるような研究である場合には、個情法違反にはならない、という事か。
8の1⑹関係】
5