よむ、つかう、まなぶ。
資料2-6 サリドマイド登録システム(SMUD)年次報告書の公開について[1.4MB] (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40727.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
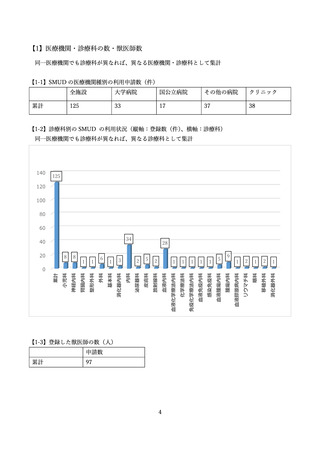
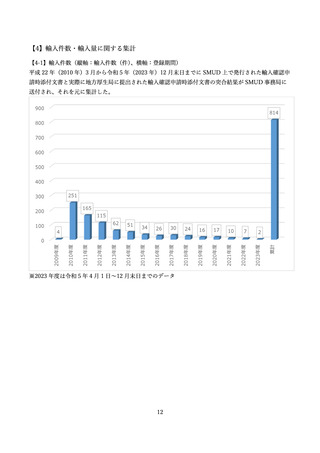
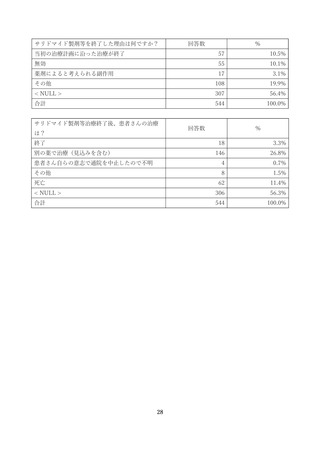
【6】投与終了時の患者情報の集計
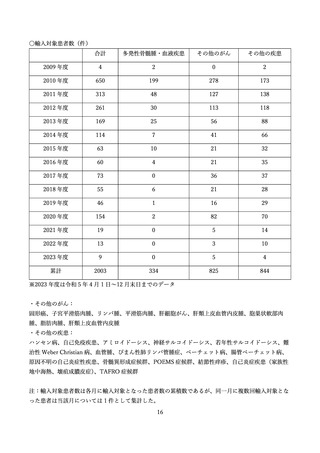
投与終了登録患者は 588 名であったが、そのうち、患者登録をしたが、一度もサリドマイド製剤等を
投与することなく治療終了となった患者が 44 名存在したため、投与終了時の患者情報の集計は、患
者登録をしたが、一度もサリドマイド製剤等を投与することなく治療終了となった患者を除く、544 名
について行った。
【6-1】患者一人あたりのサリドマイド製剤等の平均投与期間と平均一日投与量に関する集計
平均投与期間(日間)
480.8
平均一日投与量(mg)
85.7
【6-2】サリドマイド製剤等と因果関係が否定できない有害事象(副作用の疑い)の発生に関する集計
【6-2A】副作用の疑いの発生に関する集計
例数
%
あり
144
26.5%
なし
400
73.5%
合計
544
100.0%
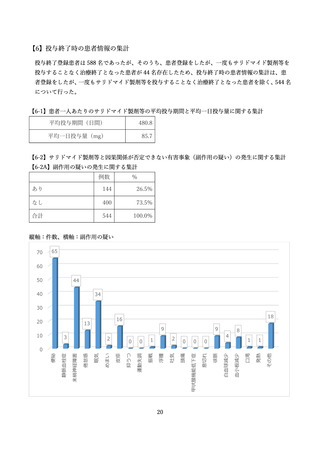
縦軸:件数、横軸:副作用の疑い
70
65
60
50
44
40
34
30
2
0
0
0
4
8
1
1
発熱
1
息切れ
0
甲状腺機能低下症
0
9
頭痛
2
振戦
3
運動失調
9
口渇
13
10
18
16
抑うつ
20
20
その他
血小板減少
白血球減少
徐脈
吐気
浮腫
皮疹
めまい
眠気
倦怠感
末梢神経障害
静脈血栓症
便秘
0
投与終了登録患者は 588 名であったが、そのうち、患者登録をしたが、一度もサリドマイド製剤等を
投与することなく治療終了となった患者が 44 名存在したため、投与終了時の患者情報の集計は、患
者登録をしたが、一度もサリドマイド製剤等を投与することなく治療終了となった患者を除く、544 名
について行った。
【6-1】患者一人あたりのサリドマイド製剤等の平均投与期間と平均一日投与量に関する集計
平均投与期間(日間)
480.8
平均一日投与量(mg)
85.7
【6-2】サリドマイド製剤等と因果関係が否定できない有害事象(副作用の疑い)の発生に関する集計
【6-2A】副作用の疑いの発生に関する集計
例数
%
あり
144
26.5%
なし
400
73.5%
合計
544
100.0%
縦軸:件数、横軸:副作用の疑い
70
65
60
50
44
40
34
30
2
0
0
0
4
8
1
1
発熱
1
息切れ
0
甲状腺機能低下症
0
9
頭痛
2
振戦
3
運動失調
9
口渇
13
10
18
16
抑うつ
20
20
その他
血小板減少
白血球減少
徐脈
吐気
浮腫
皮疹
めまい
眠気
倦怠感
末梢神経障害
静脈血栓症
便秘
0