よむ、つかう、まなぶ。
【資料1】新型コロナワクチン接種後の遷延する症状への対応について(感染症対策部提出資料)[3.3MB] (52 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41120.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第16回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
新型コロナワクチンの接種後の遷延する症状について
第98回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和5年度第
11回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
2023(令和5)年10月27日
資料
1-8
抜粋
○ 新型コロナワクチン接種後の遷延する症状に関する実態調査第二報(医師宛調査)において、症状の持続期間が31日、61日以上等であった症
例について調査結果の報告があったことも踏まえ、令和2年度厚生労働行政推進調査事業として実施した新型コロナワクチンの投与開始初期の
重点的調査(対象者:医療従事者等、ワクチンの種別等:コミナティ筋注、初回シリーズ)において、症状の持続期間が31日以上であったと報
告された事例がどの程度存在したか、分析を行った。
〇 さらに、3回目以降の接種については、上記事業に加え、令和3年度新型コロナワクチン追加接種並びに適応拡大にかかわる免疫持続性および
安全性調査(対象者:医療従事者等、ワクチンの種別等:初回接種コミナティ筋注またはスパイクバックス筋注、追加接種コミナティ筋注また
はスパイクバックス筋注)において症状の持続期間が31日以上であったと報告された事例がどの程度存在したか、追加分析を行うこととした。
令和2年度新型コロナワクチンの投与開始初期の重点的調査(コホート調査)および
令和3年度新型コロナワクチン追加接種並びに適応拡大にかかわる免疫持続性および安全性調査(コホート調査)
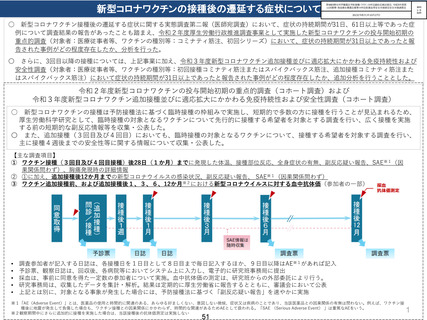
○ 新型コロナワクチンの接種は予防接種法に基づく臨時接種の枠組みで実施し、短期的で多数の方に接種を行うことが見込まれるため、
厚生労働科学研究として、臨時接種の対象となるワクチンについて先行的に接種する希望者を対象とする調査を行い、広く接種を実施
する前の短期的な副反応情報等を収集・公表した。
〇 また、追加接種(3回目及び4回目)においても、臨時接種の対象となるワクチンについて、接種する希望者を対象する調査を行い、
主に接種4週後までの安全性等に関する情報について収集・公表した。
【主な調査項目】
① ワクチン接種(3回目及び4回目接種)後28日(1か月)までに発現した体温、接種部位反応、全身症状の有無、副反応疑い報告、SAE※1(因
果関係問わず)、胸痛発現時の詳細情報
② ①に加え、追加接種後12か月までの新型コロナウイルスの感染状況、副反応疑い報告、 SAE※1(因果関係問わず)
③ ワクチン追加接種前、および追加接種後1、3、6、12か月※2における新型コロナウイルスに対する血中抗体価(参加者の一部)
•
•
•
•
•
調査参加者が記入する日誌は、各接種日を1日目として8日目まで毎日記入するほか、9日目以降はAE※1があれば記入
予診票、観察日誌は、回収後、各病院等においてシステム上に入力し、電子的に研究班事務局に提出
採血は、事前に同意を得た一定数の参加者について実施。血中抗体価の測定は、研究班からの外部委託により行う。
研究事務局は、収集したデータを集計・解析。結果は定期的に厚生労働省に報告するとともに、審議会において公表
上記とは別に、対象となる事象が発生した場合には、予防接種法に基づく「副反応疑い報告」を速やかに実施
※1「AE(Adverse Event)」とは、医薬品の使用と時間的に関連のある、あらゆる好ましくない、意図しない徴候、症状又は疾病のことであり、当該医薬品との因果関係の有無は問わない。例えば、ワクチン接
種後に地震が発生して負傷した場合も、ワクチン接種との因果関係にかかわらず、時間的な関連があるためAEとして扱われる。「SAE (Serious Adverse Event) 」は重篤なAEをいう。
※2観察期間中にさらに追加的に接種を実施した場合は、当該接種後の抗体価測定は実施しない
51
1
第98回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和5年度第
11回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
2023(令和5)年10月27日
資料
1-8
抜粋
○ 新型コロナワクチン接種後の遷延する症状に関する実態調査第二報(医師宛調査)において、症状の持続期間が31日、61日以上等であった症
例について調査結果の報告があったことも踏まえ、令和2年度厚生労働行政推進調査事業として実施した新型コロナワクチンの投与開始初期の
重点的調査(対象者:医療従事者等、ワクチンの種別等:コミナティ筋注、初回シリーズ)において、症状の持続期間が31日以上であったと報
告された事例がどの程度存在したか、分析を行った。
〇 さらに、3回目以降の接種については、上記事業に加え、令和3年度新型コロナワクチン追加接種並びに適応拡大にかかわる免疫持続性および
安全性調査(対象者:医療従事者等、ワクチンの種別等:初回接種コミナティ筋注またはスパイクバックス筋注、追加接種コミナティ筋注また
はスパイクバックス筋注)において症状の持続期間が31日以上であったと報告された事例がどの程度存在したか、追加分析を行うこととした。
令和2年度新型コロナワクチンの投与開始初期の重点的調査(コホート調査)および
令和3年度新型コロナワクチン追加接種並びに適応拡大にかかわる免疫持続性および安全性調査(コホート調査)
○ 新型コロナワクチンの接種は予防接種法に基づく臨時接種の枠組みで実施し、短期的で多数の方に接種を行うことが見込まれるため、
厚生労働科学研究として、臨時接種の対象となるワクチンについて先行的に接種する希望者を対象とする調査を行い、広く接種を実施
する前の短期的な副反応情報等を収集・公表した。
〇 また、追加接種(3回目及び4回目)においても、臨時接種の対象となるワクチンについて、接種する希望者を対象する調査を行い、
主に接種4週後までの安全性等に関する情報について収集・公表した。
【主な調査項目】
① ワクチン接種(3回目及び4回目接種)後28日(1か月)までに発現した体温、接種部位反応、全身症状の有無、副反応疑い報告、SAE※1(因
果関係問わず)、胸痛発現時の詳細情報
② ①に加え、追加接種後12か月までの新型コロナウイルスの感染状況、副反応疑い報告、 SAE※1(因果関係問わず)
③ ワクチン追加接種前、および追加接種後1、3、6、12か月※2における新型コロナウイルスに対する血中抗体価(参加者の一部)
•
•
•
•
•
調査参加者が記入する日誌は、各接種日を1日目として8日目まで毎日記入するほか、9日目以降はAE※1があれば記入
予診票、観察日誌は、回収後、各病院等においてシステム上に入力し、電子的に研究班事務局に提出
採血は、事前に同意を得た一定数の参加者について実施。血中抗体価の測定は、研究班からの外部委託により行う。
研究事務局は、収集したデータを集計・解析。結果は定期的に厚生労働省に報告するとともに、審議会において公表
上記とは別に、対象となる事象が発生した場合には、予防接種法に基づく「副反応疑い報告」を速やかに実施
※1「AE(Adverse Event)」とは、医薬品の使用と時間的に関連のある、あらゆる好ましくない、意図しない徴候、症状又は疾病のことであり、当該医薬品との因果関係の有無は問わない。例えば、ワクチン接
種後に地震が発生して負傷した場合も、ワクチン接種との因果関係にかかわらず、時間的な関連があるためAEとして扱われる。「SAE (Serious Adverse Event) 」は重篤なAEをいう。
※2観察期間中にさらに追加的に接種を実施した場合は、当該接種後の抗体価測定は実施しない
51
1